Презентація по темі: "Кислоти"
Про матеріал
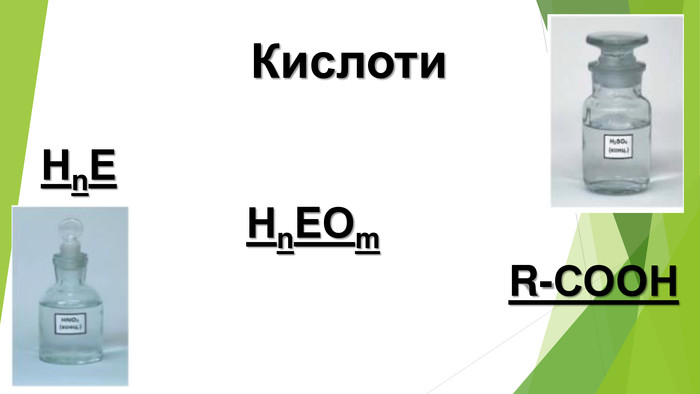
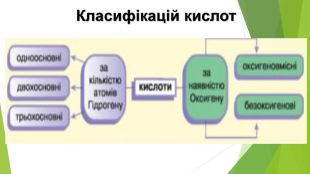
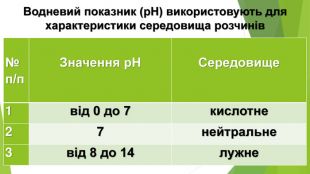
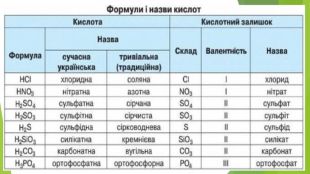
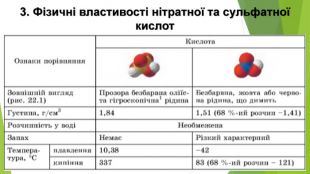
Презентація по темі: "Кислоти".
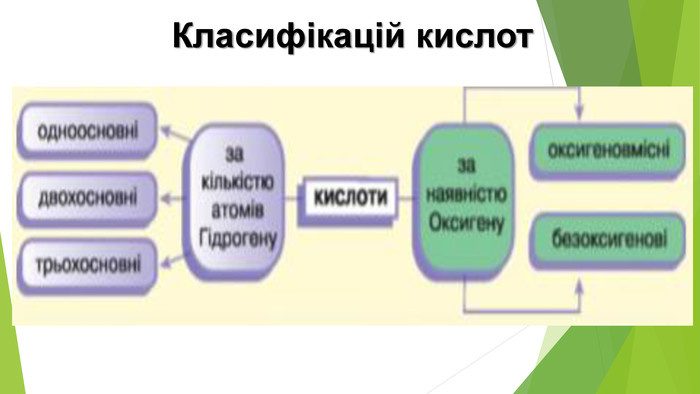
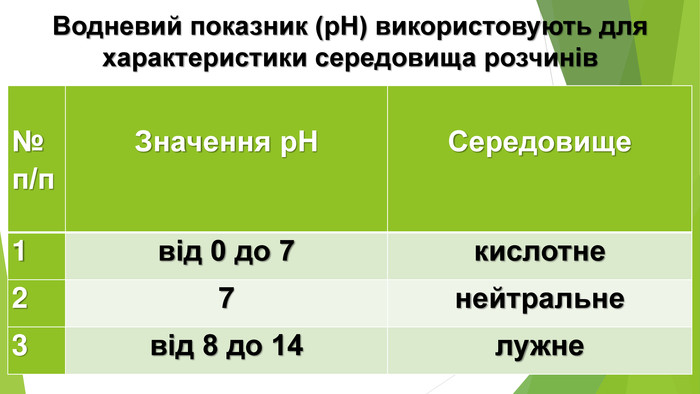
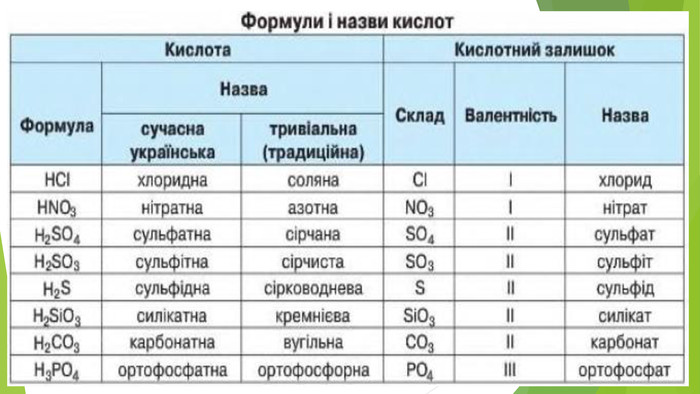
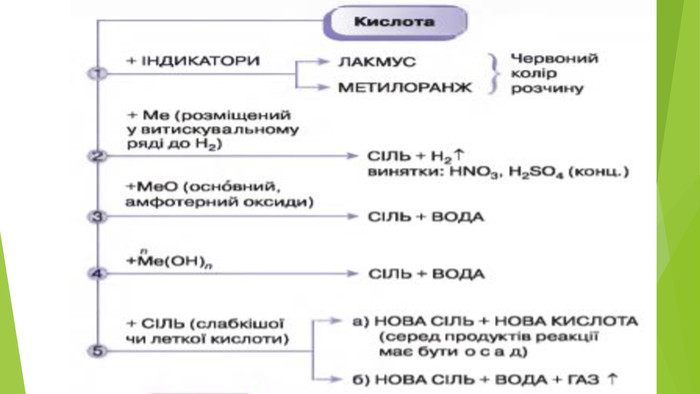
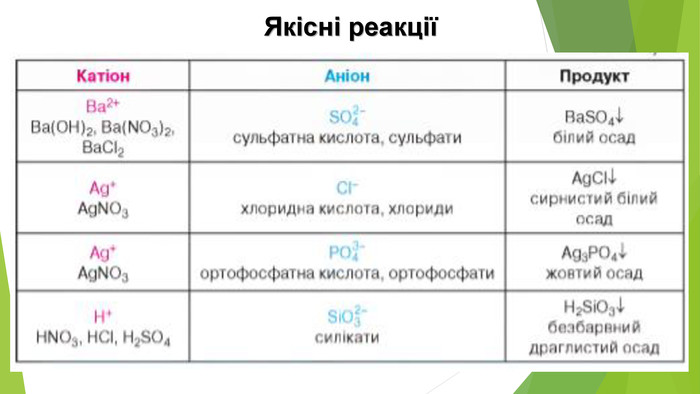
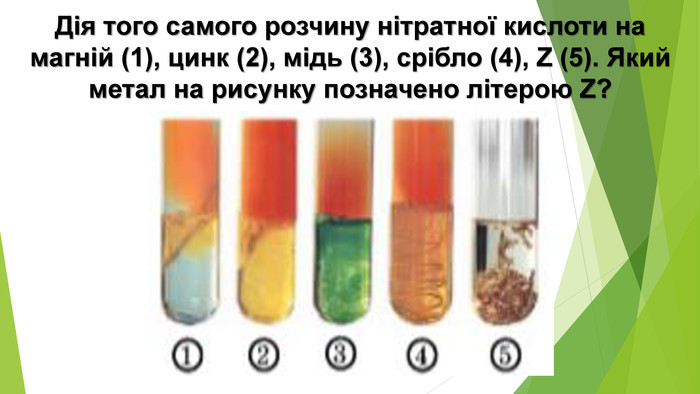
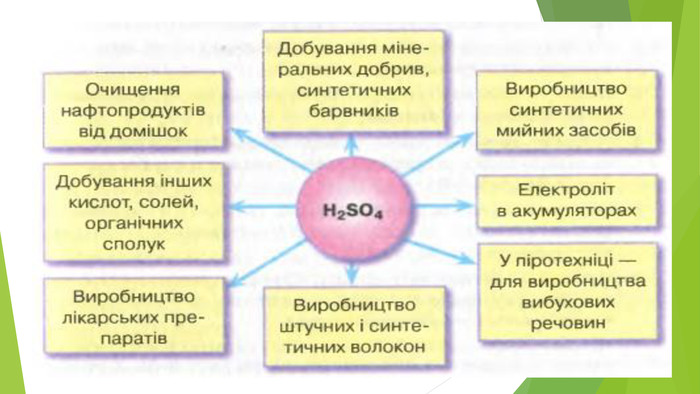
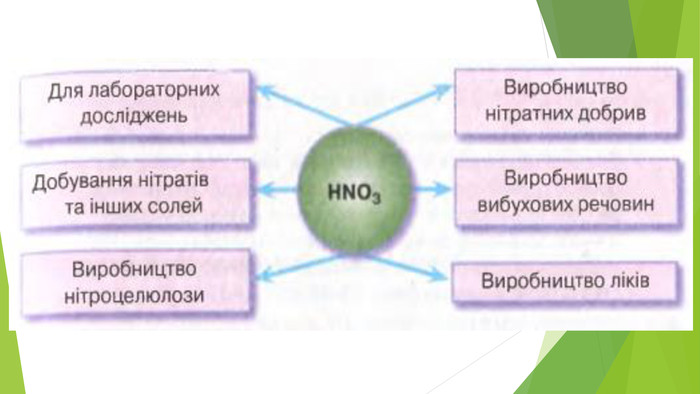
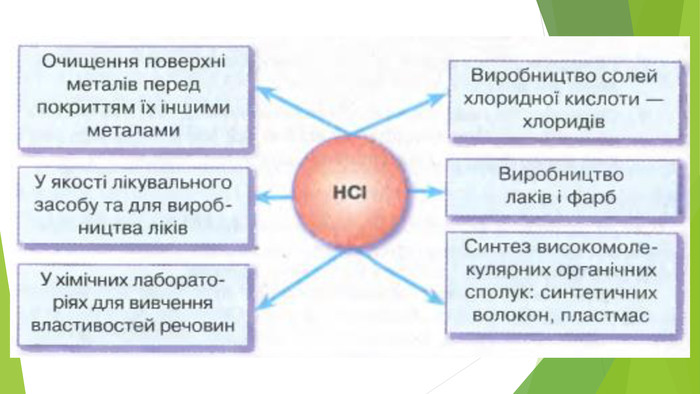
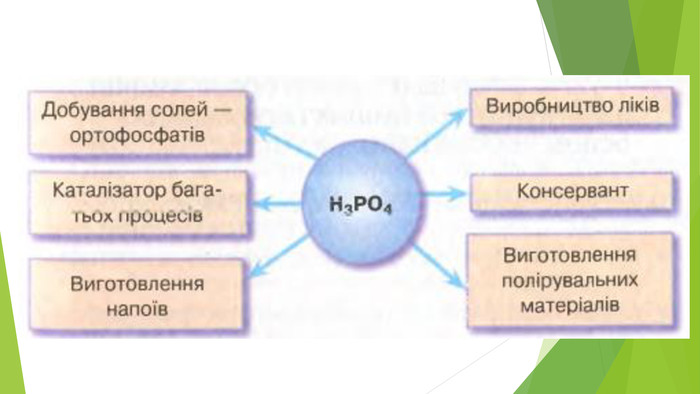
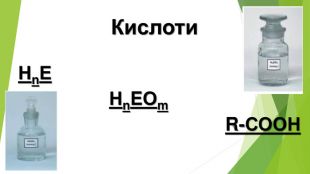
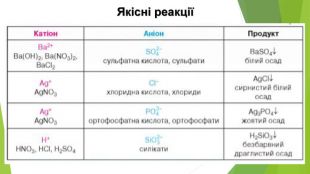
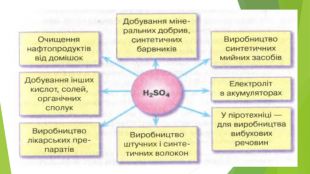
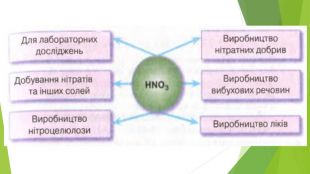
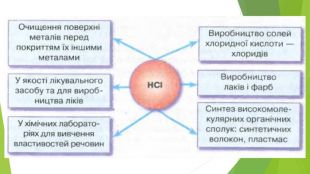
Містить матеріали про загальні фізичні та хімічні властивості кислот, їх назви і застосування. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку






















-

Стоян Любов Віталіївна
18.01.2024 в 16:40
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Товстолес Лариса
11.01.2023 в 22:37
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Велика Наталія Миколаївна
02.02.2022 в 18:07
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Dyrbaba Olga
29.04.2020 в 20:08
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук