Презентація по темі: "Кислотні дощі"
Презентація по темі: "Кислотні дощі".
Утворення кислотних дощів та їх шкідлива дія.
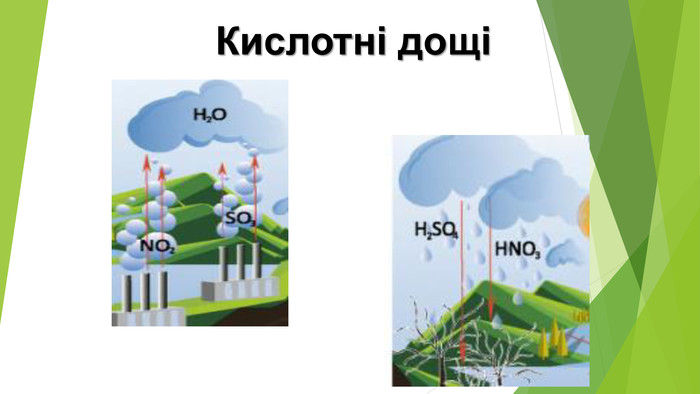

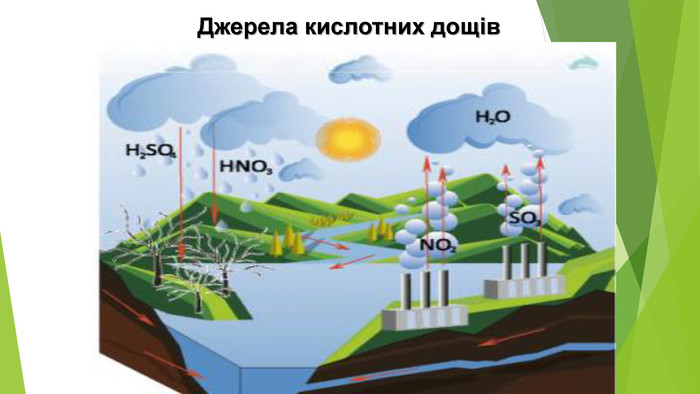









1. ПОНЯТТЯ ПРО КИСЛОТНІ ДОЩІ ТА ПРИЧИНИ ЇХ ВИНИКНЕННЯ. Кислотні дощі — це всі види опадів (дощ, сніг, град, туман), кислотність яких нижча за 5,5. Хімічний аналіз кислотних дощів показує наявність у них сульфітної, сульфатної, нітритної, нітратної кислот. Поява цих речовин в опадах — наслідок забруднення атмосфери оксидами Сульфуру та Нітрогену.{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A} №п/п. Значення р. НСередовище1від 0 до 7кислотне27нейтральне3від 8 до 14лужне
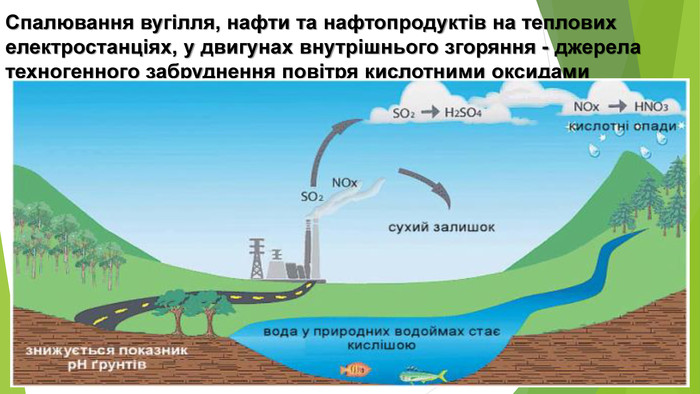
2. ҐРУНТИ Й КИСЛОТНІ ДОЩІ. Ґрунти теж потерпають від кислотних дощів: знижується родючість ґрунту, змінюється склад ґрунтових мікроорганізмів, погіршується доступність поживних речовин для рослин. Кислотність ґрунтів — властивість, зумовлена наявністю в ґрунтовому розчині катіонів Гідрогену Н+. Кислотні ґрунти — це ґрунти, p. H яких менше від 7, нейтральні — близько 7, а лужні — понад 7. Як вам відомо, для визначення точного показника кислотності використовують p. H-метри, а також спеціальні електронні прилади. Доступним для вас є спосіб визначення кислотності за допомогою універсального індикаторного папірця. Порівнюючи його колір у досліджуваному середовищі зі шкалою, з’ясовують, кислотним, лужним чи нейтральним воно є.
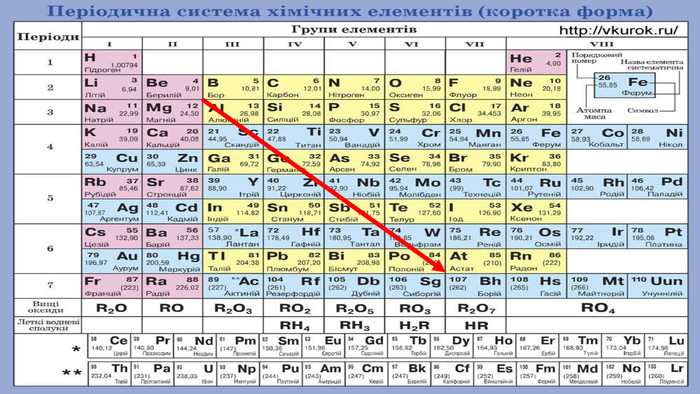
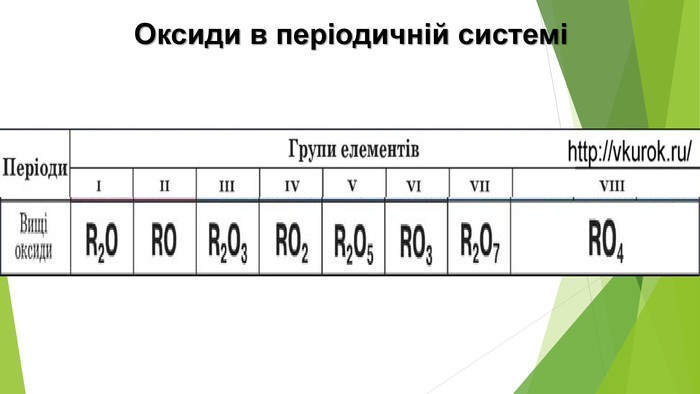
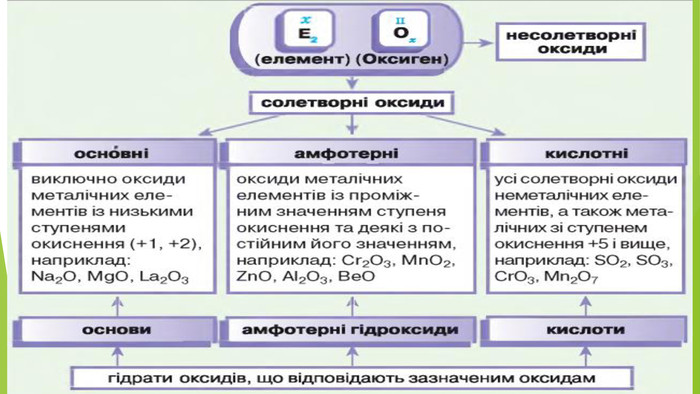
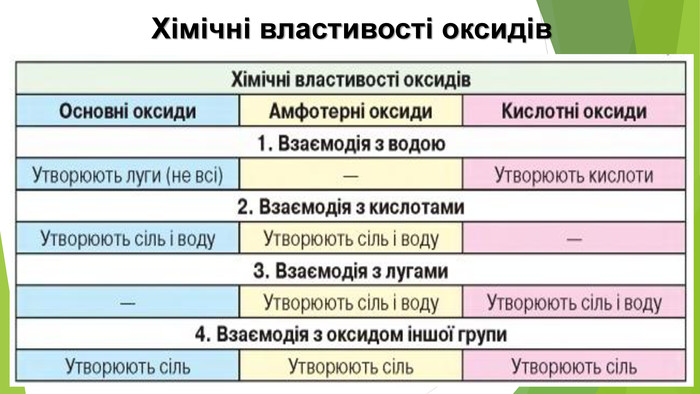
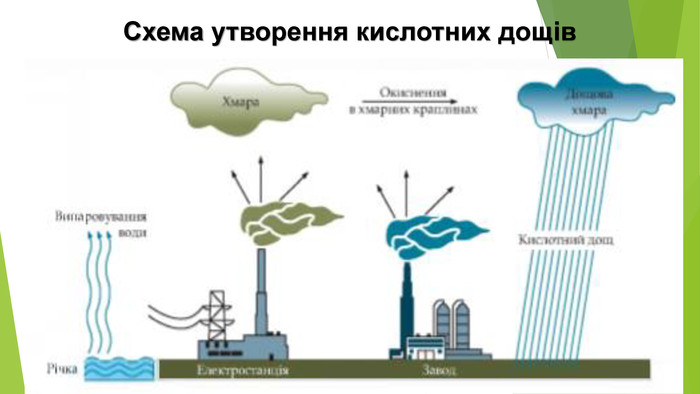
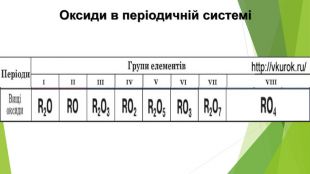
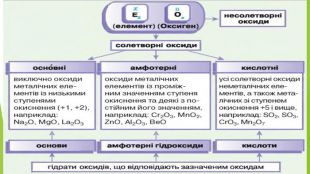
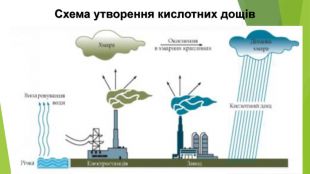
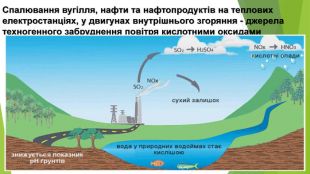
3. ЯК ВИНИКАЮТЬ КИСЛОТНІ ОПАДИКислотний дощ утворюється в атмосфері в результаті реакції між водяною парою й такими забруднювальними речовинами, як сульфур(ІV) оксид SО2, сульфур(VІ) оксид SО3, нітроген(ІV) оксид NО2. Це кислотні оксиди, тому продуктами реакцій з водою є сульфатна, сульфітна, нітратна, нітритна кислоти.
4. НАСЛІДКИ КИСЛОТНИХ ОПАДІВКислотні опади завдають значної шкоди довкіллю. Вони зменшують урожаї сільськогосподарських культур, спричиняють різні захворювання у тварин і людей, руйнування будівель і пам’ятників із мармуру та вапняку, корозію металевих виробів. Запобігти утворенню оксидів Нітрогену можна, знизивши температуру згоряння палива і пального. З метою зменшення викидів сірчистого газу в атмосферу теплоелектростанціями перевагу віддають паливу з меншим вмістом Сульфуру, а відпрацьовані гази очищають від сульфур(ІV) оксиду пропусканням крізь водну суспензію кальцій гідроксиду чи розпилюють у них негашене вапно.
5. ШЛЯХИ ВИРІШЕННЯ ПРОБЛЕМИ КИСЛОТНИХ ДОЩІВ. Щоб за побігти кислотним дощам, необхідно скорочувати викиди кислотоутворювальних речовин в атмосферу: установлювати пиловловлювачі й фільтри для очищення газоподібних викидів, викликаних антропогенними чинниками; користуватись високоякісним пальним для автомобілів, застосовувати альтернативні джерела енергії, упроваджувати безвідходні технології, застосовувати фізико-хімічні і хімічні методи очищення викидів в атмосферу, і в перспективі — створення екологічно безпечних виробництв. Якщо концентрація оксидів-забруднювачів у повітрі збільшується, то кислотні дощі створюють реальну загрозу людині, рослинному й тваринному світу. Дощова вода, що утворюється в результаті конденсації водяної пари, мала б нейтральне середовище. Проте і в дуже чистому повітрі завжди є вуглекислий газ, і водневий показник дощової води, у якій він розчиняється, дорівнює 5,6-5,7. Очищення промислових викидів не тільки захищає атмосферу від забруднень, а й дає додаткову сировину підприємствам. Наприклад, уловлювання сірки з газових відходів металургійних комбінатів забезпечує санітарне очищення та здешевлює отримання додаткової кількості сульфатної кислоти. У перспективі — створення екологічно безпечних виробництв, у цілому всі нові технології повинні впроваджуватися тільки після оцінки їх впливу на навколишнє середовище. Поступовий перехід на екологічні електромобілі, більш широке використання електротранспорту (тролейбусів, трамваїв, метрополітену), також буде кроком на шляху до подолання проблеми виникнення кислотних дощів. Проблема убезпечення Землі від кислотних дощів є інтернаціональною. Адже повітряні течії розносять кислотні хмари й тумани на тисячі кілометрів від місць їх виникнення. Тому всі люди повинні дбати про чистоту повітря.
1. Наведіть приклади класифікацій кислот з неорганічної й органічної хімії. 2. Поясніть суть кислотних дощів. 3. Назвіть антропогенні й природні причини появи в атмосфері оксидів неметалічних елементів.4. Чим небезпечні кислотні дощі?5. Із переліку наведених формул виберіть і класифікуйте формули кислот: NH3, НСІ, H2 SО4, Na2 SО3, Cu(OH)2, Н3 РО4, H2 S, HNО3, NО2.6. Є речовини: літій оксид, нітратна кислота, купрум(ІІ) гідроксид, ферум(ІІ) оксид, кальцій гідроксид, сульфатна кислота, барій хлорид, цинк сульфат, карбон(ІV) оксид. Які з цих речовин взаємодіятимуть із хлоридною кислотою? Складіть рівняння можливих реакцій. 7. Обчисліть середню молярну масу та густину за воднем суміші оксидів Карбону, якщо об’єм чадного газу в ній втричі більший за об’єм вуглекислого газу. 8. На спалювання 3,8 г суміші метану і чадного газу витрачено 10,4 г кисню. Обчисліть маси газів у суміші.9. Елемент VI групи утворює два оксиди. Один з них містить 50 % Оксигену за масою і має відносну молекулярну масу, що в 1,25 раза менша за відносну молекулярну масу іншого оксиду. Виведіть формули оксидів.10. Обчисліть, чи вистачить кисню об’ємом 140 л (н. у.) для добування алюміній оксиду кількістю речовини 2 моль. 11. Визначте масу магній карбонату, яку необхідно розкласти, щоб утвореного вуглекислого газу (н. у.) вистачило для взаємодії з кальцій гідроксидом масою 3,7г.


про публікацію авторської розробки
Додати розробку














-

Клепікова Ольга Анатоліївна
15.03.2026 в 23:06
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Перестюк Софія
23.05.2023 в 19:00
Дякую!!!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Осіпчук Валентина
17.12.2022 в 21:39
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Гаріян Тетяна Михайлівна
31.01.2022 в 21:27
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Панькевич Ірина Сергіївна
02.03.2021 в 19:39
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ракочий Вєліна Костянтинівна
03.05.2020 в 19:50
Дуже дякую! Дуже гарна презентація, повністю відповідає темі і чудово підходить до уроку, як в звичайних умовах, так і в умовах дистанційного навчання.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 3 відгука