Презентація "Використання інноваційних методів навчання на уроках хімії. За і проти"
Про матеріал
В майстер - класі використані такі методи:
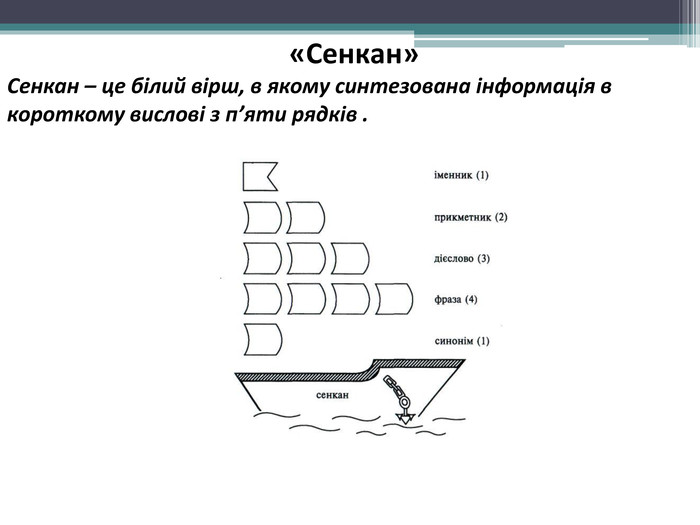
сенкан, кубування, "Ромашка Блума", метод "Шести капелюхів".
Наведені приклади використання даних методів під час викладання уроків хімії. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку