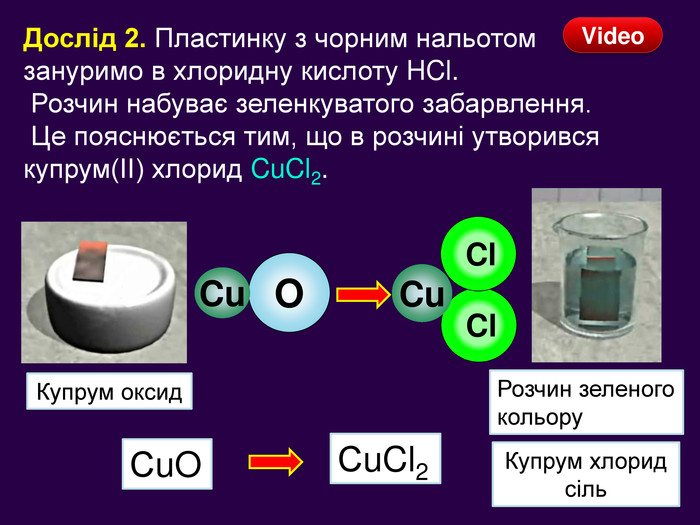
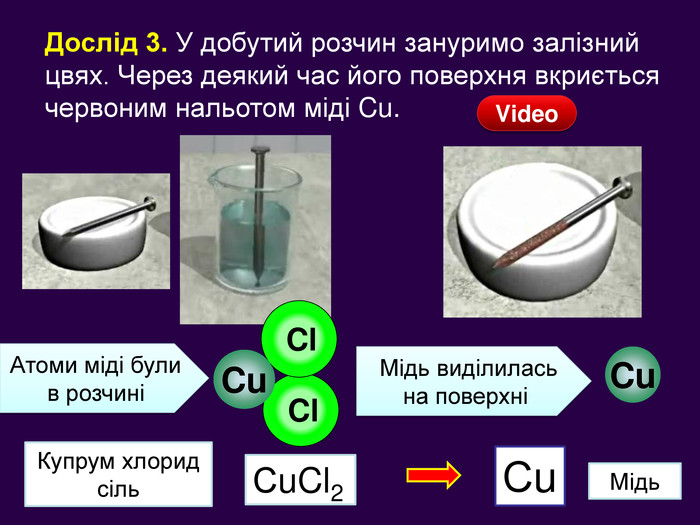
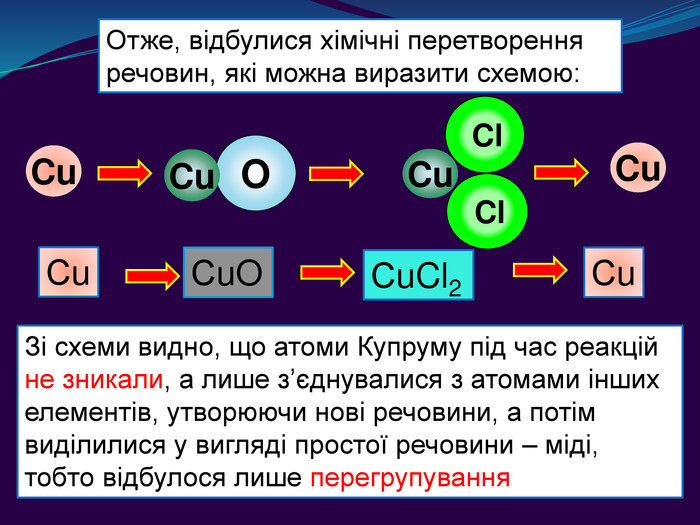
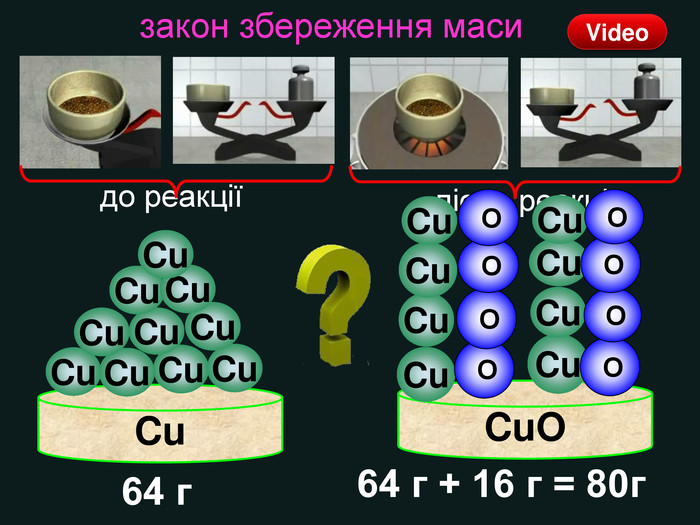
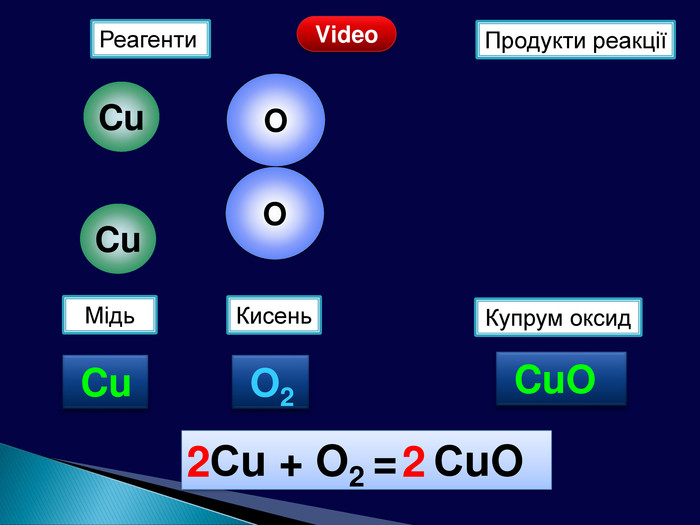
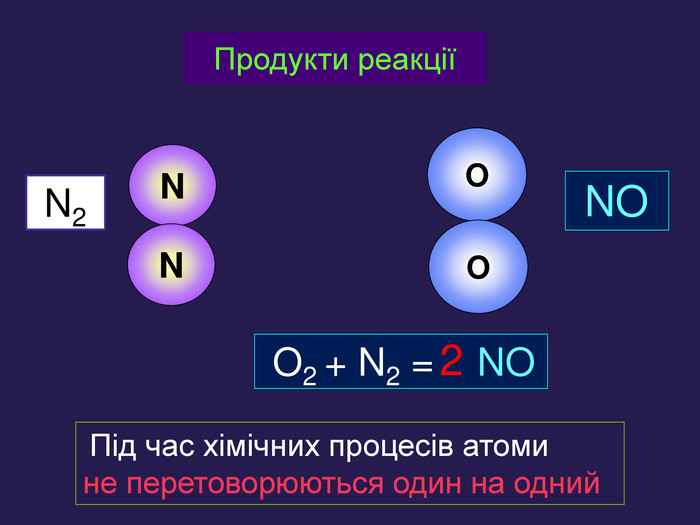
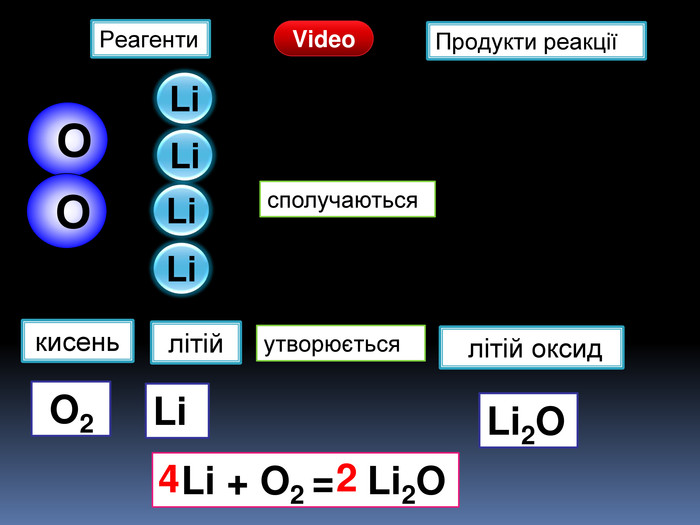
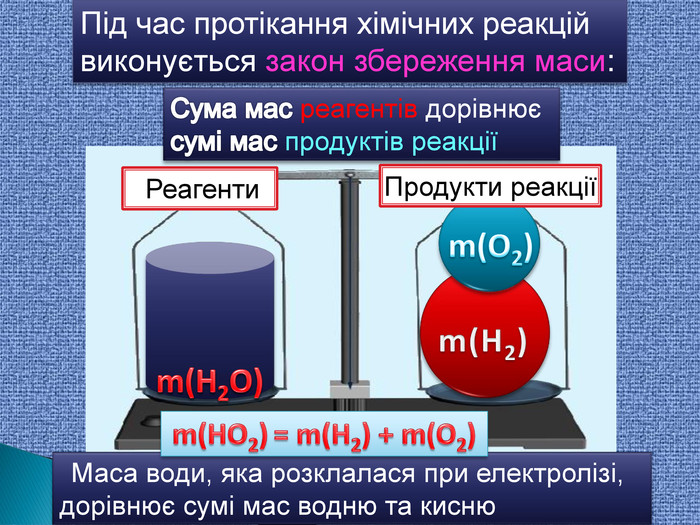
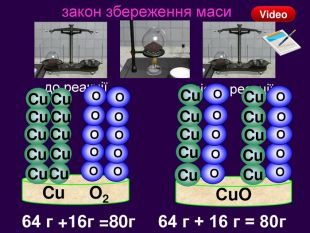
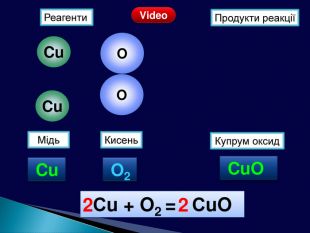
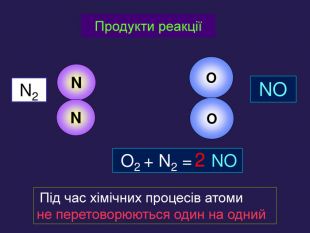
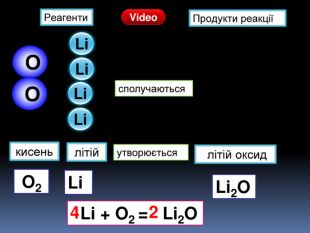
Презентація «Закон збереження маси» 7 клас
Про матеріал
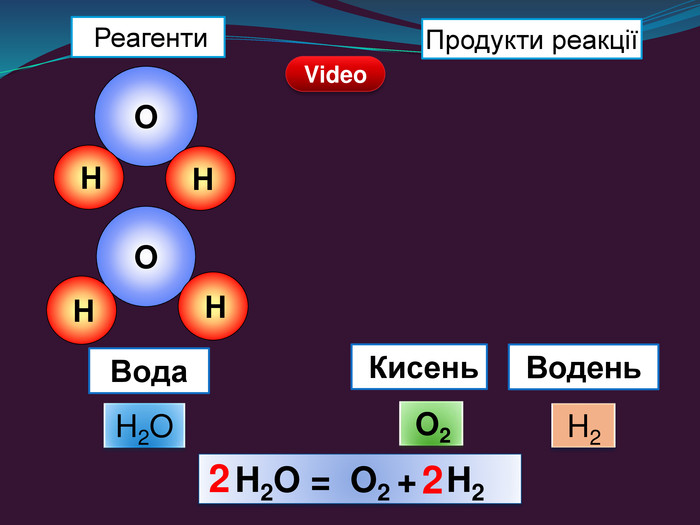
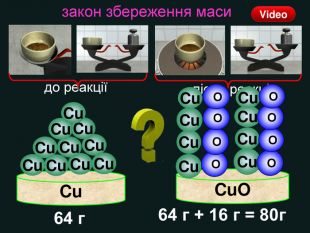
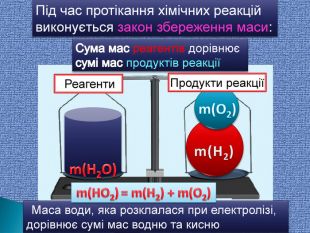
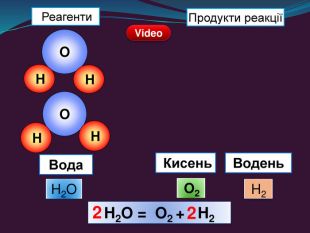
| Презентація допоможе учням та вчителю провести урок на тему «Закон збереження маси речовин під час хімічних реакцій». |
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку