Презентація "Значення води і водних розчинів у природі та житті людини"


















Вірю - не вірю- Усі речовини добре розчиняються у воді.- За збільшення температури розчинність речовин збільшується.- Вода, цукор, пісок — добре розчиняються у воді.- Крейда, пісок у воді не розчиняються.- Щоб швидше розчинити сіль, її треба подрібнити.- Щоб швидше розчинити цукор, воду треба нагріти.- Природна питна вода блакитного кольору, кисла на смак.- Та речовина, яка розчиняється у воді, називається розчинником.- Газоподібні речовини у воді не розчиняються. Проблемне запитання «Чи потрібно охороняти воду, адже її так багато?»
"Аguа" в перекладі з латинської мови означає "вода". Як алфавіт починається з букви "а", так життя починається з води. Вода міститься в кожній людині, тварині і рослині і йде з них тільки разом із життям. Ось чому девіз уроку "Вода - це життя!". Ото ж сьогодні ми проведемо розмову про добре відому, а водночас і найзагадковішу речовину - воду. Наша мета - з'ясувати її роль у нашому житті. Здавалося б, що нового і цікавого можна дізнатися про один з найважливіших мінералів Землі - про воду? Ми занадто звикли до води, занадто звичні для нас дощ, течії річок, гладь озер і морів. Життя на Землі зародилося з води. Вона стала первинним середовищем для еволюції органічного світу і входить до складу всіх живих істот. Очевидно звідси і походять вислови "Вода - чудо природи", "Вода - еліксир життя". Воду вивчають фізики, біологи, географи. Не менш важливою є вода і для хімії.
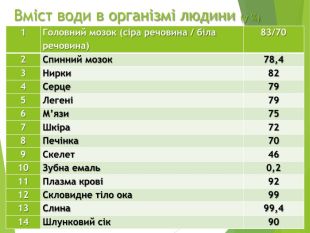
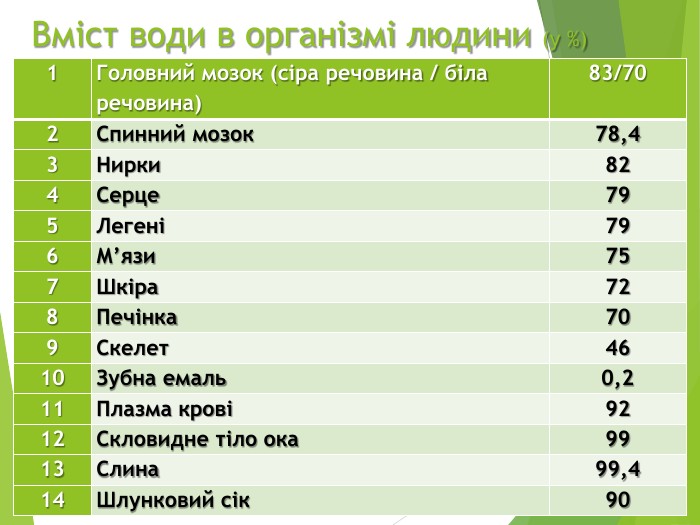
Вміст води в організмі людини (у %){5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}1 Головний мозок (сіра речовина / біла речовина)83/702 Спинний мозок78,43 Нирки824 Серце795 Легені796 М’язи757 Шкіра728 Печінка709 Скелет4610 Зубна емаль0,211 Плазма крові9212 Скловидне тіло ока9913 Слина99,414 Шлунковий сік90
У тілі здорової дорослої людини, і при нормальній вазі, міститься близько 2/3 води, тобто понад 40 літрів води на 70 кг людини. Частка води в організмі з віком зменшується:{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}97%у плода80%у новонароджених75%у немовлят70%у дітей61%у дорослих чоловіків51%у дорослих жінок45%у літніх людей
Обмін інформацією - БІОЛОГІЯВода відіграє унікальну роль як речовина, що визначає можливість існування і саме життя всіх істот на Землі. Вона виконує роль універсального розчинника, в якому відбуваються основні біохімічні процеси живих організмів. Обмін інформацією - ГЕОГРАФІЯБлизько 71% поверхні Землі вкрито водою (океани, моря, озера, річки, льодовики). На Землі приблизно 96,5% води припадає на океани, 1,7% світових запасів становлять ґрунтові води, ще 1,7% — льодовики та крижані шапки Антарктиди і Гренландії, невелика частина міститься в річках, озерах і болотах, 0,001% — у хмарах (утворюються зі зважених у повітрі часток льоду й рідкої води). Велика частина земної води — солона, непридатна для сільського господарства й пиття. Значення води в організміВода, будучи основною складовою всіх рідин організму, зокрема крові, в якій понад 90% міститься саме її, виконує такі основні функції:- регуляція температури тіла;- виведення шлаків, токсинів і продуктів життєдіяльності;- транспорт поживних речовин і кисню;- засвоєння і перетравлення продуктів харчування;- транспортна функція;- амортизація суглобів та запобігання їх тертя;- підтримка структур клітин;- захист тканин і внутрішніх органів
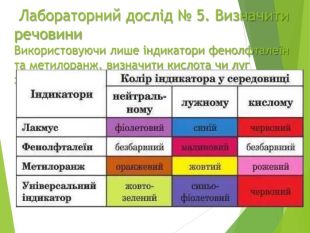
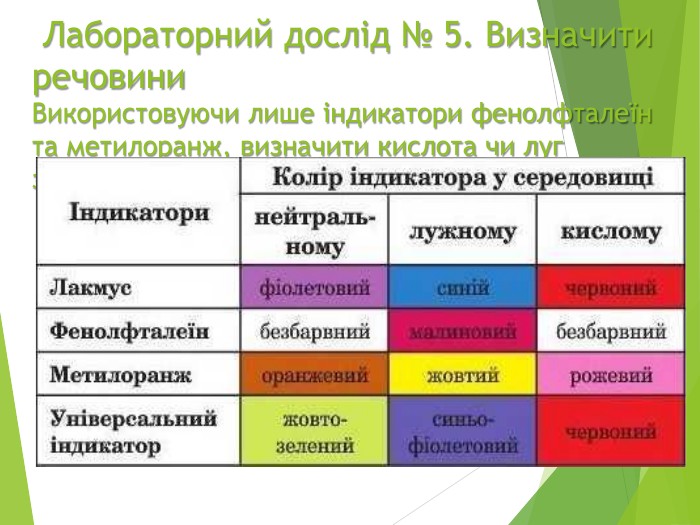
Інструктаж з БЖД при роботі з кислотами і лугами. При попаданні на шкіру або в очі кислот і лугів змити їх струменем води протягом 10 хвилин, а потім нейтралізувати відповідними розчинами:при попаданні кислоти на тіло — 5% розчином питної соди.при попаданні кислоти в очі — 3% розчином питної содипри попаданні лугу в очі 2-3% розчином борної кислоти. При проливанні кислоти або лугу на стіл або підлогу, слід засипати піском, а потім нейтралізувати. ЗАБОРОНЯЄТЬСЯ виливати відпрацьовані кислоти і луги в каналізацію.
АптекаріФізіологічний розчин – штучно приготований водно-сольовий розчин (розчин кухонної солі у воді), за осмотичним тиском і сольовим складом близький до плазми крові. Його вводять хворим при значних крововтратах. Розрахувати, які маси солі і води слід взяти, щоб виготовити 100 г фізіологічного розчину, із масовою часткою 0,9 %.
Хімічна розминка- Що треба знати, щоб розрахувати масу розчину?- Які за розчинністю речовини вам відомі?- Від чого залежить розчинність речовин?- Чому вода в морях солона?- Як називають речовини, які не розчиняються у воді?- Як змінюється розчинність речовин у воді за збільшення температури?- Як змінюється розчинність речовин у воді за перемішування?- Чи впливає на розчинення подрібнення речовин? Як саме?- Що таке розчин?- Розчин — це однорідна суміш чи неоднорідна?- Чи можна вважати розчином суміш піску з водою?
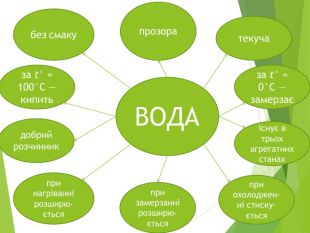
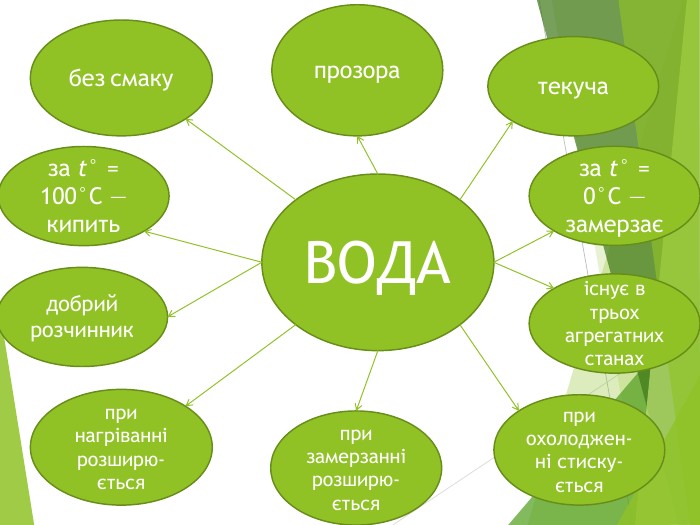
Гронування. Назвіть унікальні властивості води. Прозора. Текуча. Без смаку. Розчиняє деякі речовини. Має низьку теплопровідність. Унаслідок нагрівання розширюється. У разі охолодження стискається. Унаслідок замерзання розширюється. За t° = 0°С — замерзає За t° = 100°С — кипить. На Землі є в трьох станах.
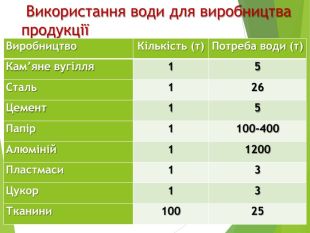
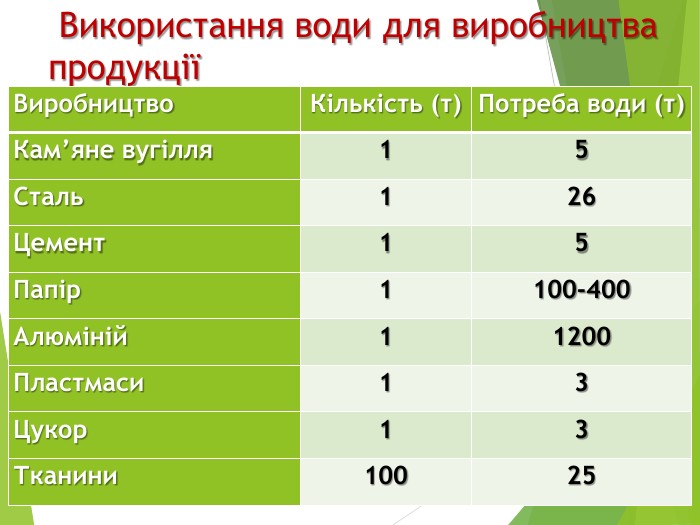
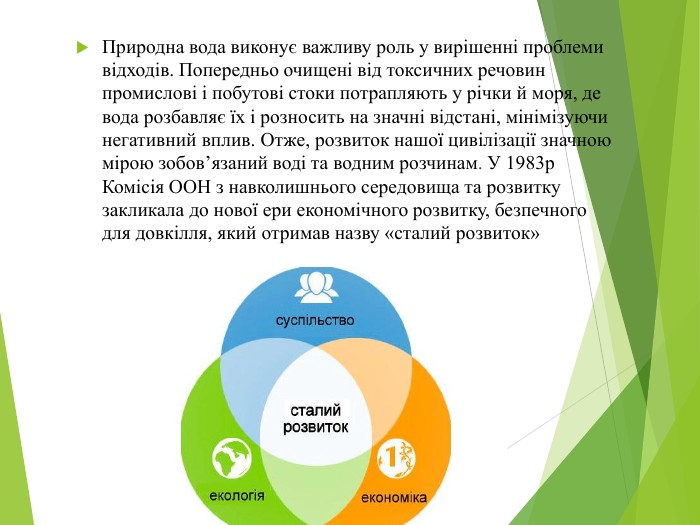
Природна вода виконує важливу роль у вирішенні проблеми відходів. Попередньо очищені від токсичних речовин промислові і побутові стоки потрапляють у річки й моря, де вода розбавляє їх і розносить на значні відстані, мінімізуючи негативний вплив. Отже, розвиток нашої цивілізації значною мірою зобов’язаний воді та водним розчинам. У 1983р Комісія ООН з навколишнього середовища та розвитку закликала до нової ери економічного розвитку, безпечного для довкілля, який отримав назву «сталий розвиток»
Домашнє завдання: опрацювати параграф 30 виконати вправи 215,216- Підготувати міні-проект: (високий рівень навчальних досягнень) «Зберігаючи воду-заощаджую родинний бюджет».- Творче завдання: підготувати презентацію на тему «Кислотні дощі»(Дотримання правила академічної доброчесності)
Джерела використаної літератури: П. П. Попель, Л,С. Крикля Хімія. Підручник для 7 кл. Київ. Видавничий центр “Академія”, 2016 Григорович О. В. Хімія.7 клас Розробки уроків Х.: Вид-во “Ранок”, 2007. Шаповалов С. А. Довідник старшокласниката абітурієнта. Х. Торсінг, 2005. Старовойтова І. Ю. Усі уроки хімії. 7 клас. Х.: Вид. група “Основа”, 2007.


про публікацію авторської розробки
Додати розробку