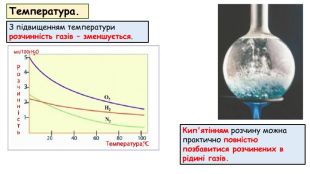
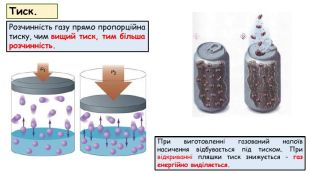
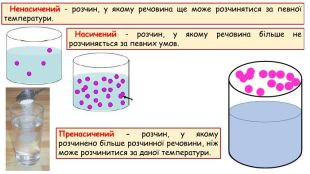
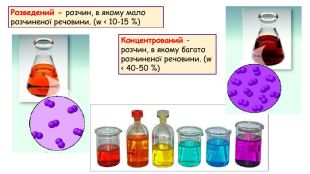
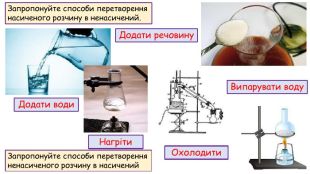
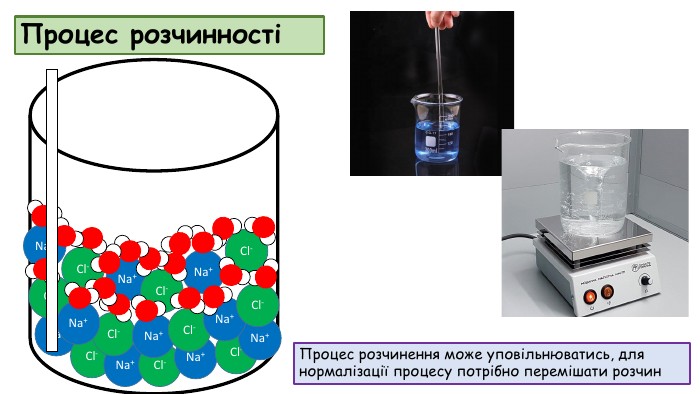
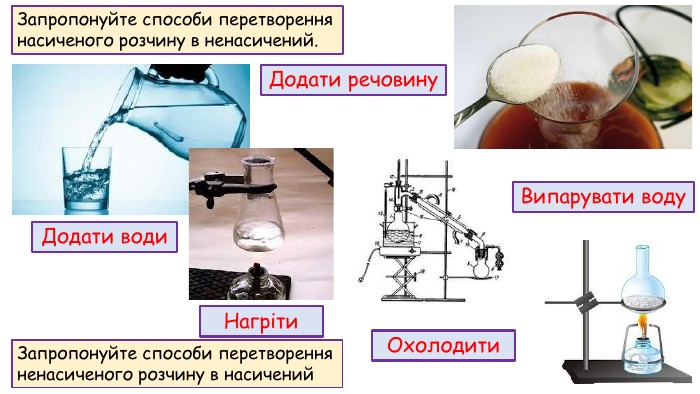
Розчинність речовин, її залежність від різних чинників. Насичені й ненасичені, концентровані й розведені розчини.




Чи існує повністю не розчинні речовини?В чому суть святої води?У IV столітті до нашої ери війська Олександра Македонського вторглися до Індії. На берегах річки Інд у військах вибухнула епідемія шлунково-кишкових захворювань, яка, як не дивно, не торкнулася жодного з военноначальников. Чому так відбулось?
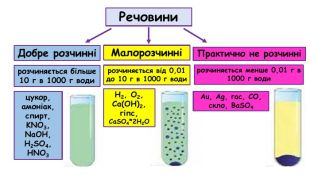
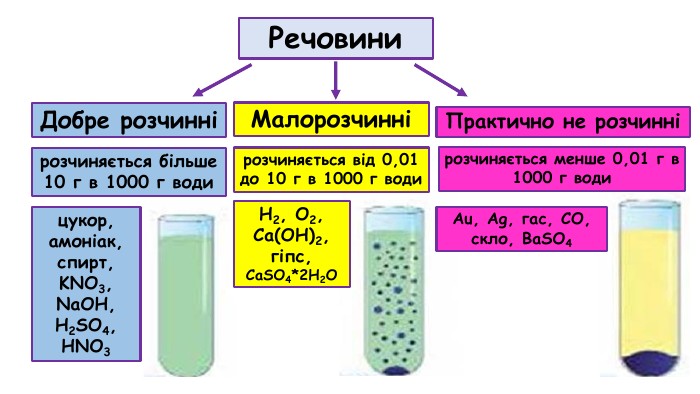
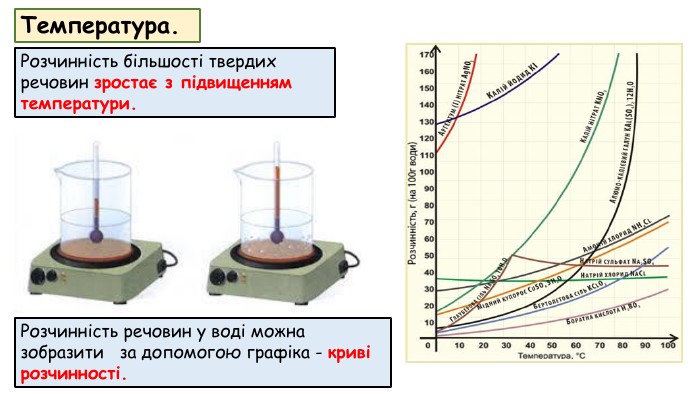
Речовини. Добре розчинніМалорозчинніПрактично не розчиннірозчиняється більше 10 г в 1000 г водицукор, амоніак, спирт, KNO3, Na. OH, H2 SO4, HNO3розчиняється від 0,01 до 10 г в 1000 г води. H2, O2, Ca(OH)2, гіпс, Ca. SO4*2 H2 Oрозчиняється менше 0,01 г в 1000 г води. Au, Ag, гас, CO, скло, Ba. SO4
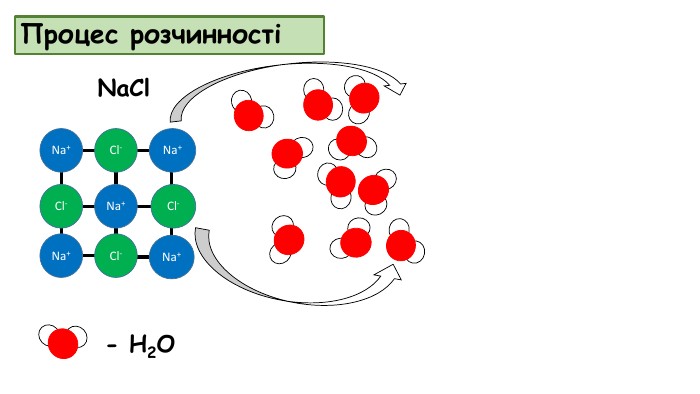
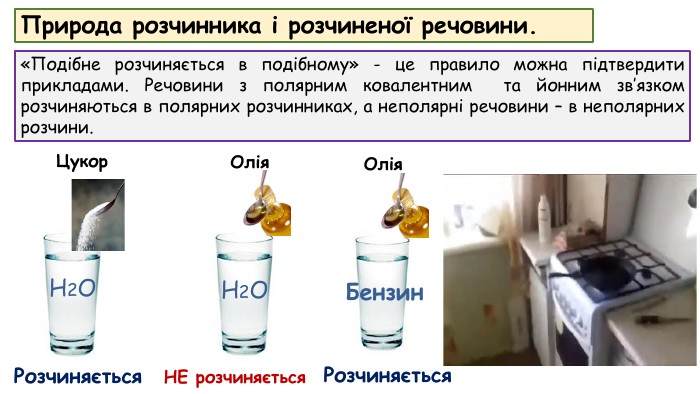
Природа розчинника і розчиненої речовини.«Подібне розчиняється в подібному» - це правило можна підтвердити прикладами. Речовини з полярним ковалентним та йонним зв’язком розчиняються в полярних розчинниках, а неполярні речовини – в неполярних розчини. Н2 ОБензин. Розчиняється. НЕ розчиняється. Цукор. Олія. Олія. Розчиняється. Н2 О


про публікацію авторської розробки
Додати розробку