Тема. Ознайомлення з Періодичною системою хімічних елементів
Урок № ____ Клас:____
Тема. Ознайомлення з Періодичною системою хімічних елементів
Мета:
Навчальна мета: ознайомити учнів із будовою періодичної системи хімічних елементів Д.І.Менделєєва ; сформувати початкові навички визначення положення хімічного елемента в періодичній системі; продовжити знайомство із символами й назвами елементів за сучасною українською номенклатурою.
Розвивальна мета: вдосконалювати вміння аналізувати, порівнювати, встановлювати причинно-наслідкові зв’язки, застосовувати теоретичні знання для прогнозування; стимулювати пізнавальну активність учнів, інтерес до предмету.
Виховна мета: виховувати свідоме ставлення до вивчення хімії, бажання здобувати нові знання.
Формувати групи компетентностей: соціально-трудову, інформаційну, загальнокультурну, уміння вчитися.
Тип уроку: формування компетентностей
Методи і методичні прийоми:
• словесний (бесіда, розповідь, робота з підручником, опорною схемою періодичною системою хімічних елементів, складання опорних конспектів);
• наочний (демонстрація періодичної системи, інтелект картки, дошки jamboard ).
Прийоми: «Асоціації», «Зоровий диктант», «Мозковий штурм», створення проблемної ситуації, «Вірю – не вірю».
Форми навчання: індивідуальна, колективна, фронтальна.
Обладнання: періодична система хімічних елементів Д. І. Менделєєва, інтелект-картка, комп’ютер, проектор, інтерактивна дошка, підручник.
Хід урок
І. Організаційний етап.
Привітання учнів, перевірка готовності до уроку.
ІІ. Актуалізація опорних знань.
Виконання завдань
Завдання 1. «Вірю, не вірю».
Із запропонованих тверджень виберіть вірні:
Хімія – це наука, яка вивчає хімічні речовини.
Прикладами однорідних сумішей є повітря, молоко, газована вода та суміш олії з водою.
До неоднорідних сумішей можна віднести кров, ґрунт, дощову воду, суміш піску з водою.
Речовина складається з молекул, молекули з атомів.
Атоми складаються з ядра та позитивно зарядженої електронної оболонки.
До складу ядра входять протони та нейтрони.
Протон має позитивний заряд.
Атом в цілому електронейтральний.
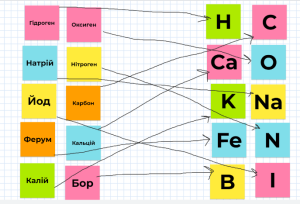
Завдання 2. «Зоровий диктант» (з використанням дошки jamboard)
На дошці записані хімічні символи та їх назви в хаотичному порядку: F, Al, B, H, O, C, Ca, N, Na, K,Fe, I, потрібно з’єднати хімічний символ з вимовою символа.
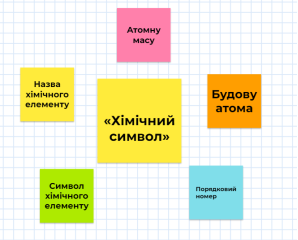
Завдання 3. Створення куща асоціації « Хімічний символ»
(з використанням дошки jamboard)
Які відомості можна знайти про хімічний елемент у періодичній системі?
• Назву;
• порядковий номер;
• атомну масу;
• будову атома.
ІІІ. Мотивація навчальної діяльності.
Створення і обговорення проблемного питання:
Чи мають адресу хімічні елементи?
Сьогодні в кінці уроку, після розглядання нової теми ми спробуємо написати листа хімічному елементу, але щоб підписати конверт нам потрібно з’ясувати ряд нових понять:
• Країна (періодична система хімічних елементів Д.І. Менделєєва)
• Область (номер періоду)
• Місто (номер групи)
• Будинок (підгрупа)
• Квартира (порядковий номер)
• Прізвище (назва хімічного елементу)
• Ім’я (символ хімічного елементу)
Мета нашого уроку: сформувати початкові навички визначення положення хімічного елемента в періодичній системі та ознайомитися із структурою Періодичної системи та принципами розташування хімічних елементів у таблиці.
Пригадайте. Що ви знаєте про будову атома? (Прийом «Мозковий штурм»)
IV. Вивчення нового матеріалу
- Періодичний закон хімічних елементів
Пояснення розповідь вчителя
Дмитро Іванович Менделєєв розташував елементи в певному порядку – збільшення відносної атомної маси. Періодична система була складена на основі періодичного закону, відкритого в 1869 році Д. І. Менделєєвим. Періодичний закон ми розглянемо трохи пізніше, а до Періодичної системи звертатимемося впродовж усього курсу вивчення хімії. На момент створення Періодична система містила лише 63 елементи — саме стільки їх було відкрито на той час. У міру відкриття нових елементів вона доповнювалася новими даними. На честь Д. І. Менделєєва хіміки називають Періодичну систему його ім’ям. Геніальність Д. І. Менделєєва полягала в тому, що він передбачив існування невідкритих на той час елементів і залишив для них вільні місця в таблиці.
Сьогодні до Періодичної системи внесено 118 елементів. Вона поповнюється щойно відкритими елементами, і поки що вчені не можуть однозначно стверджувати, скільки всього елементів може існувати.
- Структура періодичної системи хімічних елементів
Пояснення розповідь вчителя з використанням інтелект-карти «Періодична система»
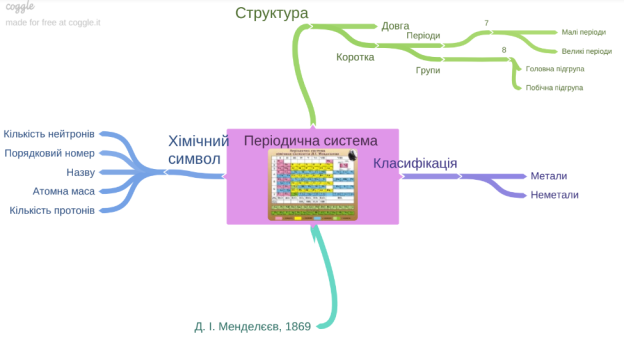
Поширено два варіанти таблиці: короткий і довгий. Розгляньмо ці варіанти. Елементи розташовуються в порядку зростання атомних мас і мають порядковий номер.
Складений ряд елементів Д. І. Менделєєв поділив на короткі ряди, що починалися характерними металами (лужні метали: Li, Na, K, Rb, Cs, Fr) і закінчувалися типовими неметалами (галогени: F, Cl, Br, I, At). Пізніше було відкрито інертні елементи (благородні гази: He, Ne, Ar, Kr, Xe, Rn), що завершують кожен ряд. Так сформувалися горизонтальні ряди — періоди.
Періоди — це горизонтальні ряди хімічних елементів. На сьогодні відомо сім періодів.
І, ІІ, ІІІ — малі періоди, що складаються з одного ряду елементів.
IV, V, VI, VII — великі періоди, що складаються з двох рядів елементів і можуть мати навіть більш ніж два ряди.
Після розташування періодів один під одним утворилося вісім груп.
Група — вертикальний стовпець елементів. У них зібрані елементи, що мають подібні хімічні властивості, хоча вони можуть відрізнятися за фізичними властивостями.
Усередині групи елементи поділяються на головну і побічну групу.
3. Значення періодичної системи
Робота з підручником
Прочитайте розділ «Значення періодичної системи» с. 62–63, дайте відповідь на запитання: Які ми можемо знайти відомості про елемент у кожній клітинці Періодичної системи?
V. Узагальнення та систематизація знань
Виконання завдань з використанням Періодичної системи.
1. Зі скількох періодів і груп складається сучасна Періодична система?
2. Як з допомогою Періодичної системи визначити заряд ядра атома? Визначте заряд ядер в атомів Оксигену, Нітрогену, Хлору та Натрію.
3. Дайте відповідь на запитання:
Назвіть елемент 5 групи головної підгрупи;
Назвіть елемент 3 групи побічної підгрупи;
Назвіть елемент 8 групи побічної підгрупи;
Назвіть елемент 2 групи головної підгрупи.
4. Назвіть період і групу, в якій знаходяться атоми:
C — II період, IV група, головна підгрупа;
Al — III період, III група, головна підгрупа;
F — II період, VII група, головна підгрупа;
Fe — IV період, VIII група, побічна підгрупа;
Cu — IV період, I група, побічна підгрупа.
VI. Підведення підсумків уроку
Сьогодні на уроці ми з вами довідалися багато нового про хімічний елемент.
Зокрема:
• Всі хімічні елементи розташовані в періодичній системі хімічних елементів, яка була створена Д.І. Менделєєвим у 1861 році.
• Періодична система складається з періодів та груп.
• Кожний хімічний елемент крім назви та символу має порядковий номер, атомну масу та певну будову.
• Порядковий номер вказує на кількість протонів та електронів атома хімічного елемента.
Висновок: періодична система хімічних елементів Д.І. Менделєєва – унікальний довідковий посібник хіміка, що містить відповіді на багато питань про будову атомів, властивості елементів та їх сполук.
Чим більше ми з вами будемо користуватися періодичною системою тим більше в цьому будемо переконуватися.
Повертаємося до проблемного питання.
Тож спробуємо написати листа хімічному елементу, але перш за все подпишем конверт. Що вказують на конверті?
• Країна (періодична система хімічних елементів Д.І.Менделєєва).
• Область (номер періоду)
• Місто (номер групи)
• Будинок (підгрупа)
• Квартира (порядковий номер)
• Прізвище (назва хімічного елементу)
• Ім’я (символ хімічного елементу)
Підбиття підсумків уроку, виставлення оцінок.
Сьогодні на уроці я дізнався нового…
Сьогодні на уроці я був здивований…
Сьогодні на уроці була відома мені інформація про …
Сьогодні на уроці мені не сподобалося …
VII. Домашнє завдання:
§ 8 опрацювати, виконати № 3 с. 64 усно, № 6 с. 64 письмово.


про публікацію авторської розробки
Додати розробку
