Тема: Повітря, його склад. Оксиген. Поширеність оксигену в природі. Кисень, склад його молекули, поширеність у природі. Фізичні властивості кисню. Озон. Урок у 7 класі
Урок хімії в 7 класі
Тема: Повітря, його склад. Оксиген. Поширеність оксигену в природі. Кисень, склад його молекули, поширеність у природі. Фізичні властивості кисню. Озон.
Мета: освітня: ознайомити учнів із повітрям, як сумішшю газів, його фізичними властивостями , з найпоширенішим на Землі хімічними елементом – оксигеном, простими речовинами: киснем – оксигеном, простими речовинами: киснем і озоном, фізичними властивостями;
розвивальна: продовжити формувати навички учнів аналізувати й робити висновки за спостереженням дослідів;
виховна: виховувати в учнів допитливість.
Тип уроку: набуття нових знань та навичок.
Обладнання: періодична система хімічних елементів Д.І. Менделєєва, таблиця складу повітря, свічка, трубка, колби.
Форми і методи роботи: метод проблемного запитування, хімічний експеримент, «мозковий штурм», робота в парах.
Хід уроку
- Організований момент.
- Актуалізація опорних знань.
Бесіда за планом:
- Які речовини називаються простими?
- На які дві групи поділяються прості речовини? (Метали й неметали).
- За якими ознаками можливо відрізнити метали від неметалів? (Блиск, ковкість, пластичність, теплопровідність, електропровідність).
Вправа: У кожного учня є грибочки з простими та складними речовинами. Потрібно на дошці розташувати в корзинки прості та складні речовини.
- Мотивація пізнавальної діяльності.
Бесіда.
Які асоціації у вас викликає слово «повітря»?:
![]()
![]()
![]()

![]()
![]()
![]()
![]()
Одним з найважливіших і найпоширеніших елементів на Землі є Оксиген. Він входить до складу простих і складних речовин. Одна із простих речовин – це О2. Сьогодні ми почнемо вивчати кисень.
- Визначення теми, мети й завдань уроку. Записуємо поняття і терміни: повітря, кисень, озон, фізичні властивості повітря.
- Вивчення нового матеріалу.
Учитель: Навколо Землі «Повітряний океан» . У цьому океану не берегів, він починається від поверхні Землі й поступово переходить у Космос. Він складається з повітря і є дуже легкий та безбарвний. Ми його не бачимо, адже він прозорий. Кожного дня ми «купаємося» в ньому. Повітря є повсюди: на вулиці, у кімнаті, у землі, у воді.
Що ж входить у склад повітря:
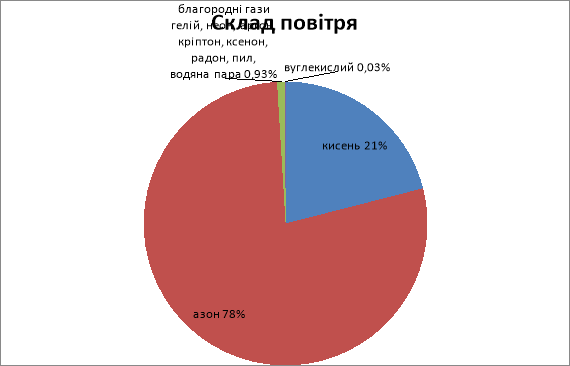
Метод: «Проблемного запитання»
- Що спільного між усіма складниками повітря? (Газоподібні речовини, невидимі, прозорі, безбарвні.)
- Які основні джерела забруднення повітря? (Виверження вулканів, пилові бурі, видобуток корисних копалин, спалювання листя, робота автотранспорту, викиди підприємств, тощо).
- Який з складників повітря найцінніший? (Так, кисень відіграє особливу роль природі.
- Як кисень утворюється у природі? (фотосинтез)
Саме тому епіграф нашого уроку:
«Кисень – ти не просто необхідний
для життя, ти і є саме життя»
Він виступає одночасно і будівельником і руйнівником, окиснюючі органічні речовини, кисень підтримує дихання а отже й життя. Енергія, що при цьому вивільняється, забезпечує життєдіяльність організмів.
Проте за участю кисню в природі відбуваються і руйнівні процеси: іржавіння металів, горіння речовин, гниття рослинних і тваринних решток.
Робота біля дошки:
- Складання характеристики оксигену;
Хімічний елемент: О
Порядковий номер: 8
Будова атома: +8
Відносна атомна маса: 16
Валентність: ІІ
Проста речовина: О2; О3
Відносна молекулярна маса: О2; О3
Сьогодні ми спробуємо визначити властивості повітря експериментальним шляхом.
- Повторення техніки безпеки.
Дослід 1: Запалюємо свічку й накриваємо її скляним ковпаком. Що спостерігаємо?
Дослід 2: В склянку з водою подути через соломинку. Що спостерігаємо?
Дослід 3: До скляної банки, заповненої водою, опускаємо догори дном колбу так, щоб в неї не заходила вода. Чому вода не заходить до колби?
Дослід 4: Нагріваємо колбу з водою, починають виходити бульбашки повітря. Чому ?
Дослід 5: На банку з гарячою водою одягаємо гумову рукавичку. Охолола вода, рукавичка здулась? Чому так відбувається?
Дослід 6: Надуємо повітряну кульку. Вона стає пружною. (Повітря пружне).
Після виконання дослідів робимо висновок властивості повітря.
Висновок: суміш газів без кольору, запаху і смаку, займає певний об’єм, погано розчинюється у воді, розширюється під час нагрівання і стискається під час охолодження, пружне.
Поширення оксигену у природі. Оксиген – найпоширеніший хімічний елемент на Землі. Масова частка його в оболонці Землі 52 % Оксиген входить до складу води, піску, глини, гірських порід і мінералів. Він є у складі всіх речовин, з яких побудовані живі організми.
|
Гідросфера |
33,1% |
|
Атмосфера |
21% |
|
Літосфера |
58% |
|
Людина |
25,7 % |
|
Вода |
88,8 % |
|
Живі організми |
50-85% |
Проста речовина кисень О2, озон О3.
Робота учнів в парах з підручником:
Фізичні властивості кисню;
Збереження кисню;
6. Узагальнення та систематизування знань.
Мозковий штурм:
- Чому повітряна куля, наповнена теплим повітрям, підіймається вгору?
- Чому звірі до зими вдягають теплі пухнасті шуби?
- Чому звірі та птахи в сильний холод ховаються в сніг?
- Чому кисень називають «життєвим» газом?
- Чому риба, викинута на берег, швидше гине, навіть якщо її весь час обливають водою?
- У воді масова частка Оксигену 89,9%. Чому юдина не дихає водою, а дихає повітрям?
7. Оцінювання учнів. Підведення підсумків.
8. Домашнє завдання.
1


про публікацію авторської розробки
Додати розробку
