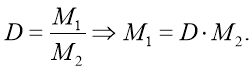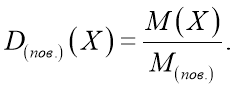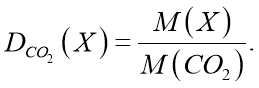Тема уроку :ВІДНОСНА ГУСТИНА ГАЗІВ. 8 клас
Тема уроку :ВІДНОСНА ГУСТИНА ГАЗІВ. 8 клас
Цілі:
- Формування ключових компетентностей:
- саморозвитку й самоосвіти — вміння розв’язувати задачі;
- інформаційної — вміння робити короткий раціональний запис, робити висновки та узагальнення.
- Формування предметних компетентностей: формувати поняття «відносна густина газів»; формувати вміння виконувати обчислення густини газів та молярну масу речовини за відносною густиною; розвивати хімічну мову; виховувати інтерес до хімії як науки.
Обладнання: роздавальний матеріал, мультимедійний проектор, комп’ютер.
Тип уроку: ВНМ (Д).
Форми роботи: розповідь, бесіда, прийом «Мікрофон».
ХІД УРОКУ
І. ОРГАНІЗАЦІЯ КЛАСУ
ІІ. ОГОЛОШЕННЯ ТЕМИ Й МЕТИ УРОКУ
ІІІ. АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ
Прийом «Мікрофон» (за основними поняттями попередніх уроків)
(Запитання проектують на екран.)
- Відносна атомна маса.
- Відносна молекулярна маса.
- Молярна маса.
- Нормальні та стандартні умови.
- Величина молярного об’єму за нормальних умов.
- Обчислення відносної молекулярної маси речовини.
- Обчислення молярної маси.
- Обчислення густини речовини.
- Обчислення густини газу кількістю речовини 1 моль.
- Обчислення кількості речовини за відомою масою.
- Обчислення маси за відомою кількістю речовини.
- Обчислення кількості речовини за відомим об’ємом газу.
- Обчислення об’єму газу за відомою кількістю речовини.
|
Речовина |
Mr (реч.) |
M (реч.), г/моль |
ν(реч.), моль |
m (реч.), г |
V (реч.), л |
ρ(реч.), г/л |
|
N2O |
|
|
2 |
|
|
|
|
N2 |
|
|
2 |
|
|
|
|
С2Н2 |
|
|
2 |
|
|
|
IV. МОТИВАЦІЯ НАВЧАЛЬНОЇ ДІЯЛЬНОСТІ. БЕСІДА ЗА ПИТАННЯМИ
З таблиці видно, що газоподібні речовини за однакових умов та однакової кількості речовини мають однаковий об’єм, але різні масу та густину.
На сьогоднішньому уроці ми порівняємо густини різних газів.
V. ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
(Необхідні схеми проектують на екран.)
1. 1 моль будь-якого газу займає однаковий об’єм, але має різну масу. Маса 1 моль одного газу більша за масу 1 моль іншого газу в стільки разів, у скільки більша молярна маса одного газу за інший.
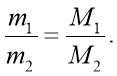
Таке відношення називають відносною густиною газів і позначають D.
2. Наведемо приклади виразів для обчислення відносних густин різних газів.
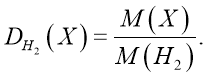
![]()
Приклад розв’язування задач
Обчислити відносну густину вуглекислого газу за воднем.
Аналіз задачі: Що відомо? Що знайти? Як це зробити?
|
Дано: CO2 |
Розв’язання 1. Які молярні маси водню та вуглекислого газу? M (H2) = 2 г/моль. M (CO2) = 44 г/моль. |
|
DH2 (CO2) = ? |
2. Яка відносна густина вуглекислого газу за воднем?
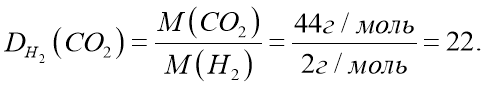
Відповідь: DH2 (CO2) = 22.
VІ. ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
Розв’язування задач
Учням пропонують роздавальний матеріал із переліком задач. Одну задачу учень розв’язує біля дошки.
1. Обчислити відносну густину хлору за воднем, повітрям, чадним газом.
2. Обчислити відносну густину газу за повітрям, якщо його відносна густина за воднем дорівнює 30.
VІІ. ПІДБИТТЯ ПІДСУМКІВ УРОКУ
VІІІ. ДОМАШНЄ ЗАВДАННЯ


про публікацію авторської розробки
Додати розробку