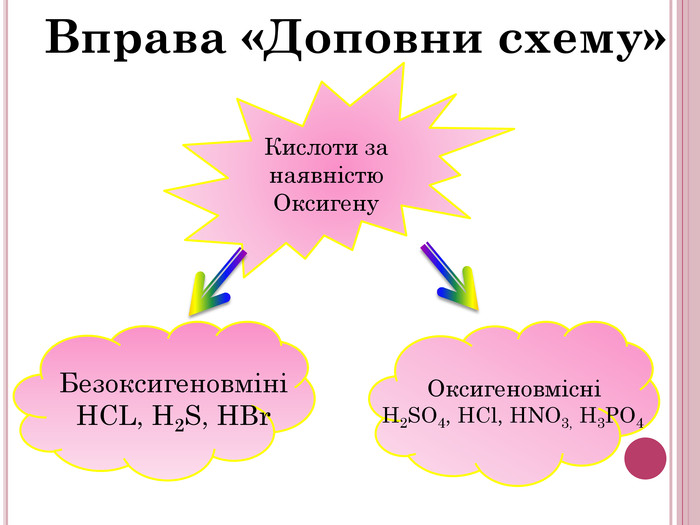
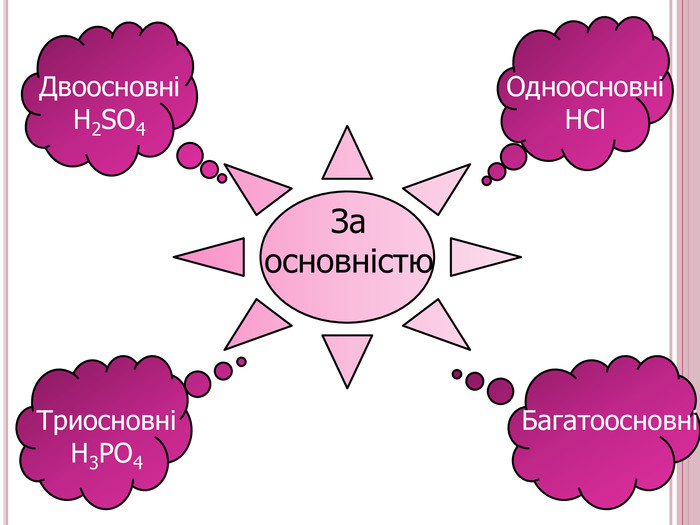
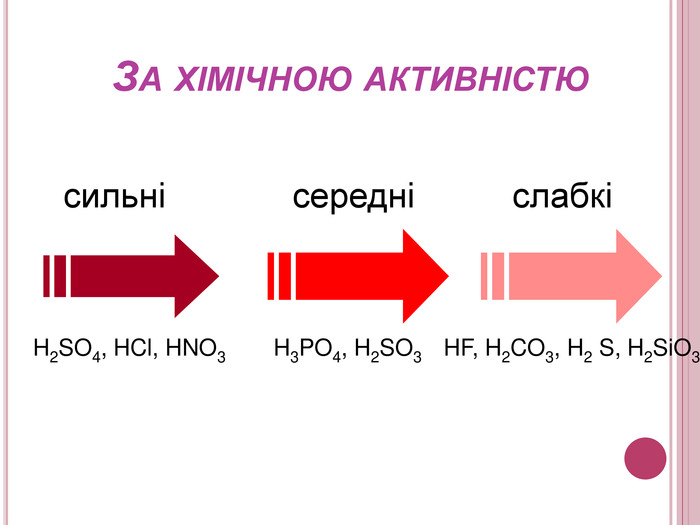
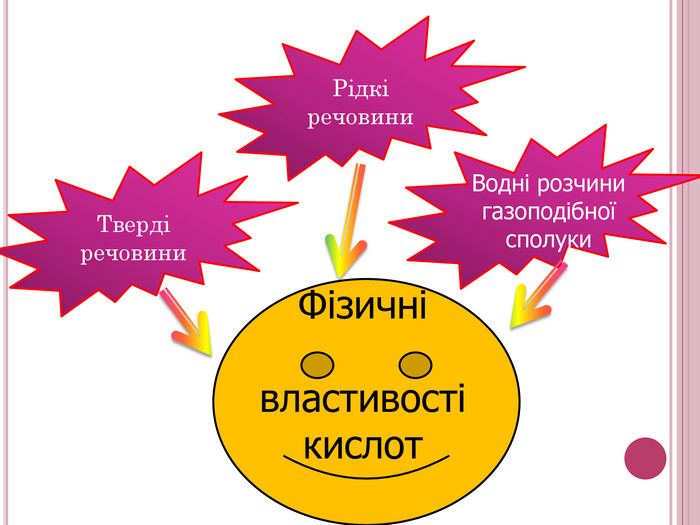
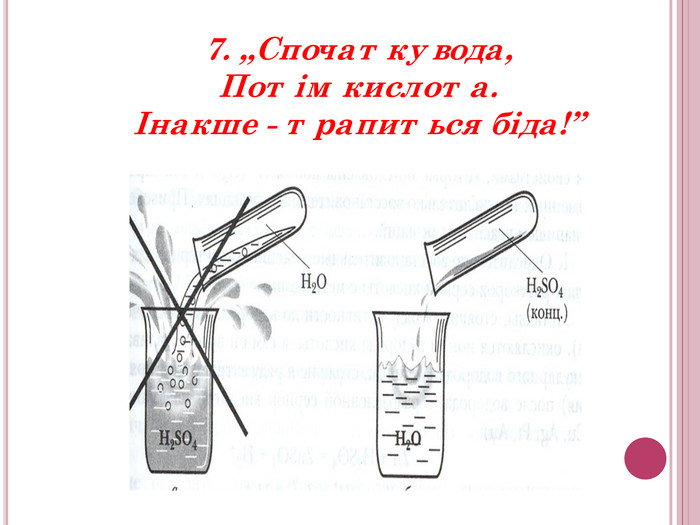
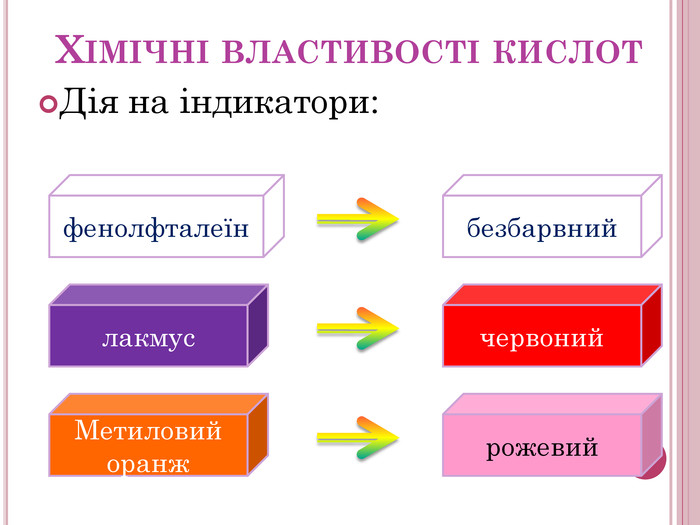
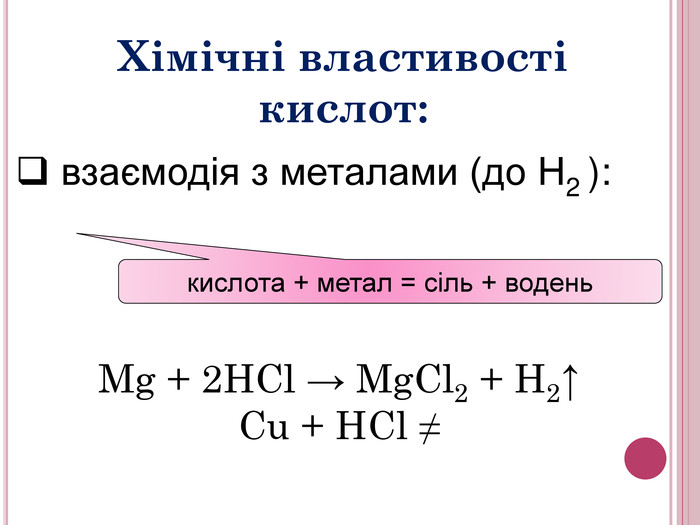
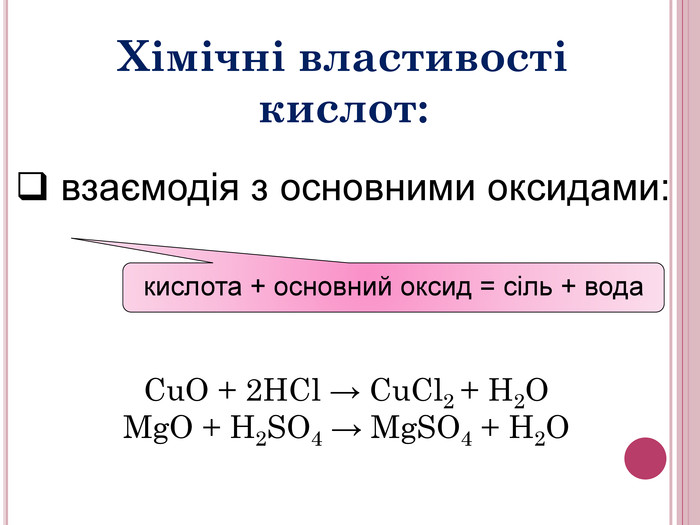
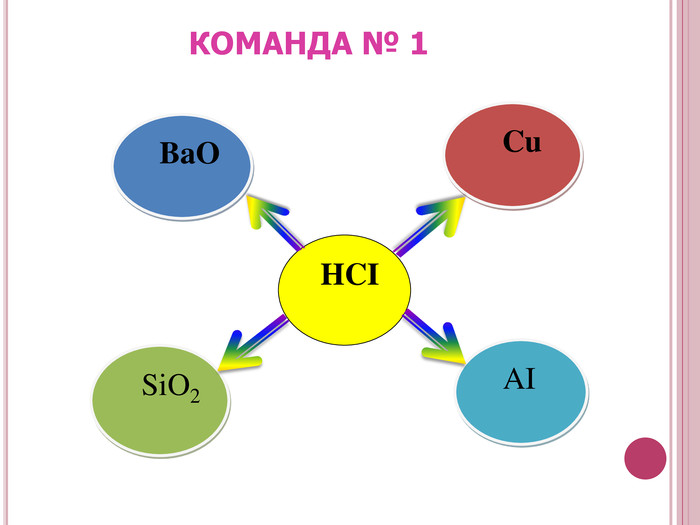
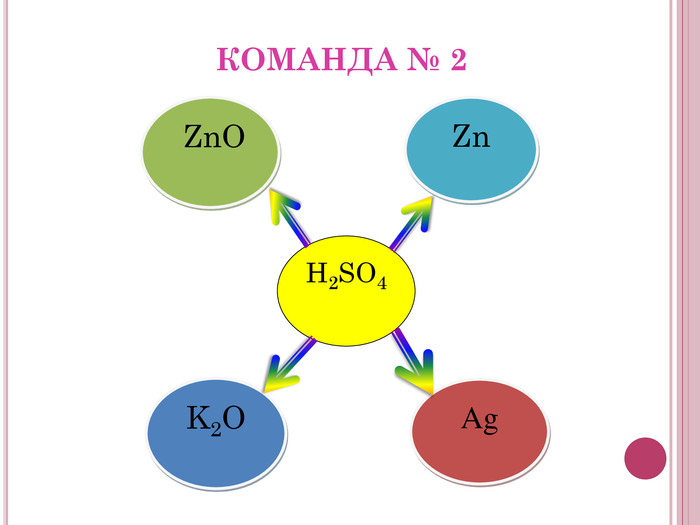
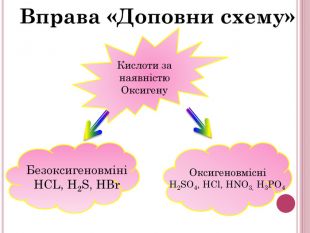
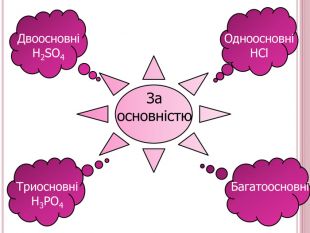
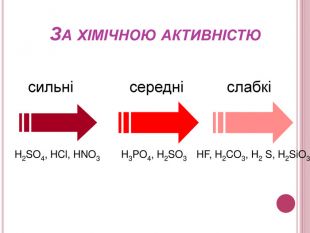
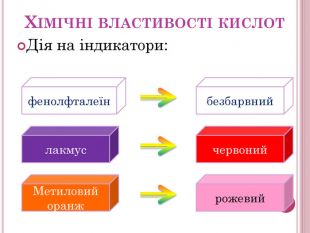
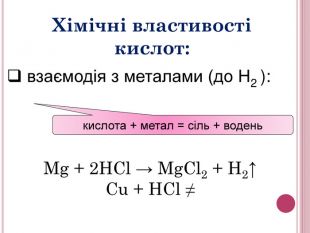
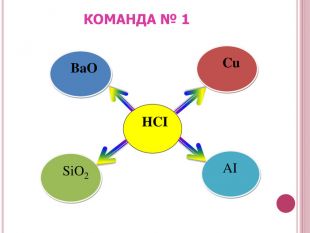
Урок-презентація. Хімічні властивості кислот: дія на індикатори, взаємодія з металами, основними оксидами. Ряд активності металів. Реакції заміщення й обміну.
Про матеріал
Розробка відкритого уроку з хімії для 8 класу на тему"Хімічні властивості кислот: дія на індикатори, взаємодія з металами, основними оксидами. Ряд активності металів. Реакції заміщення й обміну".
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку