Урок «Радіоактивність. Основний закон радіоактивного розпаду»
Урок
Тема уроку: «Радіоактивність. Основний закон радіоактивного розпаду»
Мета уроку: ознайомити учнів з поняттям радіоактивність; розглянути основний закон радіоактивного розпаду;
Хід уроку.
І. Організаційний момент. Оголошення теми та мети уроку.
ІІ. Перевірка домашнього завдання.
ІІІ. Актуалізація опорних знань.
Переглянути презентацію «Радіоактивність» за посиланням https://1drv.ms/p/s!Ak4lTFJFXw91gRT6dPWJvPKaqmgd
ІV. Вивчення нового матеріалу.
- Радіоактивність – це здатність ядер деяких хімічних елементів (материнське ядро) довільно перетворюватися на ядра інших елементів (дочірнє ядро) із випромінюванням мікрочастинок. ПриПри цьому деякі ядра випускають тільки α -частинки, інші — β -частинки, треті — і α -, і β -частинки.
- Причини радіоактивного розпаду
Було встановлено, що під час радіоактивного випромінювання реалізується мрія алхіміків: випромінювання супроводжується перетворенням одних хімічних елементів на інші.
Намагаючись пояснити явища, що спостерігаються, Е. Резерфорд і його співробітник Ф.Содді висунули гіпотезу, відповідно до якої причиною радіоактивного випромінювання є мимовільний розпад атомів.
З гіпотези Резерфорда й Содді випливало, що кожен атом радіоактивної речовини — це «сховище» енергії. Під час розпаду атома частина енергії зі «сховища» несеться α- і β-частками і γ-променями, а енергія, що залишилася, зберігається в новому атомі, що утворився в результаті розпаду. Стало очевидним, що енергія, що вивільнюється під час радіоактивного розпаду, міститься не просто в атомах, а в атомних ядрах.
- Період напіврозпаду
Резерфорд, досліджуючи перетворення радіоактивних речовин, установив дослідним шляхом, що їхня активність зменшується з часом. Так, активність радону зменшується вдвічі вже за 1 хв.
Для кожної радіоактивної речовини існує визначений інтервал часу, протягом якого активність зменшується вдвічі.
Період напіврозпаду Т — це час, протягом якого розпадається половина наявного числа радіоактивних атомів.
Наприклад, для ядра![]() період напіврозпаду складає близько 1600 років. Отже, якщо взяти 1 г радію, то через 1600 років його буде 0,5 г, а через 3200 років — 0,25 г. Таким чином, вихідна кількість радію повинна перетворитися на нуль через нескінченний проміжок часу.
період напіврозпаду складає близько 1600 років. Отже, якщо взяти 1 г радію, то через 1600 років його буде 0,5 г, а через 3200 років — 0,25 г. Таким чином, вихідна кількість радію повинна перетворитися на нуль через нескінченний проміжок часу.
У різних речовин період напіврозпаду дуже різний: від мільйонних часток секунди до мільярдів років. Чим менше період напіврозпаду, тим активніше протікає розпад.
|
Радіоактивна речовина |
Період напіврозпаду |
Радіоактивна речовина |
Період напіврозпаду |
|
Полоній |
3 · 10-7 с |
Стронцій |
27 років |
|
Радон |
52 с |
Радій |
1622 роки |
|
Каліфорній |
55 діб |
Уран |
4,5 · 109 років |
|
Кобальт |
5,26 року |
Торій |
1,4 · 1010 років |
З таблиці видно, що активність полонію зменшується вдвічі майже миттєво, стронцію — за 27 років, а активність радію, урану і торію не змінюється протягом людського життя.
3. Закон радіоактивного розпаду
Нехай число радіоактивних атомів у початковий момент часу (t =0) дорівнює N0. Через час t1 = Т число ядер, що не розпалися, дорівнює![]() , через t2 = 2Т залишиться
, через t2 = 2Т залишиться![]() , через t3 = 3Т таких ядер виявиться
, через t3 = 3Т таких ядер виявиться![]() і т. ін. Отже, наприкінці проміжку часу t = nT ядер, що не розпалися, залишиться
і т. ін. Отже, наприкінці проміжку часу t = nT ядер, що не розпалися, залишиться![]() . Оскільки
. Оскільки ![]() , то закон радіоактивного розпаду набуває вигляду:
, то закон радіоактивного розпаду набуває вигляду:
![]()
За цією формулою знаходять число атомів, що не розпалися, у будь-який момент часу. Період напіврозпаду — стала величина, що не може бути змінена такими доступними впливами, як охолодження, нагрівання, тиск тощо.
Закон розпаду атомів не є законом, що керує розпадом одного атома, тому що не можна вгадати, коли відбудеться цей розпад.
Розпад атома не залежить від його віку, тобто атоми «не старіють».
Розпад будь-якого атомного ядра — це, так би мовити, не «смерть від старості», а «нещасливий випадок» у його житті. Для радіоактивних атомів не існує поняття віку. Можна визначити лише середню тривалість життя τ.
![]()
Середня тривалість життя — це просто середнє арифметичне тривалості життя досить великої кількості атомів даного виду. Передбачити, коли відбудеться розпад даного атома, неможливо. Закон радіоактивного розпаду визначає середнє число атомів, що розпадаються за певний інтервал часу. Закон радіоактивного розпаду є статистичним законом.
Питання до учнів у ході викладу нового матеріалу
1.Чим відрізняються радіоактивні атоми від нерадіоактивних?
2. Яка причина радіоактивного розпаду?
3. Що розуміють під періодом напіврозпаду?
4. Чи існує вік у радіоактивних атомів?
V. Закріплення вивченого матеріалу
1. Якісні питання
- Чому не визначають час повного розпаду всіх ядер?
- Чи правильним є твердження, що чим довше існує атом, тим більше ймовірність його розпаду?
- Лічильник реєструє β-частки радіоактивного препарату. Чи спрацьовує лічильник через однакові інтервали часу?
2. Навчаємося розв'язувати задачі
- Дві різні речовини містять однакове число N радіоактивних атомів. Період напіврозпаду першої з них 1 рік, другої — 4 роки. Яка з речовин більш активна?
- Існує певна кількість радіоактивного ізотопу срібла. Маса радіоактивного срібла зменшилася у 8 разів за 810 діб. Визначте період напіврозпаду радіоактивного срібла.
Розв'язання:![]() , звідки
, звідки![]() або
або![]() .
.
Тоді![]() , звідки=
, звідки=![]() 270 (діб).
270 (діб).
- Скільки за масою радіоактивної речовини залишиться через три доби, якщо спочатку її було 100 г? Період напіврозпаду речовини дорівнює дві доби. (Відповідь: 35,4 г.)
VI. Висновки урока.
Період напіврозпаду Т — це час, протягом якого розпадається половина наявного числа радіоактивних атомів.
Закон радіоактивного розпаду:
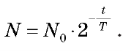
Розпад атома не залежить від його віку, тобто атоми «не старіють».
Домашнє завдання
Опрацювати конспект уроку; виконати домашнє завдання з презентації.


про публікацію авторської розробки
Додати розробку
