Урок "Солі. Кислі солі" 11 клас
Про матеріал
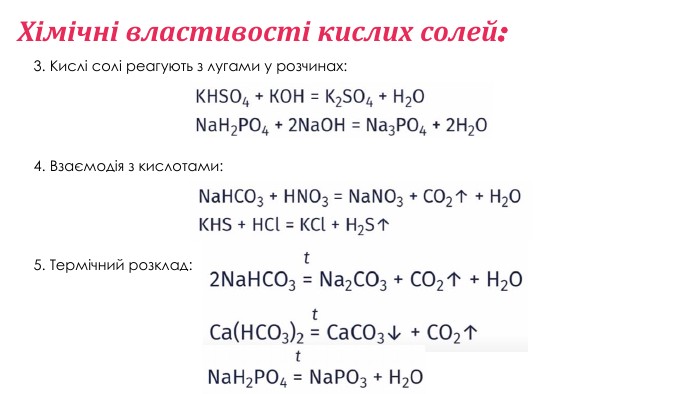
Солі. Кислі солі. Назви кислих солей. Хімічні властивості кислих солей. Застосування кислих солей. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
ДЯКУЮ! Успіхів Вам!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку