Урок з хімії для 11 класу на тему: "Кислоти. Кислотні дощі"
Дата_______ Урок № ____ (Хімія, 11 клас)
Кислоти. Кислотні дощі.
Особливості взаємодії металів з нітратною кислотою
і концентрованою сульфатною кислотою.
Цілі уроку:
актуалізувати знання і вміння в області вивчення природного довкілля; поглибити знання про кислоти, кислотні оксиди; сформувати знання про кислотні дощі;
розвивати вміння складати рівняння реакцій, складати схеми електронного балансу;
виховувати екологічну компетенцію, бережливе ставлення до навколишнього середовища; формувати самоосвітню компетенцію.
Тип уроку: поглиблення й засвоєння знань, умінь, навичок.
Хід уроку
І. Організація класу
ІІ. Мотивація
На дошці записаний епіграф «Земля не належить нам. Це ми належимо землі» (мудрість індіанців Сіу)
За їх допомогою одержують багато необхідних людині речовин: добрива, без яких не можуть розвиватися рослини, вибухові речовини, ліки, барвники, пластмаси, волокна та ін.
Проте ці речовини можуть нести й величезну загрозу людству та всьому живому на Землі…
Як ви думаєте, яким речовинам ми присвятимо наш урок?
(діти висувають свої припущення)
ІІІ. Повідомлення теми і мети уроку
ІV. Актуалізація опорних знань
Робота учнів біля дошки
Вправа 1. «Логічні квадрати»
(знайдіть у логічних квадратах місце для Натрію і Нітрогену)
|
K |
Ca |
|
|
Ag |
|
C |
Cl |
|
P |
|
Вправа 2. «Дзеркало» (з’єднайте стрілками формулу речовини та її назву)
Ag2O силіцій (IV) оксид
ZnO алюміній оксид
P2O5 хлор (VІІ) оксид
Cl2O7 цинк оксид
SiO2 фосфор (V) оксид
Al2O3 аргентум (І) оксид
Вправа 3. «Біла ворона» (знайти зайвий оксид у кожному рядку)
А) CaO, BaO, CO2, MgO
Б) Fe2O3, Cr2O3, SO3, Al2O3
В) Na2O, H2O, K2O, N2O5
Доки 3 учні працюють біля дошки, інші учні працюють з картками.
Вправа «Естафета незакінчених речень» (робота з картками)
1. Формула сульфатної кислоти...
2. Сульфатна кислота... сполука.
3. За звичайних умов чиста сульфатна кислота ...
4. Розчинення кислоти у воді супроводжується ... .
5. Кислоту ... , а не навпаки.
6. Сульфатна кислота реагуючи з металом буде ... .
7. Якщо з металом взаємодіє розбавлена сульфатна кислота, то ... .
8. Якщо реагентом є концентрована сульфатна кислота, то ... .
9. Чиста сульфатна кислота, а також її концентрований розчин ... .
10.Вона добре поглинає ...
11.Сульфатна кислота утворює солі ... .
12.Якісною реакцією на йони SO42- є утворення ...
V. Вивчення нового матеріалу
Пояснення вчителя та записи в робочий зошит
(з використанням презентації та відео-сюжетів)
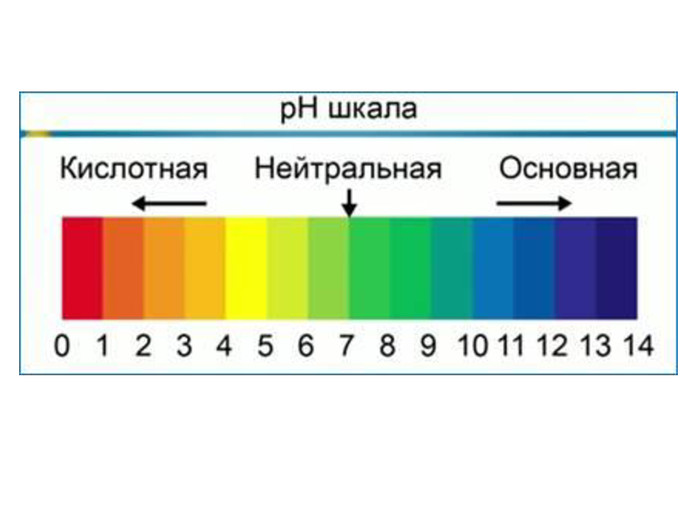
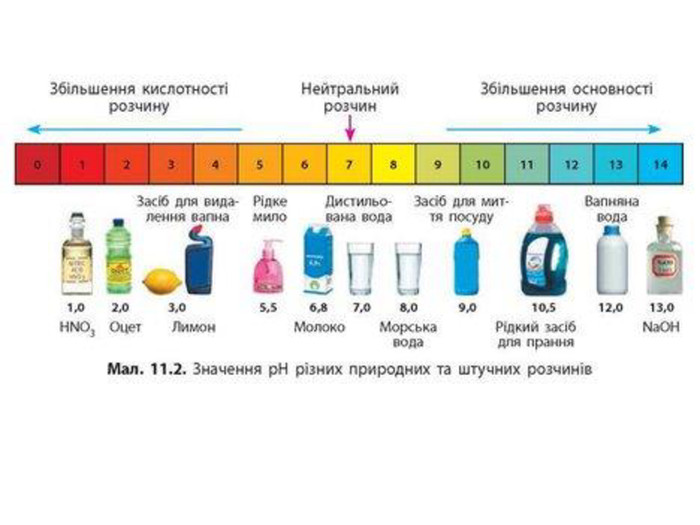
1. Пригадуємо та конспектуємо в зошити визначення поняття кислоти, загальну формулу речовин цього класу, класифікацію кислот.
2. Фізичні властивості нітратної кислоти HNO3
Безбарвна рідина, жовтіє при зберіганні, має різкий запах; вибухонебезпечна, «димить».
= 1,5 г/см3, tкип. = 86 ⁰С, tзамерз. = – 41 ⁰С.
Нітратна кислота токсична!
У разі потрапляння на шкіру викликає опіки у вигляді жовтих плям.
3. Хімічні властивості HNO3
Розведена нітратна кислота має всі типові властивості кислот.
З металами поводиться по різному в залежності від активності металу та міцності кислоти.
Водень під час взаємодії з металами концентрованої нітратної кислоти ніколи не виділяється.
Концентрована нітратна кислота не реагує із залізом, хромом, алюмінієм (пасивний стан). Отже, її можна зберігати в залізній або алюмінієвій тарі.
Але варто лише додати туди води, як починається реакція й не залишається ні кислоти, ані металевої оболонки, в якій вона містилася.
(Перегляд відео «Окислювальні властивості нітратної кислоти» https://www.youtube.com/watch?v=JOX6Z9nWDog)
Суміш одного об’єму HNO3 та трьох об’ємів НСl називається «царською горілкою».
У такий спосіб можна розчинити золото і платину.
Записуємо рівняння реакції:
Au + HNO3 + 3HCl = AuCl3 + NO + 2H2O
3Pt + 4HNO3 + 12HCl = 3PtCl4 + 4NO + 8H2O
Хімічний калейдоскоп
Датський учений Нільс Бор у 1943 році під час окупації території Данії німецькими фашистами вимушений був залишити батьківщину і, щоб врятувати Нобелівську медаль, розчинив її у царській горілці, а після повернення за допомогою метода електролізу виділив золото та замовив собі нову медаль.


3.1. Взаємодія концентрованої HNO3 з міддю
Cu + 4HNO3 → Cu(NO3)2 + 2NO2↑+ H2O
«лисячий хвіст» (газ бурого кольору)
(Перегляд відео «Взаємодія концентрованої нітратної кислоти з міддю» https://www.youtube.com/watch?v=-sK32VMsR8E)
3.2. Властивості нітратної кислоти, спільні з іншими кислотами:
(складіть рівняння реакцій)
HNO3 + Mg(OH)2 =
HNO3 + Al2O3 =
HNO3 + (NH4)2CO3 =
Перевіряємо рівняння.
Рубрика «Потрібно знати»
- Миття й очищення овочів знижує вміст нітратів приблизно на 10 %.
- Під час відварювання овочів у відвар переходить до 50 % нітратів.
- Під час консервування та квашення до 30% нітратів переходить у розчин
Запобіжні засоби, до яких потрібно вдаватися, аби уникнути отруєння нітратами:
- дотримання правил агротехніки вирощування сільськогосподарських культур;
- обмежене споживання овочевих культур, що виросли у теплицях;
- дотримання рекомендацій щодо зменшення вмісту нітратів у процесі приготування овочевих страв.
4. Сульфатна кислота H2SO4
Це важка оліїста рідина, безбарвна, без запаху.
Ця дуже гігроскопічна речовина роз'їдає папір і тканини, спричинює опіки шкіри. Під час розчинення сульфатної кислоти у воді, розчин нагрівається настільки, що може закипіти!
Це дуже небезпечно!
(Перегляд відео із записами рівнянь хімічних реакцій
«Хімічні властивості сульфатної кислоти» https://www.youtube.com/watch?v=Td6itaNfJrU)
4.1. Взаємодія цукру з концентрованою сульфатною кислотою

(Перегляд відео «Утворення вугільної піни»
https://www.youtube.com/watch?v=De5B-LyYCVI)
5. Кислотні дощі
Доповіді та презентації учнів.
VІ. Систематизація й узагальнення нових знань
Розв’язання екологічних задач (за варіантами)
1. Протягом однієї години ТЕС спалює близько 1т вугілля, масова частка Сульфуру в якому становить 3%. Яка маса SO2 потрапить в атмосферу протягом доби?
2. Деякі країни забезпечують свої потреби в сульфатній кислоті за рахунок сульфур (IV) оксиду, що вловлюють з вихідних газів під час роботи ТЕС. Обчисліть,яку масу сульфатної кислоти можна одержати в результаті спалювання 100т вугілля,що містить 2% Сульфуру,а практичний вихід кислоти становить 93%.
VІІ. Рефлексія.
Вправа «Сенкан».
(іменник) - Сульфатна кислота
(2 прикметника) - безбарвна, оліїста
(3 дієслова) - димить, взаємодіє, обвуглює
(ключова фраза, 4 слова) - широко використовується на практиці
(синонім) - «хліб» хімічної промисловості.
На уроці я:
- дізнався…
- зрозумів…
- навчився…
- найбільший мій успіх – це…
- найбільші труднощі я відчув…
- я не вмів, а тепер умію…
- я змінив своє ставлення до…
- на наступному уроці я хочу…
VІІІ. Підбиття підсумків уроку.
Музика моря і дощу, гімн лісів, шелест хлібів – це нам подарувала природа. У цій красі вінцем її творіння стала людина – мудра, сильна, чуйна. А отже,від кожного з нас залежить чи буде існувати ця краса в майбутньому, чи буде існувати ця планета і люди на ній.
Домашнє завдання.
Опрацювати § 20, 21.
- Гр. А – переписати всі рівняння реакцій на ст. 105, 107;
виконати “Сторінку природодослідника” (ст. 107)
- Гр. Б – ст. 111 № 2
Завдання на розвиток логічного мислення:
- Розшифруйте один із записів алхімічного тракту: «Якщо Марс у своєму блискучому обладунку впаде в обійми Венери, яка розтанула від пекучих сліз, він обов’язково почервоніє…».
Підказка:
Під Марсом і Венерою алхіміки розуміли залізо і мідь, а пекучі сльози — концентровані кислоти (у тому числі сульфатна та нітратна).
-
Дякую!!!
-


про публікацію авторської розробки
Додати розробку