Виховний захід «Хімічні перегони»
Сценарій виховного заходу
на тему:
«Хімічні перегони»
Мета виховного заходу: формувати пізнавальний інтерес, поглибити і виявити знання учнів 9 класу з курсу "Неорганічна хімія"
Форма проведення: інтелектуальна гра.
Методи проведення: бліц-турнір, вікторини, хімічний експеримент, творчі завдання.
Засоби проведення: наочні ( картки-завдання ), хімічне обладнання та реактиви ( сухе пальне, сірники, дощечка, амоній дихромат (NH4)2Cr2O7 , етиловий спирт C2H5OH, глюконат кальцію C12H22CaO14, розчин крохмалю (С6Н10О5)n, кристалики йоду I2 )
Використані джерела:
- Науменко С. «Найрозумніший» / С. Науменко// Журнал «Хімія». – Шкільний світ, 2008. – №33 – 15-23 с.
- Джапарова З. Неметали. Інтелектуальні ігри. / З. Джапарова //Журнал «Хімія. Біологія» . – Шкільний світ, 2005. – №57 – 19-24 с.
Вступне слово вчителя.
Доброго дня, дорогі учні та гості! Ми раді вітати всіх у цьому залі, де відбудеться інтелектуальна гра, яка в черговий раз доведе, що хімія – це дуже цікава наука. Сьогодні ми весело та з користю проведемо час. На учнів 9 класу чекає інтелектуальна битва. Участь у цій грі допоможе вам перевірити та вдосконалити свої знання і вміння.
Перед тим, як почати гру, я хочу представити членів журі, які будуть допомагати мені підраховувати бали та об’єктивно вас оцінювати. Журі врахує командні й особисті досягнення кожного учня.
(Учитель представляє членів журі)
Ведучий 1. Сьогодні у двобої зійдуться команди, які будуть мати нагоду показати свої знання, кмітливість, винахідливість, начитаність та пізнати щось нове. Ми з нетерпінням хочемо познайомитися з командами і їхніми учасниками. Тож вітаємо команди. (Ведучий представляє команди).
Ведучий 2. А тепер ми можемо розпочинати нашу інтелектуальну гру. І першим конкурсом у нас буде розминка. «Розімніть» свої знання. Зараз кожній команді по черзі учитель поставить 15 запитань. Відповідати потрібно коротко. Кожна правильна відповідь принесе команді 1 бал.
1 конкурс «Розминка»
Запитання для першої команди.
- Наука про речовини і їхнє перетворення. (Хімія)
- Реакція, під час якої з однієї складної речовини утворюється кілька простих речовин. (Реакції розкладу)
- Речовини, утворені атомами одного елемента. (Прості)
- Дрібні хімічно неподільні частинки. (Атоми)
- Одиниця виміру кількості речовини. (Моль)
- Ступінь окиснення Гідрогену. (+1)
- Формула кухонної солі. (NaCl)
- Число Авогадро. (6,02*1023структурних одиниць / моль)
- Число атомів у молекулі позначають за допомогою… (індексу)
- Реакції, які одночасно відбуваються у двох протилежних напрямках. (Оборотні)
- Назвіть речовину, формула якої Na3PO4. (Натрій ортофосфат)
- Реакція, що відбуваються з виділенням тепла. (Екзотермічна)
- Складні речовини, до складу яких входять два елементи, один із яких Оксиген. (Оксиди)
- Речовина, що пришвидшує швидкість хімічної реакції. (Каталізатор)
- Рівняння, в якому зазначений тепловий ефект хімічної реакції. (Термохімічне)
Запитання для другої команди.
- Умовний запис складу речовини за допомогою хімічних символів та індексів. (Хімічна формула)
- Реакція між простою і складною речовиною, в яких атоми простої речовини заміщують атоми в складній. (Реакція заміщення)
- Речовини, утворені атомами різних елементів. (Складні)
- Дрібна частинка речовини, що зберігає її властивості. (Молекула)
- Одиниця виміру молярного об’єму. ( л/моль)
- Ступінь окиснення Оксигену. (-2)
- Формула гашеного вапна. (Са(ОН)2)
- Молярний об’єм. (22,4 л/моль)
- Число, яке записують перед формулою або хімічним символом і позначає кількість формульних одиниць. (Коефіцієнт)
- Реакції, які відбуваються в одному напрямку і завершуються повним перетворенням реагентів на продукти реакції. (Необоротні)
- Назвіть речовину, формула якої K2SO4. (Калій сульфат)
- Реакція, що відбувається поглинанням тепла. (Ендотермічна)
- Складні речовини, до складу яких входять атоми Гідрогену і кислотні залишки. (Кислоти)
- Речовини, що сповільнюють швидкість хімічної реакції. (Інгібітори)
- Реакції, під час яких відбувається зміна ступеня окиснення елементів. (Окисно-відновні)
Ведучий 1. Журі підраховує бали, а ми рухаємось далі. Наступний конкурс – «Детективи»
Ведучий 2. Як Шерлок Холмс з його дедуктивним методом, так і ви, як справжні детективи, маєте тільки по опису визначити, про яку речовину йдеться. Командам будуть прочитані деякі визначення, що стосуються загаданої речовини. Якщо є відповідь після першого визначення, то команді присуджуються 5 балів, якщо після другого – 4 бали, після третього – 3 бали тощо.
2 конкурс «Детективи»
Завдання для першої команди.
- - Його називають безжиттєвим газом. (5 балів)
- Це досить інертний газ. (4 бали)
- Він легший за повітря. (3 бали)
- Він входить до складу повітря. (2 бали)
- Його хімічна формула N2. (1 бал)
( Азот )
- - Дуже поширений неметалічний елемент. (5 балів)
- Цей елемент входить до складу білків. (4бали)
- Незамінний елемент у виробництві гуми. (3 бали)
- Використовується в сільському господарстві для боротьбизі шкідниками виноградної лози. (2 бали)
- Жовта речовина, що не змочується. (1 бал)
( Сірка )
- - За поширеність в земній корі посідає друге місце після Оксигену. (5 балів)
- Головний елемент у царстві мінералів та гірських порід . (4 бали)
- Входить до складу кремнезему. (3 бали)
- Приємноспекотноголітнього дня полежатибіля моря на йогооксиді. (2 бали)
- Добуваютьсиліконові каучуки. (1 бал)
( Силіцій )
Завдання для другої команди.
- - Хімічно активний газ. (5 балів)
- Це алотропна модифікація типового неметалу. (4 бали)
- Газ із приємним свіжим запахом. (3 бали)
- Утворюється під час грози. (2 бали)
- Утворює озоновий шар. (1 бал)
( Озон.)
- - 1771 року Карл Шеєле розробив спосіб добування цієї речовини з кісток, що застосовували аж до ХІХ століття. (5 балів)
- Потрібенрослинам для якнайшвидшогодозріванняплодів. (4 бали)
- Входить до складу білків. (3 бали)
- 1669 року ГенінгБранддобувбілуречовину. (2 бали)
- У перекладі з грецькоїмовиназваозначає«світлоносний». (1 бал)
( Фосфор )
- - Елементутворюєнайтвердішуречовину. (5 балів)
- З ньоговиготовляютьдрукарськуфарбу. (4 бали)
- З цьогонеметалувиготовляютьприкраси. (3 бали)
- Його оксид бере участь у процесі фотосинтезу. (2 бали)
- З ньоговиготовляютьграфітовістрижні для олівців. (1 бал)
( Вуглець )
Ведучий 1. Ну що, замучилися детективи? Пропоную трішки розвантажитись, адже на черзі «Розвантажувальний» конкурс.
Ведучий 2. За відведений час ви повинні написати якомога більше слів на букву С, які мають стосунок до хімії. Це може бути хімічний посуд, назви елементів, терміни, речовини і т.д. За кожне слово – 1 бал. Час пішов.
3 конкурс «Розвантажуючий»
(Спиртівка, сірники, сіль, сода, суміш, сплав, Сульфур, Силіцій, Скандій, Селен, Стронцій, Станум, Сіборгій, Самарій, спирт, сполучення, сполука і т.д.)
Учитель. Журі підбиває підсумки трьох конкурсів, а у нас – експериментальна пауза. Зараз ви будете мати змогу спостерігати справжній вулкан. Сумніваєтесь? Тоді дивіться.
Опис досліду: на залізну пластинку насипаємо невелику купку амоній дихромату, зробивши заглиблення, у яке наливаємо кілька крапель етанолу. Спирт підпалюємо. Відбувається бурхливий процес розкладання амоній дихромату, що нагадує виверження вулкана, з кратера якого вилітає вогонь. Під час розкладання амоній дихромату утворюються сіро-зелений хром(ІІІ) оксид, азот і водяна пара, які спучують суміш.
(NH4)2Cr2O7 = N2 + 4H2O + Cr2O3
Ведучий 2. А зараз надаємо слово журі для оголошення результатів попередніх конкурсів. (Журі оголошує результати)
Ведучий 2. Дякуємо. А ми продовжуємо нашу гру. «Знайди мене» – так називається наш 4 конкурс.
Ведучий 1. Кожна команда отримає листок із завданням. У першій колонці у вас наведені формули речовин. Ваше завдання – визначити, до якого класу речовин відноситься дана сполука і обвести букву у відповідній клітинці. З літер, що відповідають правильним відповідям, складіть слово. За правильне виконання даного завдання команда отримає 10 балів, проте команда, яка виявиться спритнішою, зможе додати до свого рахунку ще 5 бонусних балів.
4 конкурс «Знайди мене»
Завдання для першої команди.
|
Формула |
Оксид |
Кислота |
Основа |
Сіль |
|
HCl |
І |
Д |
В |
И |
|
CaO |
И |
Б |
А |
П |
|
Cu(OH)2 |
Х |
К |
С |
Л |
|
H3PO4 |
У |
О |
Л |
М |
|
Na2SiO3 |
Р |
С |
І |
Ц |
|
Al(OH)3 |
К |
Т |
І |
О |
|
CO2 |
А |
П |
Р |
Г |
|
HNO3 |
О |
Ц |
К |
М |
|
Li2SO3 |
В |
Я |
У |
I |
|
NaOH |
К |
О |
Я |
Ж |
Завдання для другої команди.
|
Формула |
Оксид |
Кислота |
Основа |
Сіль |
|
Fe2O3 |
Е |
Д |
В |
И |
|
Ca(OH)2 |
И |
Б |
Л |
П |
|
HBr |
Х |
Е |
С |
Л |
|
BaO |
К |
О |
Л |
М |
|
Na2SiO3 |
Р |
С |
І |
Т |
|
Zn(OH)2 |
К |
Т |
Р |
О |
|
SO2 |
О |
П |
Р |
Г |
|
HNO3 |
Н |
Л |
К |
М |
|
K2SO4 |
В |
Я |
У |
I |
|
LiOH |
К |
О |
Т |
Ж |
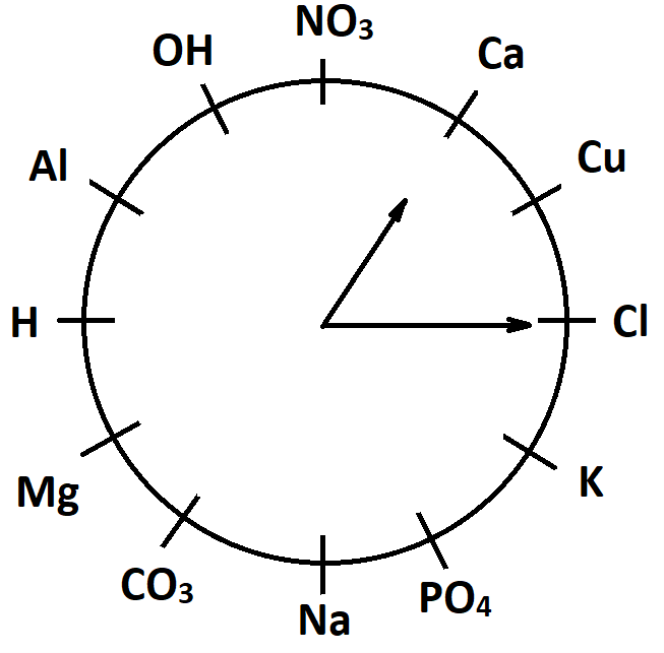
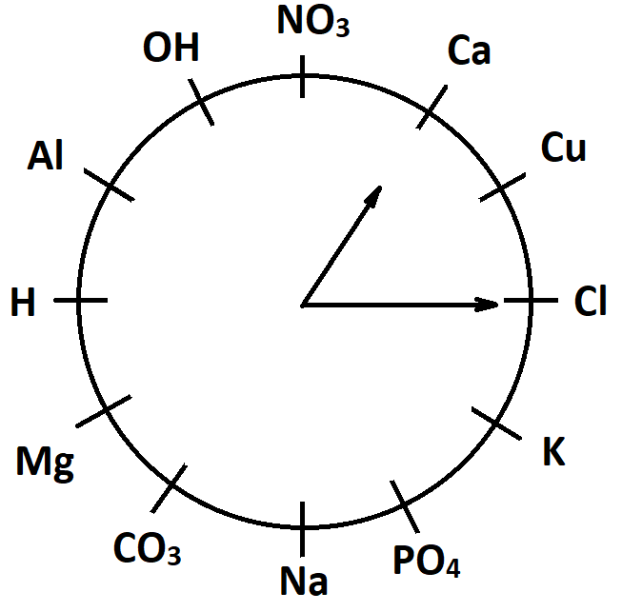
Ведучий 1. Рухаємось далі. Чи знаєте ви, що існують годинники, за якими можна визначити не лише час? Зараз ви будете мати можливість у цьому переконатись, адже наступний наш конкурс має назву «Хімічний годинник».
Ведучий 2. На столах у вас «хімічні годинники». Придивіться уважніше. Замість цифр у вас метали , кислотні залишки, гідроксильна група та Гідроген. У завданні кожної команди буде зазначений час, під яким зашифрована певна речовина, формулу якої ви повинні скласти та дати їй назву. Для виконання завдання вам буде відведено 3 хвилини. За цей час ви повинні скласти якомога більше формул речовин. Кожна правильна відповідь буде оцінена в 2 бали: один бал за правильно складену формулу, другий бал – за правильну назву речовини.
5 конкурс «Хімічний годинник»

Приклад: 13:15 – CaCl2 – кальцій хлорид
13:25 – ( Ca3(PO4)2 – кальцій ортофосфат)
10:15 – ( AlCl3 – алюміній хлорид )
20:55 – ( Mg(OH)2 – магній гідроксид )
16:00 – ( KNO3 – калій нітрат )
18:35 – ( Na2CO3 – натрій карбонат )
04:15 – ( KCl – калій хлорид )
09:25– ( H3PO4 – ортофосфатна кислота )
21:00 – ( HNO3 – нітратна кислота )
18:55 – ( NaOH – натрій гідроксид )
02:00 –(Cu(NO3)2 – купрум нітрат )
09:15 – ( HCl – хлоридна кислота )
04:25 – ( K3PO4 – калій ортофосфат)
16:35 – ( K2CO3 – калій карбонат )
10:00 – ( Al(NO3)3 – алюміній нітрат )
13:55 – ( Ca(OH)2 – кальцій гідроксид )
02:15 – ( CuCl2 – купрум хлорид )
21:35 – ( H2CO3 карбонатна кислота )
18:15 – ( NaCl – натрій хлорид )
20:00 – ( Mg(NO3)2 – магній нітрат )
06:25 – ( Na3PO4 – натрій ортофосфат)
Ведучий 2. Час, відведений для цього конкурсу, вийшов. Просимо капітанів команд представити результати вашої роботи нашим суддям.
Ведучий 1. А ми тим часом дійшли до 6 конкурсу, який має назву «Гонка за лідером». Участь у цьому конкурсі беруть лише капітани команд. Вони будуть мати можливість особисто вплинути на результат команди. Вам по черзі будуть задані запитання. Кожна правильна відповідь капітана принесе команді 1 бал.
6 конкурс «Гонка за лідером»
- Кислота, нерозчинна у воді. (Силікатна)
- Кількість валентних електронів у атомі Нітрогену. (5)
- Солі нітратної кислоти. (Нітрати)
- Оксид P2O5 відповідає кислоті… (H3PO4)
- Які властивості виявляє сульфур(VI) оксид? (Кислотні)
- Котрий з елементів має більш виражені неметалічні властивості: Оксиген чи Нітроген? (Оксиген)
- Назва VII групи хімічних елементів періодичної системи. (Галогени)
- Назва І групи хімічних елементів періодичної системи. (Лужні метали)
- Газ, якого в повітрі найбільше. (Азот)
- Найлегша речовина. (Водень)
- Буква, що позначає відносну густину одного газу за іншим. (D)
- Молярна маса кисню. (32 г/моль)
- Розчинні у воді гідроксиди металічних елементів. (Луги)
- Кількістю атомів якого елемента визначається валентність кислотного залишку? (Гідрогену)
- Тип хімічних реакцій, які відбуваються за наявністю каталізатора. (Каталітичні)
- Позначення теплового ефекту хімічної реакції. (∆Н)
- Речовина, що утворюється при взаємодії водню та кисню. (Вода)
- Газ, яким наповнюють подушки для дихання хворих. (Кисень)
- Яка кислота міститься в складі шлункового соку? (Хлоридна)
- Речовини, які змінюють своє забарвлення під дією кислот чи лугів. (Індикатори)
Ведучий 1. Капітани зробили все, щоб вивести свою команду у лідери. Їхні старання оцінять журі.
Ведучий 2. А ми продовжуємо нашу інтелектуальну гру. Наступне завдання, яке чекає на наших учасників, – це «Хімічний кросворд». У розпорядженні команд буде однакове завдання та 5-7 хв на те, щоб відгадати у кросворді якомога більше слів. За кожне правильно написане слово – 1 бал.
7 конкурс «Хімічний кросворд»
|
1е |
н |
д |
о |
т |
е |
2р |
м |
і |
ч |
н |
і |
|
|
13т |
|
|
|
19к |
|
к |
|
|
|
|
|
о |
|
|
|
|
|
|
|
е |
|
|
|
а |
|
3з |
а |
п |
а |
х |
|
з |
|
|
9з |
|
|
|
|
м |
|
|
|
т |
|
о |
|
|
|
|
|
к |
|
10г |
а |
з |
|
|
|
п |
|
|
|
а |
|
4т |
и |
с |
к |
|
|
л |
|
|
м |
|
|
|
|
е |
|
|
|
л |
|
е |
|
|
|
|
|
а |
|
|
і |
|
12о |
б |
о |
р |
о |
т |
н |
і |
|
р |
|
|
6о |
с |
а |
д |
|
|
щ |
|
б |
|
|
а |
|
|
|
з |
|
м |
|
|
|
|
|
у |
|
11ф |
е |
р |
м |
е |
н |
т |
и |
|
18к |
|
|
і |
|
7н |
|
|
|
|
|
|
н |
|
і |
|
|
у |
|
|
о |
|
|
ч |
|
е |
|
|
|
8к |
|
|
н |
|
н |
|
|
р |
|
|
н |
|
|
5н |
а |
г |
р |
і |
в |
а |
н |
н |
я |
|
у |
|
|
а |
|
|
ц |
|
|
і |
|
а |
|
|
|
т |
|
|
|
|
|
|
|
|
16п |
|
е |
|
|
|
|
т |
|
14р |
е |
а |
г |
е |
н |
т |
и |
|
|
|
о |
|
н |
|
|
|
|
и |
|
у |
|
л |
|
|
|
|
|
|
|
|
з |
|
т |
|
|
|
|
в |
|
х |
|
15і |
н |
г |
і |
б |
і |
т |
о |
р |
и |
|
р |
|
|
|
|
н |
|
о |
|
з |
|
|
|
|
|
|
|
|
т |
|
а |
|
|
|
|
и |
|
м |
|
а |
|
|
|
|
|
|
|
|
и |
|
ц |
|
|
|
|
й |
|
а |
|
т |
|
|
|
|
|
|
|
|
в |
|
і |
|
|
|
|
|
|
|
|
о |
|
17с |
п |
о |
л |
у |
ч |
е |
н |
н |
я |
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
|
и |
|
|
|
|
|
|
|
20а |
к |
т |
и |
в |
н |
і |
|
|
|
|
|
й |
|
|
|
Запитання до кросворду
По горизонталі.
1.Хімічні реакції, які відбуваються з поглинанням теплоти.
3.Зовнішній ефект, який супроводжує хімічну реакцію.
4.Чинник, який впливає на хімічну рівновагу.
5.Що сприяє збільшенню числа активних молекул і зростанню швидкості більшості хімічних реакцій?
6.Одна з характерних ознак хімічних реакцій.
10. Зовнішній ефект, який супроводжує хімічну реакцію.
11.Особливі біологічні каталізатори.
12. Хімічні реакції, які відбуваються одночасно у двох протилежних напрямках.
14.Назва речовин, які вступають в хімічну реакцію.
15. Речовини, які сповільнюють хімічні реакції.
17. Реакції, в результаті яких із двох або кількох речовин утворюється одна нова речовина.
20.Назва найбільш реакційноздатних молекул.
По вертикалі
1.Хімічні реакції, які відбуваються з виділенням теплоти.
2.Реакції, в результаті яких з однієї речовини утворюється дві або більше нових речовин.
7.Каталіз, який зменшує швидкість реакції.
8.Речовини, які пришвидшують швидкість хімічної реакції, але не входять до складу їх продуктів.
9.Реакції між простою і складною речовинами, у процесі яких атоми простої речовини заміщують атоми одного з елементів складної речовини, утворюючи нову просту й нову складну речовини.
12.Реакції, у процесі яких дві речовини обмінюються своїми складовими частинами, утворюючи дві нові речовини.
13.Чинник, який впливає на швидкість перебігу реакцій.
14.Рівновага, коли оборотні реакції не доходять до кінця, а пряма та зворотна реакції продовжують відбуватися з однаковою швидкістю.
16. Каталіз, який прискорює реакції.
18.Чинник, який впливає на швидкість перебігу реакції.
19.Процес зміни швидкості реакції під впливом каталізатора.
Ведучий 2. Ми наближаємось до завершення нашої інтелектуальної гри. Останній конкурс – «Зіпсований телефон». Всі ви опинялися в ситуації, коли під час розмови по телефону якість зв’язку погіршувалася, або ж узагалі переривалась. Неприємна ситуація? Звісно ж. Інколи доводилось просто здогадуватись, про що саме йшлося.
Ведучий 1. Давайте перевіримо який зв’язок сьогодні у нашому класі. Вам буде запропоноване певне визначення, яке ви будете передавати один одному по уявному телефону. Останній учасник «розмови» озвучить те визначення, яке до нього дійшло. Після цього перший учасник має сказати, про що саме йшлося. Тоді учитель вголос зачитає початковий варіант. Судді оцінять повноту і правильність переданої інформації. Максимальний бал за конкурс – 3 бали.
8 конкурс «Зіпсований телефон»
Завдання для першої команди.
Горизонтальні рядки хімічних елементів, розміщених у порядку зростання їх атомних мас, що починаються лужним металічним елементом і закінчуються інертним. (Період)
Завдання для другої команди.
Взаємодія атомів або інших частинок у речовині, яка зумовлює їхнє сполучення в молекули або кристали. (Хімічний зв’язок)
Учитель. А поки судді перевірятимуть ваші роботи і підбивають підсумки гри, ми подивимось два цікавих досліди. Перший дослід має назву «Фараонові змії».
Опис досліду:на дощечку кладемо шматочок сухого пального. На нього зверху викладаємо кілька таблеток кальцій глюконатуC12H22CaO14. Сірником запалюємо сухе пальне і таблетки. Кальцій глюконат починає плавитися і при нагрівання розкладається. Спостерігаємо як «виповзають» так звані змії.
Учитель. Наступний дослід нам доведе, що все таємне стає явним.
Опис досліду:готуємо розчин крохмального клейстеру. За допомогою пензлика на аркуші папері пишемо таємне слово. Написане можні проявити, помістивши папір у сухий стакан з кількома кристаликами простої речовини йоду. При цьому на папері з’являються сині знаки.
Учитель. Ну що, діти? Вам сподобалась гра? Сподіваюся ви поглибили свої знання та взяли для себе щось нове та цікаве. Час оголосити результати змагання. Тож передаю слово журі.
(Журі підводять підсумок гри, оголошують результати та нагороджують команди грамотами )
Учитель. Дякую командам за старання та участь у грі, суддям – за об’єктивність оцінювання і всім присутнім – за гарний настрій та приємно проведений час.
До нових зустрічей!
Завдання для першої команди.
|
Формула |
Оксид |
Кислота |
Основа |
Сіль |
|
HCl |
І |
Д |
В |
И |
|
CaO |
И |
Б |
А |
П |
|
Cu(OH)2 |
Х |
К |
С |
Л |
|
H3PO4 |
У |
О |
Л |
М |
|
Na2SiO3 |
Р |
С |
І |
Ц |
|
Al(OH)3 |
К |
Т |
І |
О |
|
CO2 |
А |
П |
Р |
Г |
|
HNO3 |
О |
Ц |
К |
М |
|
Li2SO3 |
В |
Я |
У |
I |
|
NaOH |
К |
О |
Я |
Ж |
Зашифроване слово – __________________________
Завдання для другої команди.
|
Формула |
Оксид |
Кислота |
Основа |
Сіль |
|
Fe2O3 |
Е |
Д |
В |
И |
|
Ca(OH)2 |
И |
Б |
Л |
П |
|
HBr |
Х |
Е |
С |
Л |
|
BaO |
К |
О |
Л |
М |
|
Na2SiO3 |
Р |
С |
І |
Т |
|
Zn(OH)2 |
К |
Т |
Р |
О |
|
SO2 |
О |
П |
Р |
Г |
|
HNO3 |
Н |
Л |
К |
М |
|
K2SO4 |
В |
Я |
У |
I |
|
LiOH |
К |
О |
Т |
Ж |
Зашифроване слово – ___________________________
Завдання для першої команди.
13:15 – CaCl2 – кальцій хлорид
13:25 –
10:15 –
20:55 –
16:00 –
18:35 –
04:15 –
09:25–
21:00 –
18:55 –
02:00 –
09:15 –
04:25 –
16:35 –
10:00 –
13:55 –
02:15 –
21:35 –
18:15 –
20:00 –
06:25 –
Завдання для другої команди.
13:15 – CaCl2 – кальцій хлорид
13:25 –
10:15 –
20:55 –
16:00 –
18:35 –
04:15 –
09:25–
21:00 –
18:55 –
02:00 –
09:15 –
04:25 –
16:35 –
10:00 –
13:55 –
02:15 –
21:35 –
18:15 –
20:00 –
06:25 –
Завдання для першої команди.
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
13 |
|
|
|
19 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
12 |
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
11 |
|
|
|
|
|
|
|
|
18 |
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
16 |
|
|
|
|
|
|
|
|
14 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
17 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Завдання для другої команди.
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
13 |
|
|
|
19 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
12 |
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
11 |
|
|
|
|
|
|
|
|
18 |
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
16 |
|
|
|
|
|
|
|
|
14 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
15 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
17 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 конкурс «Знайди мене»
Завдання для першої команди.
|
Формула |
Оксид |
Кислота |
Основа |
Сіль |
|
HCl |
І |
Д |
В |
И |
|
CaO |
И |
Б |
А |
П |
|
Cu(OH)2 |
Х |
К |
С |
Л |
|
H3PO4 |
У |
О |
Л |
М |
|
Na2SiO3 |
Р |
С |
І |
Ц |
|
Al(OH)3 |
К |
Т |
І |
О |
|
CO2 |
А |
П |
Р |
Г |
|
HNO3 |
О |
Ц |
К |
М |
|
Li2SO3 |
В |
Я |
У |
I |
|
NaOH |
К |
О |
Я |
Ж |
4 конкурс «Знайди мене»
Завдання для другої команди.
|
Формула |
Оксид |
Кислота |
Основа |
Сіль |
|
Fe2O3 |
Е |
Д |
В |
И |
|
Ca(OH)2 |
И |
Б |
Л |
П |
|
HBr |
Х |
Е |
С |
Л |
|
BaO |
К |
О |
Л |
М |
|
Na2SiO3 |
Р |
С |
І |
Т |
|
Zn(OH)2 |
К |
Т |
Р |
О |
|
SO2 |
О |
П |
Р |
Г |
|
HNO3 |
Н |
Л |
К |
М |
|
K2SO4 |
В |
Я |
У |
I |
|
LiOH |
К |
О |
Т |
Ж |
5 конкурс «Хімічний годинник»
( Завдення для обох команд однакове )
Приклад: 13:15 – CaCl2 – кальцій хлорид
13:25 – ( Ca3(PO4)2 – кальцій ортофосфат )
10:15 – ( AlCl3 – алюміній хлорид )
20:55 – ( Mg(OH)2 – магній гідроксид )
16:00 – ( KNO3 – калій нітрат )
18:35 – ( Na2CO3 – натрій карбонат )
04:15 – ( KCl – калій хлорид )
09:25– ( H3PO4 – ортофосфатна кислота )
21:00 – ( HNO3 – нітратна кислота )
18:55 – ( NaOH – натрій гідроксид )
02:00 –( Cu(NO3)2 – купрум нітрат )
09:15 – ( HCl – хлоридна кислота )
04:25 – ( K3PO4 – калій ортофосфат )
16:35 – ( K2CO3 – калій карбонат )
10:00 – ( Al(NO3)3 – алюміній нітрат )
13:55 – ( Ca(OH)2 – кальцій гідроксид )
02:15 – ( CuCl2 – купрум хлорид )
21:35 – ( H2CO3 карбонатна кислота )
18:15 – ( NaCl – натрій хлорид )
20:00 – ( Mg(NO3)2 – магній нітрат )
06:25 – ( Na3PO4 – натрій ортофосфат )
5 конкурс «Хімічний годинник»
( Завдення для обох команд однакове )
Приклад: 13:15 – CaCl2 – кальцій хлорид
13:25 – ( Ca3(PO4)2 – кальцій ортофосфат )
10:15 – ( AlCl3 – алюміній хлорид )
20:55 – ( Mg(OH)2 – магній гідроксид )
16:00 – ( KNO3 – калій нітрат )
18:35 – ( Na2CO3 – натрій карбонат )
04:15 – ( KCl – калій хлорид )
09:25– ( H3PO4 – ортофосфатна кислота )
21:00 – ( HNO3 – нітратна кислота )
18:55 – ( NaOH – натрій гідроксид )
02:00 –( Cu(NO3)2 – купрум нітрат )
09:15 – ( HCl – хлоридна кислота )
04:25 – ( K3PO4 – калій ортофосфат )
16:35 – ( K2CO3 – калій карбонат )
10:00 – ( Al(NO3)3 – алюміній нітрат )
13:55 – ( Ca(OH)2 – кальцій гідроксид )
02:15 – ( CuCl2 – купрум хлорид )
21:35 – ( H2CO3 карбонатна кислота )
18:15 – ( NaCl – натрій хлорид )
20:00 – ( Mg(NO3)2 – магній нітрат )
06:25 – ( Na3PO4 – натрій ортофосфат )
7 конкурс «Хімічний кросворд»
|
1е |
н |
д |
о |
т |
е |
2р |
м |
і |
ч |
н |
і |
|
|
13т |
|
|
|
19к |
|
к |
|
|
|
|
|
о |
|
|
|
|
|
|
|
е |
|
|
|
а |
|
3з |
а |
п |
а |
х |
|
з |
|
|
9з |
|
|
|
|
м |
|
|
|
т |
|
о |
|
|
|
|
|
к |
|
10г |
а |
з |
|
|
|
п |
|
|
|
а |
|
4т |
и |
с |
к |
|
|
л |
|
|
м |
|
|
|
|
е |
|
|
|
л |
|
е |
|
|
|
|
|
а |
|
|
і |
|
12о |
б |
о |
р |
о |
т |
н |
і |
|
р |
|
|
6о |
с |
а |
д |
|
|
щ |
|
б |
|
|
а |
|
|
|
з |
|
м |
|
|
|
|
|
у |
|
11ф |
е |
р |
м |
е |
н |
т |
и |
|
18к |
|
|
і |
|
7н |
|
|
|
|
|
|
н |
|
і |
|
|
у |
|
|
о |
|
|
ч |
|
е |
|
|
|
8к |
|
|
н |
|
н |
|
|
р |
|
|
н |
|
|
5н |
а |
г |
р |
і |
в |
а |
н |
н |
я |
|
у |
|
|
а |
|
|
ц |
|
|
і |
|
а |
|
|
|
т |
|
|
|
|
|
|
|
|
16п |
|
е |
|
|
|
|
т |
|
14р |
е |
а |
г |
е |
н |
т |
и |
|
|
|
о |
|
н |
|
|
|
|
и |
|
у |
|
л |
|
|
|
|
|
|
|
|
з |
|
т |
|
|
|
|
в |
|
х |
|
15і |
н |
г |
і |
б |
і |
т |
о |
р |
и |
|
р |
|
|
|
|
н |
|
о |
|
з |
|
|
|
|
|
|
|
|
т |
|
а |
|
|
|
|
и |
|
м |
|
а |
|
|
|
|
|
|
|
|
и |
|
ц |
|
|
|
|
й |
|
а |
|
т |
|
|
|
|
|
|
|
|
в |
|
і |
|
|
|
|
|
|
|
|
о |
|
17с |
п |
о |
л |
у |
ч |
е |
н |
н |
я |
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
|
и |
|
|
|
|
|
|
|
20а |
к |
т |
и |
в |
н |
і |
|
|
|
|
|
й |
|
|
|
7 конкурс «Хімічний кросворд»
|
1е |
н |
д |
о |
т |
е |
2р |
м |
і |
ч |
н |
і |
|
|
13т |
|
|
|
19к |
|
к |
|
|
|
|
|
о |
|
|
|
|
|
|
|
е |
|
|
|
а |
|
3з |
а |
п |
а |
х |
|
з |
|
|
9з |
|
|
|
|
м |
|
|
|
т |
|
о |
|
|
|
|
|
к |
|
10г |
а |
з |
|
|
|
п |
|
|
|
а |
|
4т |
и |
с |
к |
|
|
л |
|
|
м |
|
|
|
|
е |
|
|
|
л |
|
е |
|
|
|
|
|
а |
|
|
і |
|
12о |
б |
о |
р |
о |
т |
н |
і |
|
р |
|
|
6о |
с |
а |
д |
|
|
щ |
|
б |
|
|
а |
|
|
|
з |
|
м |
|
|
|
|
|
у |
|
11ф |
е |
р |
м |
е |
н |
т |
и |
|
18к |
|
|
і |
|
7н |
|
|
|
|
|
|
н |
|
і |
|
|
у |
|
|
о |
|
|
ч |
|
е |
|
|
|
8к |
|
|
н |
|
н |
|
|
р |
|
|
н |
|
|
5н |
а |
г |
р |
і |
в |
а |
н |
н |
я |
|
у |
|
|
а |
|
|
ц |
|
|
і |
|
а |
|
|
|
т |
|
|
|
|
|
|
|
|
16п |
|
е |
|
|
|
|
т |
|
14р |
е |
а |
г |
е |
н |
т |
и |
|
|
|
о |
|
н |
|
|
|
|
и |
|
у |
|
л |
|
|
|
|
|
|
|
|
з |
|
т |
|
|
|
|
в |
|
х |
|
15і |
н |
г |
і |
б |
і |
т |
о |
р |
и |
|
р |
|
|
|
|
н |
|
о |
|
з |
|
|
|
|
|
|
|
|
т |
|
а |
|
|
|
|
и |
|
м |
|
а |
|
|
|
|
|
|
|
|
и |
|
ц |
|
|
|
|
й |
|
а |
|
т |
|
|
|
|
|
|
|
|
в |
|
і |
|
|
|
|
|
|
|
|
о |
|
17с |
п |
о |
л |
у |
ч |
е |
н |
н |
я |
|
|
|
|
|
|
|
|
р |
|
|
|
|
|
|
|
|
и |
|
|
|
|
|
|
|
20а |
к |
т |
и |
в |
н |
і |
|
|
|
|
|
й |
|
|
|
Запитання до кросворду
По горизонталі.
1.Хімічні реакції, які відбуваються з поглинанням теплоти.
3.Зовнішній ефект, який супроводжує хімічну реакцію.
4.Чинник, який впливає на хімічну рівновагу.
5.Що сприяє збільшенню числа активних молекул і зростанню швидкості більшості хімічних реакцій?
6.Одна з характерних ознак хімічних реакцій.
10. Зовнішній ефект, який супроводжує хімічну реакцію.
11.Особливі біологічні каталізатори.
12. Хімічні реакції, які відбуваються одночасно у двох протилежних напрямках.
14.Назва речовин, які вступають в хімічну реакцію.
15. Речовини, які сповільнюють хімічні реакції.
17. Реакції, в результаті яких із двох або кількох речовин утворюється одна нова речовина.
20.Назва найбільш реакційноздатних молекул.
По вертикалі
1.Хімічні реакції, які відбуваються з виділенням теплоти.
2.Реакції, в результаті яких з однієї речовини утворюється дві або більше нових речовин.
7.Каталіз, який зменшує швидкість реакції.
8.Речовини, які пришвидшують швидкість хімічної реакції, але не входять до складу їх продуктів.
9.Реакції між простою і складною речовинами, у процесі яких атоми простої речовини заміщують атоми одного з елементів складної речовини, утворюючи нову просту й нову складну речовини.
12.Реакції, у процесі яких дві речовини обмінюються своїми складовими частинами, утворюючи дві нові речовини.
13.Чинник, який впливає на швидкість перебігу реакцій.
14.Рівновага, коли оборотні реакції не доходять до кінця, а пряма та зворотна реакції продовжують відбуватися з однаковою швидкістю.
16. Каталіз, який прискорює реакції.
18.Чинник, який впливає на швидкість перебігу реакції.
19.Процес зміни швидкості реакції під впливом каталізатора.
Запитання до кросворду
По горизонталі.
1.Хімічні реакції, які відбуваються з поглинанням теплоти.
3.Зовнішній ефект, який супроводжує хімічну реакцію.
4.Чинник, який впливає на хімічну рівновагу.
5.Що сприяє збільшенню числа активних молекул і зростанню швидкості більшості хімічних реакцій?
6.Одна з характерних ознак хімічних реакцій.
10. Зовнішній ефект, який супроводжує хімічну реакцію.
11.Особливі біологічні каталізатори.
12. Хімічні реакції, які відбуваються одночасно у двох протилежних напрямках.
14.Назва речовин, які вступають в хімічну реакцію.
15. Речовини, які сповільнюють хімічні реакції.
17. Реакції, в результаті яких із двох або кількох речовин утворюється одна нова речовина.
20.Назва найбільш реакційноздатних молекул.
По вертикалі
1.Хімічні реакції, які відбуваються з виділенням теплоти.
2.Реакції, в результаті яких з однієї речовини утворюється дві або більше нових речовин.
7.Каталіз, який зменшує швидкість реакції.
8.Речовини, які пришвидшують швидкість хімічної реакції, але не входять до складу їх продуктів.
9.Реакції між простою і складною речовинами, у процесі яких атоми простої речовини заміщують атоми одного з елементів складної речовини, утворюючи нову просту й нову складну речовини.
12.Реакції, у процесі яких дві речовини обмінюються своїми складовими частинами, утворюючи дві нові речовини.
13.Чинник, який впливає на швидкість перебігу реакцій.
14.Рівновага, коли оборотні реакції не доходять до кінця, а пряма та зворотна реакції продовжують відбуватися з однаковою швидкістю.
16. Каталіз, який прискорює реакції.
18.Чинник, який впливає на швидкість перебігу реакції.
19.Процес зміни швидкості реакції під впливом каталізатора.


про публікацію авторської розробки
Додати розробку
