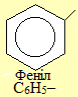
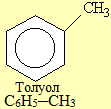
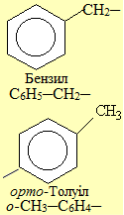
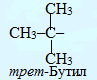
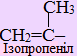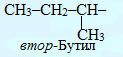Вуглеводні. Класифікація вуглеводнів.
КЛАСИФІКАЦІЯ ВУГЛЕВОДНІВ
Раніше вже наголошувалося, що органічна хімія охоплює в своїх дослідженнях майже 20 млн. сполук, переважна більшість яких має дуже складну будову. Тому розібратися в такому величезному масиві можна тільки, по-перше, на основі чіткої класифікації і, по-друге, на знайомстві з характерним и родовими ознаками окремих груп сполук залежно від особливостей їх будови і складу.
Будь-яку органічну сполуку можна розглядати як похідне відповідного вуглеводню, в якому один чи декілька атомів гідрогену заміщені вуглеводневими радикалами чи функціональними групами. Саме тому класифікація і номенклатура переважної більшості органічних сполук базується на основі класифікації та номенклатури вуглеводнів.
Вуглеводні – це органічні сполуки, молекули яких складаються з атомів двох елементів – карбону і гідрогену.
Кожний тип вуглеводнів утворює свій гомологічний ряд – послідовність подібних за будовою і властивостями сполук, склад якої відображається спільною загальною формулою.
За будовою карбонового ланцюгу вуглеводні поділяються на такі ряди (рис. 9.1):
- Аліфатичні вуглеводні (інша назва – ациклічні вуглеводні), які мають незамкнуту структуру – нормальну чи розгалужену;
-
Циклічні вуглеводні, в основі будови яких лежить замкнутий ланцюг. В свою чергу, циклічні вуглеводні включають:
- Карбоциклічні вуглеводні, замкнутий ланцюг яких може бути насиченим чи ненасиченим;
- Ароматичні вуглеводні, в основі будови яких лежить бензенове кільце складу С6Н6.
Залежно від характеру хімічних зв’язків між атомами карбону вуглеводні можуть бути такими (рис. 9.1):
- Насичені вуглеводні, в яких атоми карбону сполучені одинарними σ-зв’язками;
- Ненасичені вуглеводні, що містять кратні зв’язки – подвійні (один σ- і один π-), потрійні (один σ- і два π-зв’язки) чи їх комбінацію.
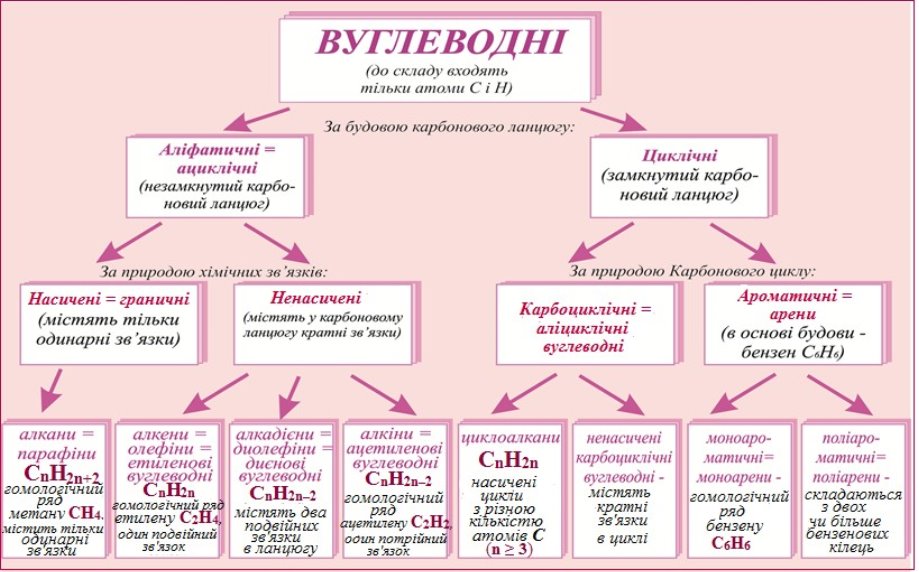
Рисунок 9.1 – Класифікація вуглеводнів за будовою карбонового ланцюгу і характером зв’язків між атомами карбону
Генетичною основою гомологічних рядів аліфатичних і аліциклічних вуглеводнів є гомологічний ряд насичених незамкнутих вуглеводнів – алканів (табл. 1).
Таблиця 1 – Гомологічний ряд алканів
|
Склад (брутто-формула) |
Раціональна структурна формула |
Назва |
|
СН4 |
СН4 |
Метан |
|
С2Н6 |
СН3–СН3 |
Етан |
|
С3Н8 |
СН3–СН2–СН3 |
Пропан |
|
С4Н10 |
СН3–(СН2)2–СН3 |
Бутан |
|
С5Н12 |
СН3–(СН2)3–СН3 |
Пентан |
|
С6Н14 |
СН3–(СН2)4–СН3 |
Гексан |
|
С7Н16 |
СН3–(СН2)5–СН3 |
Гептан |
|
С8Н18 |
СН3–(СН2)6–СН3 |
Октан |
|
С9Н20 |
СН3–(СН2)7–СН3 |
Нонан |
|
С10Н22 |
СН3–(СН2)8–СН3 |
Декан |
НАСИЧЕНІ ВУГЛЕВОДНІ
АЛІФАТИЧНІ НАСИЧЕНІ ВУГЛЕВОДНІ
Насичені аліфатичні вуглеводні утворюють гомологічний ряд алканів з загальною формулою CnH2n+2 (табл. 9.1). Інша назва алканів – парафіни (від грецького para affinis, тобто позбавлені хімічної спорідненості, малоактивні) – свідчить про їх невисоку реакційну здатність.
Номенклатура алканів. Згідно із замісниковою номенклатурою IUPAC для перших чотирьох членів гомологічного ряду алканів офіційно затверджені тривіальні назви: метан СН4, етан С2Н6, пропан С3Н8, бутан С4Н10, а також для розгалужених алканів
- ізобутану, ізопентану і неопентану:
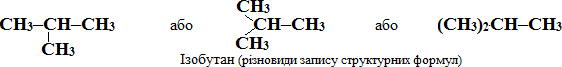
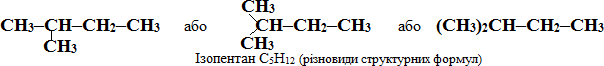
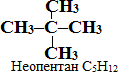
Назви решти алканів з нормальним (нерозгалуженим) ланцюгом складаються із кореня грецького чи латинського числівника, який зазначає кількість атомів С в головному ланцюгу, із додаванням суфікса -ан. Іноді перед назвою алкану нормальної будови додають букву «н-», щоб підкреслити його нерозгалужену структуру: наприклад, н-пентан СН3–СН2–СН2–СН2–СН3.
Алкани з розгалуженим ланцюгом вважаються похідними алкану нормальної будови, в яких один (чи декілька) атомів гідрогену заміщені вуглеводневим радикалом.
Назви алканів складають на підставі такого алгоритму:
- Вибирають найдовший карбоновий ланцюг – незалежно від геометричного розміщення структурної формули, наприклад:
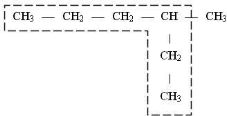
Якщо молекула містить два ланцюги однакової довжини, то головним вважають найбільш розгалужений.
-
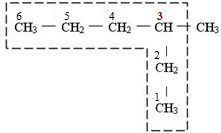
Нумерують арабськими цифрами атоми С головного ланцюгу, починаючи з того краю, до якого найближче знаходиться вуглеводневий радикал. Правильна нумерація ланцюгу для прикладу, що розглядається:
Інші варіанти нумерації не годяться, оскільки або лацюг не буде найдовшим, або атом С, сполучений з замісником-радикалом, не матиме найменшого номера:
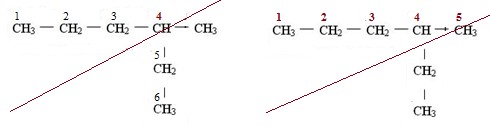
-
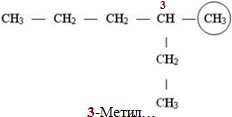
За допомогою цифри-локанту вказують положення радикалу в головному ланцюгу і називають радикал (табл. 2):
- Таблиця 2 – Номенклатура одновалентних вуглеводневих радикалів
|
Вихідний вуглеводень |
Радикал, утворений з вуглеводню |
Вихідний вуглеводень |
Радикал, утворений з вуглеводню |
|
|
|
СН2=СН2 Етен (Етилен) |
СН2=СН– Етеніл (Вініл) |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
-
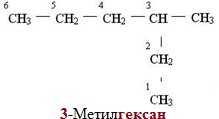
До назви радикалу додають назву головного ланцюгу, яка визначається назвою відповідного алкану (табл. 9.1) з такою ж кількістю атомів С: - Якщо карбоновий ланцюг містить декілька однакових замісників, то перед назвою родопочаткового алкану передбачається множувальний префікс, якому повинна відповідати кількість цифр-локантів. При цьому слід дотримуватися такого правила: при написанні назви сполуки між цифрами необхідно ставити кому, між цифрою і буквою – дефіс, а назви радикалів не відокремлювати від назви головного ланцюгу, як це показано у прикладі:
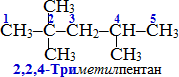
- У випадку декількох різних замісників, що знаходяться на однаковій відстані від обох країв структури, нумерацію починають з боку складнішого радикалу. Проте в назві вуглеводню замісники перелічуються в алфавітному порядку, причому, наявність множувальних часток на алфавітну послідовність переліку не розповсюджується. Наприклад:
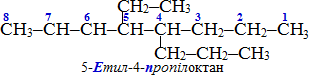
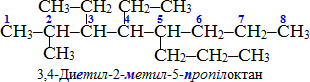
Хімічні властивості алканів визначаються особливостями будови їх молекул, що містять майже неполярні звязки С–С і С–Н, які зумовлюють дуже незначну реакційну здатність за звичайних умов. Однак за жорстких умов (нагрівання, опромінювання, змінення тиску, каталізатор) алкани вступають в реакції радикального заміщення (їх позначають символом SR від англ. substitution – заміщення, а індекс R вказує на вільний радикал). На відміну від поняття «вуглеводневий радикал», який є боковим фрагментом молекули, безпосередньо сполученим з головним ланцюгом, поняття
«вільний радикал» характеризує нейтральний атом чи частинку, що має неспарений електрон, за рахунок якого виявляє підвищену реакційну здатність. Вільні радикали завдяки підвищеній реакційній здатності можуть існувати протягом дуже короткого часу (приблизно 10–7 с); вони утворюються внаслідок гомолізу.
![]()
Гомоліз, або гомолітичний розрив зв’язку – руйнування спільної електронної пари хімічного зв’язку, внаслідок чого кожна одержана частинка набуває по одному неспареному електрону, утворюючи вільні радикали. Формули радикалів записують з крапкою, яка символізує неспарений електрон:
Як приклад механізму радикального заміщення SR можна навести реакцію галогенування алканів, у результаті яких утворюються галогенопохідні, наприклад, хлорування метану при опромінюванні розсіяним світлом (hν):
![]()
Механізм реакції SR складається з трьох стадій.
![]()
Перша стадія – ініціювання ланцюгу, під час якої завдяки опромінюванню відбувається гомолітичне розщеплення галогену на два вільні радикали, неспарений електрон яких зображується точкою:
Друга стадія – зростання ланцюгу. Радикал Cl атакує молекулу алкану і вириває з неї атом гідрогену. Це призводить до гомолітичного розриву звязку С–Н в метані, виникнення нового радикалу (СН3) і утворення нейтральної молекули хлороводню:
![]()
У метильному радикалі СН3 атом карбону переходить в стан sp2-гібридизації. Три гібридизовані орбіталі перекриваються з s-орбіталями трьох атомів Н, а на негібридизованій р-орбіталі знаходиться неспарений електрон. Велика реакційна здатність радикалу СН3 пояснюється прагненням неспареного електрона до утворення ковалентного -звязку (оскільки це дає виграш в енергії і стабілізує всю систему в цілому) та доступністю негібридизованої р-орбіталі для атаки.
![]()
Далі метильний радикал атакує молекулу хлору Cl2, в якій відбувається гомолітичний розрив звязку. Утворюється молекула хлорметану та новий радикал хлору:
При вивченні процесів галогенування алканів зясувалося, що найскладніше відбувається одержання хлорметану СН3Cl, а утворення ди-, три- і тетрагалогенопохідних (СН2Cl2, CHCl3 i CCl4) проходить дуже швидко і супроводжується виділенням теплоти. Це пояснюється дією негативного індуктивного ефекту атома хлору.
Індуктивний ефект І – це зміщення електронної густини по ланцюжку - звязків, що зумовлюється різницею електронегативності хімічно сполучених атомів. Напрямок індуктивного ефекту І позначають стрілкою, яка співпадає із σ- зв’язком, наприклад:
СН3–СН2→Cl, HO←СН2–СН2→Cl, СН3–СН2→COOH, СН3–СН2→NO2.

Наявність в молекулі полярного ковалентного σ-зв’язку спричиняє поляризацію найближчих двох-трьох σ-зв’язків, внаслідок чого виникають часткові заряди на сусідніх атомах, які позначаються грецькою буквою дельта з відповідним знаком: δ+ (позитивний) і δ– (негативний). Індуктивний ефект передається по системі -звязків із затуханням, а напрямок зміщення електронної густини σ-зв’язків залежить від природи замісників Х і Y:
Атом більш електронегативного елемента – електроноакцептор – відтягує електронну густину на себе і набуває часткового негативного заряду (–). Його партнер по -звязку має рівний за величиною дефіцит електронної густини, тобто частковий позитивний заряд (+), і називається електронодонор. Наприклад, в 1- бромбутані атом брому є електроноакцептором, а сполучений з ним атом карбону – електронодонором:

Залежно від напрямку зміщення електронної густини -звязку індуктивний ефект може бути позитивним (+І) і негативним (–І), наприклад:
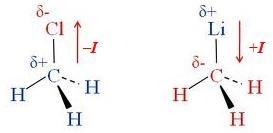
Негативний індуктивний ефект (–І) приписують тим атомам і групам, які зміщують електронну густину -зв’язку в свій бік, а позитивний індуктивний ефект (+І) – тим, від яких зміщується електронна густина -зв’язку.
Негативний індуктивний ефект (–І) виявляють електроноакцепторні атоми і атомні групи – тобто такі, що здатні притягувати електронну густину зв'язку сильніше, ніж атоми Н. До них належать: галогени (Hal: F, Cl, Br, I), =O, –OH, –NO2, – NH2 (або заміщені аміногрупи: –NHR, –NR2), –COOH, –CH=O, –COOR, –CN, –CH=CH2, – CCH, –CF3 тощо. Сила негативного індуктивного ефекту –І зменшується у ряді:

Для простих замісників (індивідуальних атомів) негативний індуктивний ефект зменшується в періоді справа наліво (F > O > N), а в групі періодичної системі – зверху униз (F > Cl > Br > І). У випадку замісників, які мають не частковий, а повний позитивний заряд, –І зростає зі збільшенням електронегативності атома, сполученого з атомом карбону (O+ >> N+), або електронегативності самого атому карбону, яка залежить від типу гібридизації його орбіталей і змінюються у напрямку: sp3 < sp2 < sp.

Позитивний індуктивний ефект (+І) виявляють електронодонори – атоми і атомні групи, що притягують електронні пари зв'язку слабше, ніж атоми Н; +І- ефект характерний для атомів металів Ме і насичених алкільних радикалів –CnH2n+1; причому, чим більш розгалужену будову має радикал, тим більший за величиною його позитивний індуктивний ефект:
Інколи формули цих радикалів записують у скороченому вигляді:
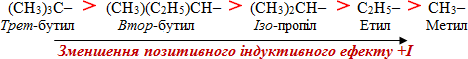
Загальний висновок щодо індуктивного ефекту: 1) виявляється тільки при наявності в молекулі полярних σ-зв’язків і атомів з різною електронегативністю;
- розповсюджується лише в одному напрямку через σ-зв’язки; 3) швидко затухає по ланцюгу σ-зв’язків; максимальна відстань впливу індуктивного ефекту – чотири σ- зв’язки.

Отже, завдяки дії негативного індуктивного ефекту (–І) атома хлору в молекулі СН3Cl відбувається поляризація -звязків С–Н порівняно з σ-зв’язками в молекулі СН4:
Це значно полегшує розрив σ-зв’язків С–Н і подальше заміщення атомів гідрогену в хлорметані СН3Cl атомами хлору Радикал хлору Cl знов атакує молекулу СН4 і повторюються всі перелічені процеси. У міру накопичення в реакційній суміші першого продукту реакції – хлорметану СН3Сl, він стає обєктом атаки вільним радикалом Cl, тому поступово утворюються не тільки монохлоропохідні, а і ди-, три-, тетрахлоропохідні:
![]()
![]()
![]()
![]()
![]()
![]()
Подібні процеси називаються ланцюговими реакціями, оскільки утворення в системі продуктів одного процесу автоматично ініціює протікання іншого.
![]()
![]()
![]()
Третя стадія – обрив ланцюгу відбувається при випадковому зіткненні двох вільних радикалів, внаслідок чого утворюється нейтральна молекула. Найчастіше обрив ланцюгу спостерігається при взаємодії двох радикалів хлору, але можуть бути й інші варіанти, тому в реакціях галогенування алканів, крім бажаних речовин, утворюється велика кількість побічних продуктів, наприклад:
Слід зазначити, що напрямок і швидкість реакцій радикального заміщення SR, зумовлюються дією багатьох чинників. Наприклад, галогенування алканів залежить, по- перше, від природи галогену: з F2 взаємодія проходить енергійно, іноді з вибухом, з Cl2 – при опромінюванні світлом (h), з Br2 – при ультрафіолетовому опромінюванні (УФ) чи при нагріванні, з І2 реакція практично не проходить. А по-друге, – від характеру атомів карбону: легше заміщується атом Н, сполучений з третинним карбоном, важче – з вторинним С і найгірше – з первинним С. Така залежність пояснюється дією індуктивних ефектів:


Як вже було зазначено, за звичайних умов алкани виявляють стійкість до дії концентрованих кислот, розчинів чи розплавів лугів і сильних окисників, за виключенням фтору F2. Однак при підвищених температурах у присутності каталізаторів алкани можуть піддаватися окисненню. Наведемо приклади процесів окиснення, що мають практичне значення:
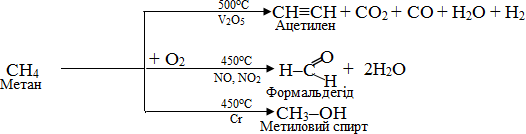
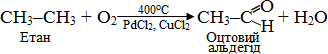
![]()
Алкани згоряють з виділенням великої кількості теплоти і утворенням вуглекислого газу і водяної пари:
![]()
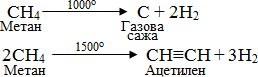
За жорстких умов алкани піддаються реакціям дегідрування – відщеплення атомів Н, яке може проходити різними шляхами. Практичного значення має крекінг алканів – процес хімічного розщеплення нафтових вуглеводнів при високих температурах (400 - 6000C) чи в присутності каталізаторів, внаслідок чого відбувається розрив звязків між атомами і утворюються вуглеводні, які можуть мати меншу кількість атомів карбону в молекулі, кратні звязки чи розгалужений ланцюг. Для метану найчастіше проводять піроліз – розклад при температурах вище 9000 за такими схемами:
Продуктами крекінгу алканів з довгим ланцюгом є суміш вуглеводнів різної довжини карбонового скелету і різної насиченості, а також водень. Наприклад, найбільш імовірні процеси під час крекінгу бутану протікають за схемами:
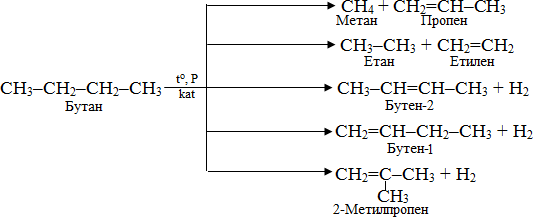
Алкани, що містять 6–9 атомів карбону, одночасно із дегідруванням піддаються циклізації та ароматизації, при якій утворюються бензин чи його гомологи з боковими ланцюгами, наприклад:

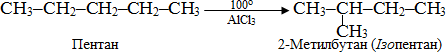
Ще одна характерна для алканів реакція – ізомерізація, що супроводжується зміненням структури карбонового ланцюгу при збереженні вихідного складу вуглеводню. Шляхом ізомерізації одержують із алканів нормальної будови розгалужені ізомери, що містять метильний радикал –СН3, сполучений з другим від краю основного ланцюгу атомом С, наприклад:
Важливим є процес нітрування алканів за реакцією Коновалова, яка протікає при дії на них розведеною нітратною кислотою (10-15%) при 110-1400С під невеликим тиском. Нітрування переважно відбувається селективно: легше на нітрогрупу заміщується атом гідрогену біля третинного атома С, потім – біля вторинного і в останню чергу – біля первинного. Продуктами нітрування є нітросполуки, наприклад:
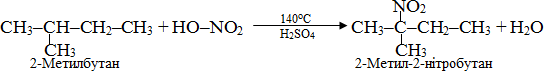
Добування алканів. Сировиною для одержання алканів є природні джерела: нафта, попутні нафтові та природничі гази, вугілля, деревина, торф. Серед синтетичних методів одержання алканів слід відмітити гідрогенізацію вугілля чи графіту; у такий спосіб найчастіше добувають метан та синтетичні бензини:
![]()
![]()
Застосовується також конверсія синтез-газу (суміш чадного газу і водню):
![]()
![]()
Важливим методом одержання алканів є гідрування ненасичених аліфатичних і аліциклічних вуглеводнів – приєднання атомів Н, наприклад:
Щоб оцінити здатність алкенів різної будови до приєднання Н2, корисно брати до уваги правило Лебедєва: алкени гідруються тим легше, чим менше замісників міститься біля подвійного звязку. Відповідно до цього правила можна прогнозувати, що пропен нормальної структури легше приєднує Н2 порівняно з розгалуженим 2-метилпропеном:
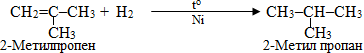
Алкіни, незважаючи на більшу ненасиченість, гідруються дещо важче, ніж алкени, причому реакція проходить у два етапи:
![]()
Якщо вуглеводень містить одночасно подвійні та потрійні зв’язки, до водень спочатку приєднується до подвійного зв’язку, а потім – до потрійного, наприклад:
![]()
циклу:
Гідрування насичених циклічних вуглеводнів супроводжується руйнуванням
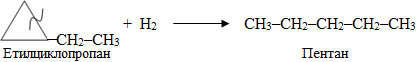
Серед лабораторних методів найпростішим є гідроліз карбіду алюмінію:
![]()
Алкани з невеликою кількістю атомів С в ланцюгу отримують при хімічному перетворенні галогенопохідних, солей чи кислот. Часто використовують метод дегалогенування – відщеплення атомів галогенів (Hal) від насичених галогенопохідних, наприклад, за реакцією Вюрца при взаємодії галогенопохідного з металічним натрієм при незначному нагріванні, внаслідок чого утворюється алкан, що має вдвічі довший ланцюг, ніж вихідний галогеналкан:
![]()
![]()
![]()
![]()
Однак слід брати до уваги, що при дії натрієм на суміш двох різних галогенопохідних реакція одночасно перебігає за трьома різними схемами з утворенням суміші трьох алканів:
Ще одним поширеним методом отримання алканів є декарбоксилювання солей (або, точніше, карбоксилатів) лужних металів – відщеплення карбоксильної групи (СООН чи СООМе) за реакцією Дюма, або реакція лужного плавлення, що проходить відповідно до загальної схеми, на якій для наочності виділено склад побічного продукту – натрій карбонату:
![]()
Декарбоксилюванню за реакцією Дюма піддають не тільки солі (СnH2n+1–COOMe), але і нерозчинні карбонові кислоти (СnH2n+1–COOH, особливо при n 6):
![]()
![]()
![]()
![]()
Декарбоксилювання солей шляхом інколи проводять при електролізі водних розчинів солей (карбоксилатів) лужних металів – реакція Кольбе. При цьому на аноді внаслідок окиснення кислотного залишку утворюються алкільні радикали (СnH2n+1), які мають підвищену реакційну здатність завдяки наявності неспареного електрона і дуже швидко сполучаються один з одним в молекулу алкану з більш довгим ланцюгом:
НЕНАСИЧЕНІ АЛІФАТИЧНІ ВУГЛЕВОДНІ
ЕТИЛЕНОВІ ВУГЛЕВОДНІ
Ненасичені аліфатичні вуглеводні з одним подвійним зв’язком в головному ланцюгу утворюють гомологічний ряд алкенів з загальною формулою CnH2n, де n 2. Інші назви алкенів – етиленові вуглеводні, олефіни.
Номенклатура алкенів. При утворюванні назви етиленового вуглеводню, суфікс -ан відповідного алкану замінюють на -ен (чи -єн), який вказує на подвійний зв’язок: етан СН3–СН3, етен СН2=СН2. У назвах сполук з більш довгим ланцюгом після суфікса (через дефіс) необхідно вказувати локант – номер атома С в карбоновому ланцюгу, від якого починається подвійний зв’язок.
Для перших членів гомологічного ряду алкенів існують тривіальні назви, які склалися історично – для етену С2Н4 – етилен (причому, назва «етилен» затверджена правилами IUPAC і вважається більш переважною), для пропену С3Н6 – пропілен, для бутену С4Н8 – бутилен:
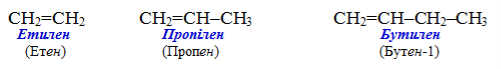
Згідно з замісниковим способом номенклатури IUPAC розроблені загальні правила
для формування назви алкену:
- в нерозгалужених алкенах нумерують атоми карбону з того краю, до якого найближче знаходиться подвійний звязок;
- в назві відповідного алкана з тим же числом атомів карбону замінюють суфікс -ан на -ен, а після нього через дефіс вказують номер атома С, від якого починається подвійний звязок, наприклад:
![]()
- у випадку розгалуженої структури головним ланцюгом вважається той, що містить подвійний звязок, навіть якщо цей ланцюг не буде найдовшим;
-
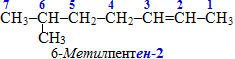
якщо вуглеводневий радикал і подвійний звязок знаходяться на однакових відстанях від країв молекули, то нумерацію проводять так, щоб подвійний звязок отримав найменший номер, наприклад: - вуглеводневі радикали позначають за допомогою префіксів: метил-, етил- тощо (табл. 9.2), а їх положення у ланцюгу вказують локантом – цифрою, що відповідає номеру атома карбона, з яким сполучений даний радикал; у випадку декількох однакових радикалів застосовують множувальні префікси ди-, три-, тетра-, перед якими записують всі номери атомів карбону, наприклад:
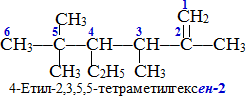
- перелічують вуглеводневі радикали в алфавітному порядку. Назви вуглеводневих радикалів, що мають подвійний звязок, зустрічаються досить рідко.
Якщо необхідно підкреслити, що алкен належить до просторових (геометричних) ізомерів, до його назви додають спеціальний префікс: цис-, коли продовження головного ланцюгу розміщується з одного боку відносно подвійного зв’язку, чи транс- – коли з різних боків, наприклад, для бутену-2:

Хімічні властивості алкенів визначаються у першу чергу їх ненасиченістю.
Дл алкенів характерні реакції приєднання реагентів до подвійного звязку, наприклад:

Слід зазначити, що взаємодія алкенів з бромом або з бромною водою – це якісна реакція на кратний зв’язок (як подвійний, так і потрійний), оскільки внаслідок неї відбувається знебарвлення Br2.

![]()

Напрямок приєднання реагентів до алкенів по місцю подвійного зв’язку визначається відповідно до правила Марковникова: При взаємодії несиметричних алкенів з полярними молекулами типа НХ атом гідрогену приєднується до найбільш гідрогенізованого атома карбону (тобто сполученого із більшою кількістю атомів Н), який утворює подвійний звязок. Наприклад, згідно з правилом Марковникова проходять реакції гідратації та гідробромування (приєднання води і галоген оводню відповідно) несиметричних алкенів:
Виключенням з правила Марковникова є взаємодія алкенів з HBr у присутності пероксидних сполук (Н2О2, С6Н5СОООН, Na2O2), які викликають пероксидний ефект Харраша: атом Н приєднується до менш гідрогенізованого атома карбону, а атом Hal – до більш гідрогенізованого атома С проти правила Марковникова, наприклад:
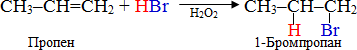
Важливою серед реакцій приєднання є взаємодія алкенів з озоном – реакція Гарієса, яку використовують для ідентифікації положення подвійного звязку.
Приєднання О3 на початковому етапі приводить до нестійких вибухових продуктів –

озонідів, при подальшому гідролізі яких утворюються карбонільні сполуки:
Залежно від складу одержаних альдегідів чи кетонів встановлюють положення подвійного звязку у вихідному алкені.
Для алкенів з довгим ланцюгом можуть проходити реакції заміщення атомів гідрогену в -положенні відносно подвійного звязку. Як правило, це реакції окиснення при температурах 350–5000С киснем в присутності каталізатора V2O5, причому залежно від тривалості зіткнення вихідних речовин утворюються різні продукти:
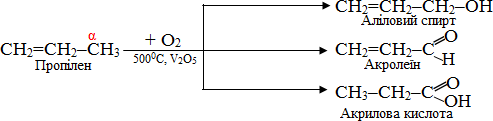
Часто замість кисню в якості окисника застосовують хлор:
![]()
Для етиленових вуглеводнів важливою є реакція полімеризації – процес послідовного приєднання молекул ненасиченої сполуки (мономеру) одна до одної за рахунок розриву -звязків і утворення нових -звязків між окремими елементарними ланками в макромолекулі високомолекулярної сполуки (полімеру), яка при цьому одержується. Елементарна ланка – фрагмент структури, що багаторазово повторюється в макромолекулі полімеру. Кількість елементарних ланок дорівнює кількості молекул мономеру, які взяли участь в реакції полімеризації, і називається ступінь полімеризації n.
Внаслідок полімеризації одна макромолекула високомолекулярної сполуки (скорочено – ВМС) може утворюватися з різної кількості молекул мономеру (n), тому полімер звичайно складається з макромолекул різної довжини і різної молекулярної маси. Молекулярна маса полімеру – це середня величина, яку розраховують як добуток молярної маси мономеру на ступінь полімеризації за формулою
МВМС = n·Ммономеру.

Схематично процес полімеризації записують так:
Добування етиленових вуглеводнів у промисловості – це, по-перше, перегонка нафти (розділення газуватої частини продуктів крекінга нафти на фракції під тиском чи при зниженій температурі). Таким чином виділяють з нафти олефіни складу С6Н12-С13Н26. По-друге – вже розглянутий раніше піроліз алканів. Крім того, для одержання етиленових вуглеводнів розроблено багато реакцій елімінування, при яких відбувається відщеплення двох атомів, чи групи атомів від сусідніх атомів карбону, внаслідок чого між ними виникає -звязок. Наприклад:
- дегідрування алканів при їх піролізі:
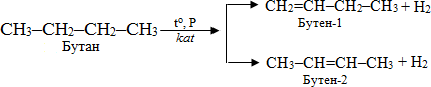
-
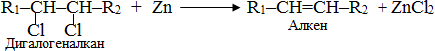
дегалогенування віцінальних дигалогенопохідних, в яких атоми галогену сполучені з двома сусідніми атомами С, за допомогою магнію чи цинку: - дегідратація спиртів – відщеплення води з утворенням алкенів:
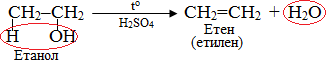

Спирти несиметричної будови піддаються елімінуванню відповідно до правила Зайцева: При відщепленні молекул типу НХ від спиртів чи галогенопохідних найбільш легко відривається атом гідрогену від найменш гідрогенізованого атома карбону (тобто такого, що сполучений з більшою кількістю атомів Н). Наприклад:
- дегідрогалогенування моногалогенопохідних – відщеплення атомів Н і Hal від двох сусідніх атомів карбону, яке проводиться при дії на галогенопохідні спиртовим розчином лугу. У випадку несиметричних галогеновуглеводнів реакція відбувається згідно з правилом Зайцева, наприклад:
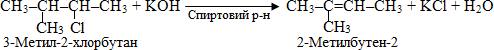
![]()
АЦЕТИЛЕНОВІ ВУГЛЕВОДНІ
Ненасичені аліфатичні вуглеводні з одним потрійним зв’язком в головному ланцюгу утворюють гомологічний ряд алкінів з загальною формулою CnH2n–2, де n 2. Інші назви алкінів – ацетиленові вуглеводні.
Номенклатура алкінів. Відповідно до вимог ІUPAC назви алкінів утворюють шляхом замінення суфіксів -ан у назвах алканів на -ін (чи -ин) із вказуванням номеру атома карбону, з якого починається потрійний звязок. Деякі алкіни частіше називають за тривіальною номенклатурою, наприклад:
![]()
Ацетиленові вуглеводні з потрійним зв’язком у крайньому положенні об’єднуються спільною назвою – термінальні алкіни.
![]()
Якщо сполука містить одночасно зв’язки різної кратності, у назві спочатку наводять суфікс подвійного зв’язку (-ен), а потім – потрійного (-ін). При цьому, якщо обидва кратні зв’язки знаходяться на однакових відстанях від країв карбонового ланцюгу, атоми карбону нумерують так, щоб подвійний зв’язок одержав найменший номер. Якщо ж потрійний зв’язок розташований ближче до краю, то нумерацію починають від найближчого до нього боку, але в назві все одно спочатку вказують подвійний зв’язок, наприклад:
Хімічні властивості ацетиленових вуглеводнів зумовлюються наявністю потрійного звязку, який за реакційною здатністю подібний до подвійного, але не перевершує його за активністю. Це пояснюється компактнішим розташуванням - електронної густини і меншої доступністю потрійного звязку до дії реагентів порівняно з алкенами. З цієї причини реакції приєднання до алкінів відбуваються повільніше, ніж з алкенами.
Реакції приєднання протікають у дві стадії: спочатку руйнується один -звязок і утворюються похідні алкенів (як правило, транс-ізомери), а при розриві другого -звязку
-

похідні алканів, наприклад:
Зважаючи на те, що потрійний звязок має меншу реакційну здатність порівняно з подвійним, при обмеженій кількості галогену за певних умов стає можливим селективне приєднання Hal2 та інших реагентів саме до подвійного звязку при одночасній наявності в молекулі і потрійного звязку, наприклад:
![]()
Важливою властивістю алкінів є їх гідратація за реакцією Кучерова – приєднання води по місцю потрійного зв’язку при каталітичній дії солей меркурію (ІІ) і сульфатної кислоти. При цьому як проміжний продукт утворюються вторинні вінілові спирти (або вторинні еноли, в яких група ОН сполучена з sp2-гібридизованим атомом С). Еноли дуже швидко ізомерізуються в кетони. З несиметричними алкінами реакція проходить згідно з правилом Марковникова:
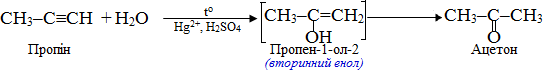


Гідратація всіх інших алкінів теж дає виключно кетони, наприклад, лінійні ізомери бутинів складу С4Н6, в яких потрійний зв'язок розміщується біля С1 чи С2, при гідратації дають один кетон:
Єдиним винятком є ацетилен, який внаслідок реакції Кучерова утворює не кетон, а альдегід:


Останнім часом гідратацію ацетилену проводять не за способом Кучерова, а використовуючи інші каталізатори:
Термінальні алкіни здатні відщеплювати атом Н при потрійному звязку і виявляти слабкі кислотні властивості за рахунок помітної поляризації звязку С–Н. Це зумовлюється, по-перше, виникненням часткового негативного заряду на атомі карбону завдяки підвищеній електронній густині потрійного звязку, а по-друге, – sp- гібридизованим станом атома С, що збільшує його відносну електронегативність (порівняно із sp2- i sp3-гібридизованими атомами карбону). Названі чинники сприяють заміщенню атома Н при потрійному звязку на метал при дії відповідних реагентів, наприклад:
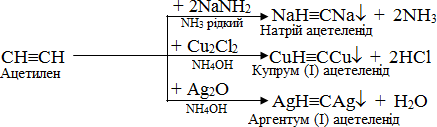
Реакції утворення алкінідів купруму (І) і арґентуму (І) є якісними на наявність потрійного зв’язку в крайньому положенні, тому їх використовують для ідентифікації термінальних алкінів.
Важливою особливістю алкінів є схильність до олігомеризації – тобто сполучення двох чи декількох молекул алкіну (мономера), внаслідок чого утворюється ненасичений олігомер – продукт нормальної чи циклічної будови, Наприклад:
- лінійна димеризація – сполучення двох молекул алкіну. Наприклад, для ацетилену:
![]()
-
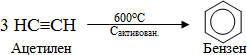
циклічна тримеризація – реакція Зелінського-Казанського:
Гомологи ацетилену в присутності металоорганічних сполук хрому, нікелю і кобальту перетворюються в похідні бензену:

-

циклічна тетрамеризація, яка дає можливість одержувати ненасичені циклічні вуглеводні, що містять чотири атоми карбону в ланцюгу:
Добування алкінів. У звязку з великим промисловим значенням ацетиленових вуглеводнів розроблені численні способи добування С2Н2 та його гомологів:
-
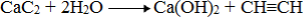
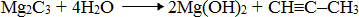
гідроліз карбідів кальцію і магнію дає ацетилен і пропін відповідно:
- піроліз вуглеводнів. Ацетилен одержують при швидкому пропусканні (тривалість реакції 0,01-0,1с) метану між електродами під час електричного розряду:
![]()
![]()
або через полумя горілки у суміші з киснем (окиснювальний піроліз):
- елімінування віцінальних дигалогенопохідних (які містять атоми галогену біля двох сусідніх атомів карбону) чи гемінальних дигалогенпохідних (які містять атоми галогену біля одного атому карбону) – при дії на них спиртовим розчином лугу:

![]()
При елімінуванні несиметричних гемінальних дигалогенопохідних виконується правило Зайцева:
- дегалогенування віцинальних тетрагалогенопохідних цинковим пилом чи магнієм:
![]()
-

із напівацетиленідів при їх взаємодії з галогеналканами отримують термінальні алкіни з кінцевим потрійним звязком:
Цим же способом можна одержувати алкіни, які містять потрійний звязок усередині ланцюгу:
![]()
АРОМАТИЧНІ ВУГЛЕВОДНІ
Ароматичні вуглеводні, або арени – це карбоциклічні вуглеводні, в основі будови яких лежить бензенове кільце.
Поняття ароматичність обєднує сукупність певних ознак, які визначає правило Хюккеля: Ароматичність сполуки – це наявність замкнутої спряженої системи, що має плоский циклічний -скелет і 4n+2 усуспільнені -електрони, де n =1,2,3…
Структура молекули бензену С6Н6 ідеально відповідає правилу ароматичності Хюккеля. В ній всі шість атомів С перебувають у стані sp2-гібридизації, тому вісі трьох sp2-гібридизованих орбіталей кожного атома С знаходяться на одній площині під валентним кутом 1200 (рис. 9.3 а), а вісь четвертої, негібридизованої рz-орбіталі розміщується перпендикулярно до них (рис. 9.3 б). Отже, кожний атом карбону утворює за рахунок sp2-гібридизованих орбіталей три -звязки: два – із сусідніми атомами С, а третій – при перекриванні зі сферичною s-орбіталлю атома Н. Оскільки вісі всіх -звязків в молекулі С6Н6 лежать на одній площині, шість атомів С без напруження замикаються через -звязки в правильний шестикутник, утворюючи -скелет молекули. Шість негібридизованих рz-орбіталей з компланарними осями (рис. 23.4 б) взаємно перекриваються, внаслідок чого виникає єдина делокалізована -електронна хмара – колове спряження (рис. 23.4 в). Найбільша електронна густина в цій спряженій системі розміщується над і під площиною -скелету молекули і однаковою мірою охоплює всі шість атомів С у циклі. Колове спряження в молекулі бензену зумовлює велику енергією спряження (або енергію делокалізації), що дорівнює 150,7 кДж/моль.
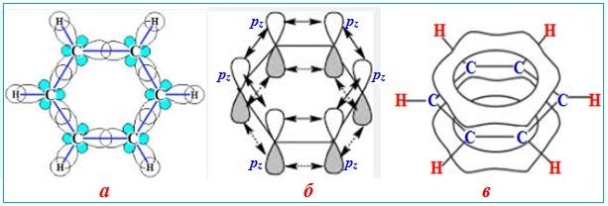
Рисунок 9.3 – Будова молекули бензену: а) -скелет молекули, утворений σ-зв‘язками (шість С–С при взаємному перекриванні sp2-гібридизованих орбіталей сусідніх атомів карбону і шість С–Н при перекриванні sp2-гібридизованих орбіталей атомів карбону з s- орбіталями атомів Н); б) компланарне розташування негібридизованих pz-орбіталей перпендикулярно до площини σ-скелету; в) утворення колового спряження делокалізованої -електронної хмари над і під площиною σ-скелету молекули
Класифікація і номенклатура ароматичних вуглеводнів. За кількістю бензенових кілець арени поділяються на дві групи.
- Моноядерні арени, до них належить сам бензен С6Н6 та його гомологи, в яких один чи декілька атомів гідрогену заміщені на бокові ланцюги (насичені чи ненасичені). Назви гомологів бензену утворюють від родопочаткової структури – бензену (стара назва, яка зустрічається досить часто, – бензол), перед якою наводять назви радикалів
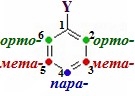
(табл. 9.2) у бокових ланцюгах та їх положення. Для багатьох моно ядерних аренів вживають тривіальні назви, які набули настільки широкого розповсюдження, що їх було введено в правила номенклатури IUPAC. Якщо бензенове кільце містить два однакові радикали, то залежно від їх взаємного розташування використовують додаткові префікси – орто- (2,6-положення відносно головного замісника Y), мета- (3,5- положення) і пара- (4-положення):
Приклади назв моноядерних аренів згідно з замісниковим методом номенклатури IUPAC (у дужках наведені більш поширені офіційні назви, які мають тривіальне походження):



Дуже часто для називання складних сполук необхідно знати назви ароматичних радикалів – арилів. Арили позначають загальним символом Ar (табл. 9.2):

- Поліядерні арени складаються з декількох бензенових ядер. Вони, у свою чергу, поділяються на конденсовані, в яких бензенові кільця мають спільні атоми карбону) і неконденсовані, або ізольовані, в молекулах яких бензенові цикли розділені -зв’язком чи метиленовою групою –СН2– (однією чи двома).
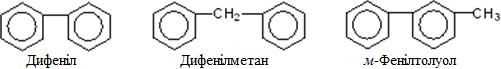
Назви неконденсованих (ізольованих) поліаренів утворюються переважно за радикально-функціональним способом IUPAC:
Для найпоширеніших конденсованих поліядерних аренів вживаються такі назви:
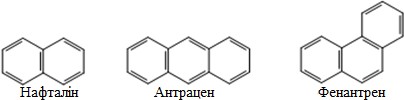
Хімічні властивості ароматичних вуглеводнів зумовлюються, в першу чергу, наявністю спряженої системи і високою енергією де локалізації. Тому для збереження енергетично вигідного стану бензен і його гомологи вступають переважно в реакції заміщення, оскільки при цьому не порушується їх ароматичність. З цієї причини, не зважаючи на велику ненасиченість, арени не дають якісних реакцій на кратний зв’язок (знебарвлення бромної води чи розчину KMnO4). Однак за жорстких умов (при тривалому нагріванні в присутності сильних каталізаторів) бензен здатний вступати в різноманітні реакції заміщення з відповідними реагентами, як це показано на схемі:

Реакції приєднання за звичайних умов для бензену не характерні, оскільки вони супроводжуються порушенням ароматичності і вимагають великої витрати енергії. Тому ці реакції проводяться в дуже жорстких умовах, наприклад, гідрування і хлорування:


Гомологи бензену, що мають боковий радикал, вступають в реакції заміщення легше порівняно з бензеном. Докладніше властивості гомологів бензену буде розглянуто пізніше (§ 9.5), а тут наведемо тільки загальну тенденцію: внаслідок таких реакцій одночасно утворюються три продукти: о-, n- і м-ізомери, але їх відносна кількість буде різною. Наприклад, при нітруванні толуену продукти утворюються у таких масових співвідношеннях (зазначені на схемі у дужках):

Добування ароматичних вуглеводнів. Більшість аренів мають важливе практичне значення, тому їх виробляють у великій кількості багатьма способами.
- Фракційне розділення камяновугільної смоли. Із 1 т вугілля внаслідок коксування одержують близько 55 кг камяновугільної смоли, з якої виділяють приблизно 0,9 кг бензену, 2,3 кг нафталіну, 200 г толуену, 45 г ксилолів, а також невеликі кількості - і - метилнафталінів, антрацену, фенантрену, дифенілу. Оскільки коксування вугілля – це багатотоннажне виробництво, виділення аренів із смоли досягає великих обємів.
-

Ароматизація насичених вуглеводнів нафти, під час якої проходять процеси циклізації, дегідрування, ізомеризації, наприклад: - Тримеризація алкінів при пропусканні їх над активованим вугіллям при високій температурі – реакція Зелінського-Казанського:

-

Лужне плавлення солей – реакція Дюма: - Відновлення фенолів при їх перегонці з цинковим порошком
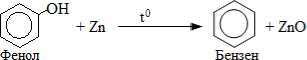
- Гідроліз бензенсульфонових кислот гострою парою:
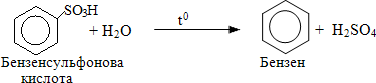
Одержання гомологів бензену включає і додаткові способи, крім перелічених:
- із галогенопохідних за реакцією Вюрця-Фіттігу:

-
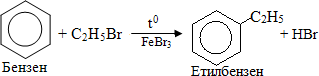
алкілювання за реакцією Фріделя-Крафтса:


про публікацію авторської розробки
Додати розробку