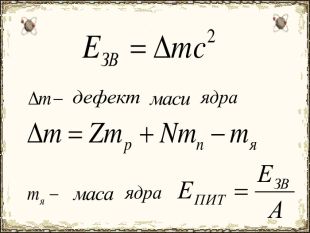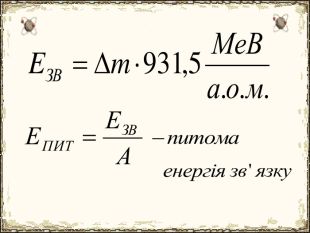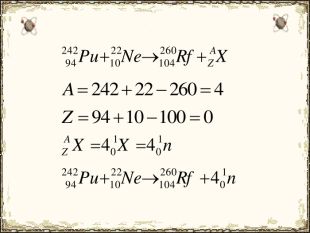Ядерна фізика 11 клас
Про матеріал
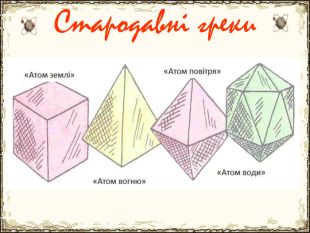
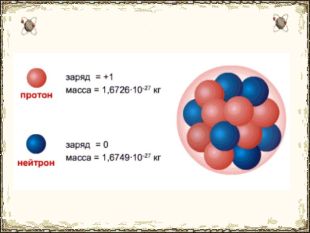
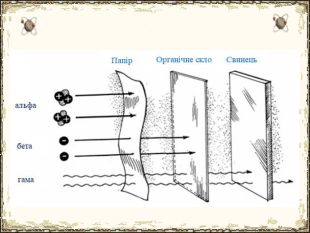
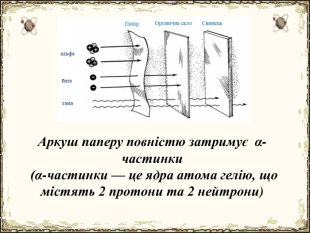
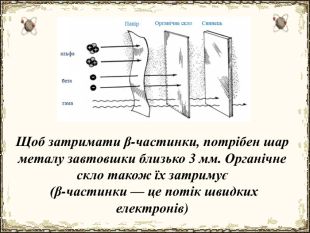
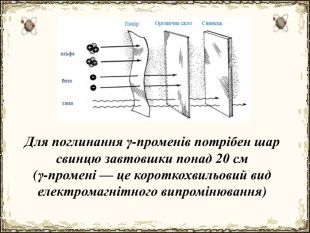
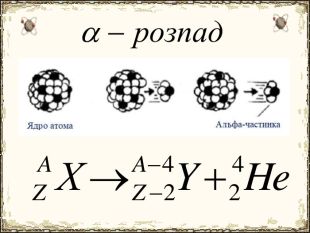
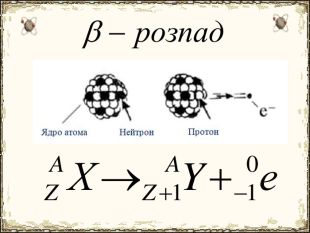
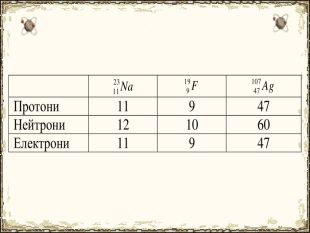
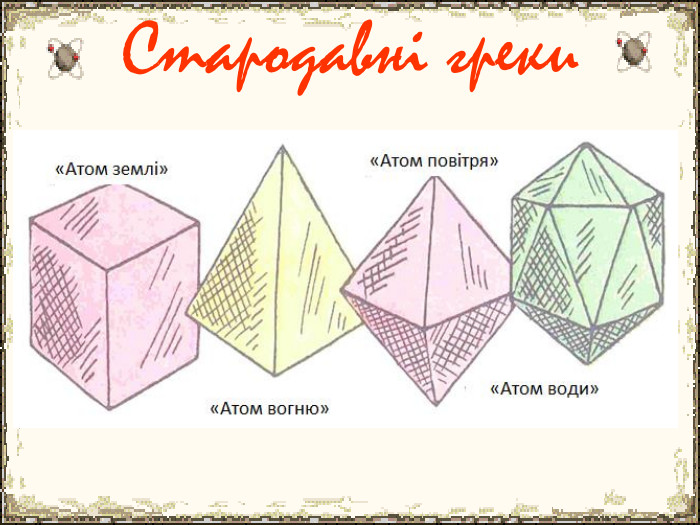
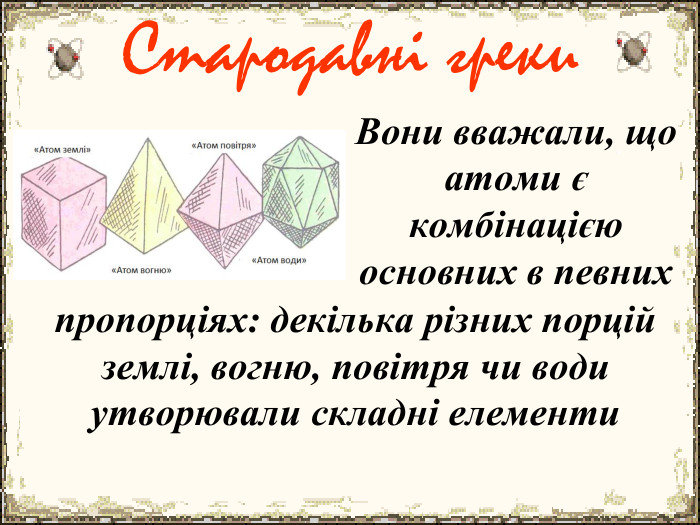
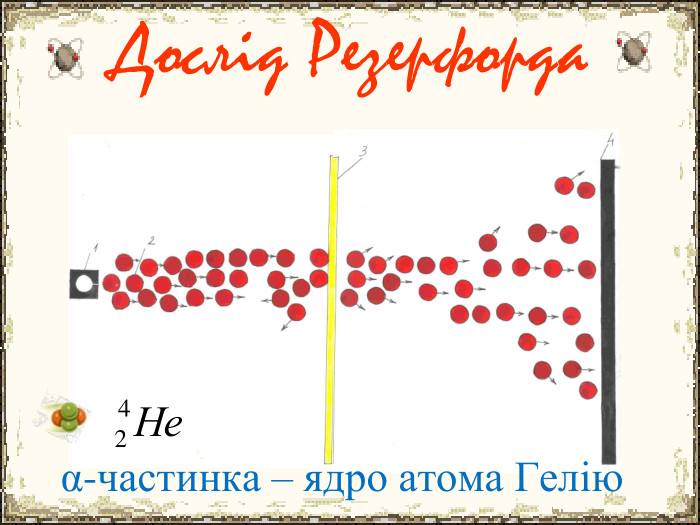
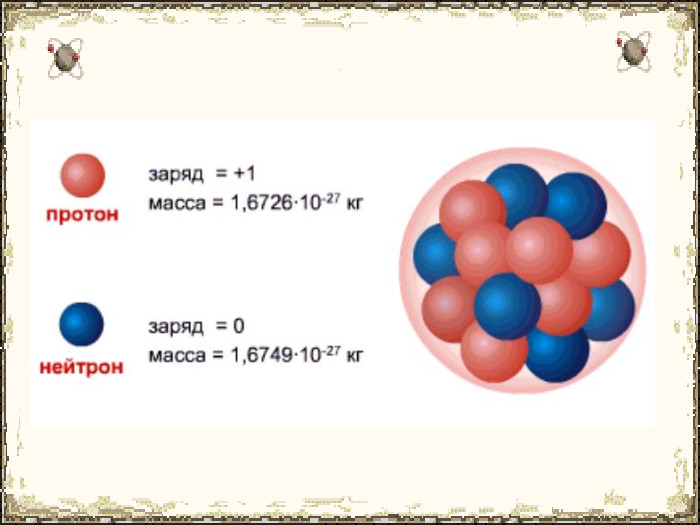
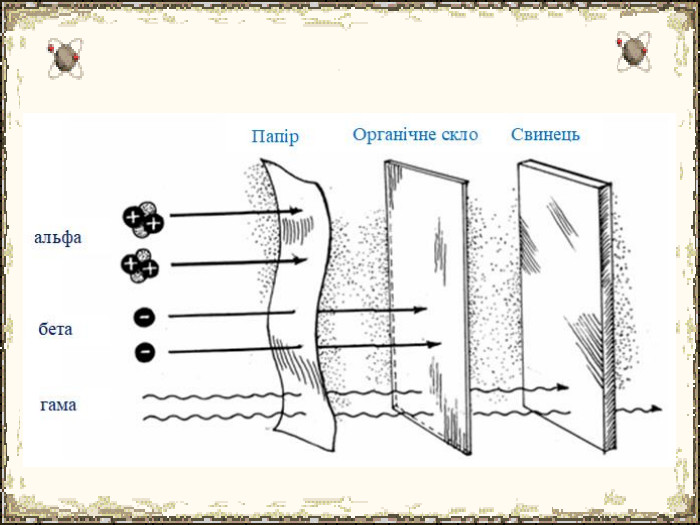
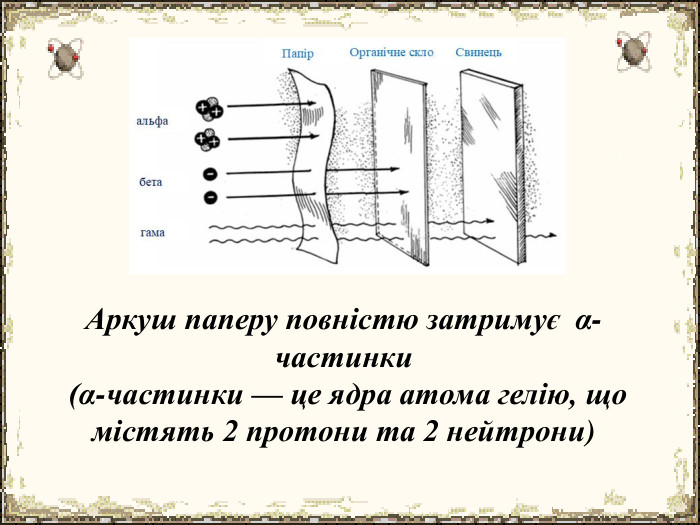
Матеріал містить додаткову інформацію щодо історії вивчення атома та ядерної моделі атома, складу атомних ядер та ядерних реакцій, енергії зв'язку, радіоактивності, закону радіоактивного розпаду.
Перегляд файлу











































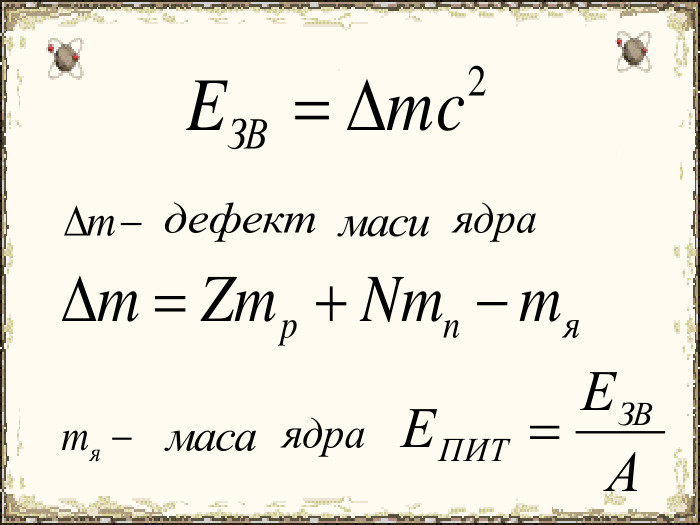
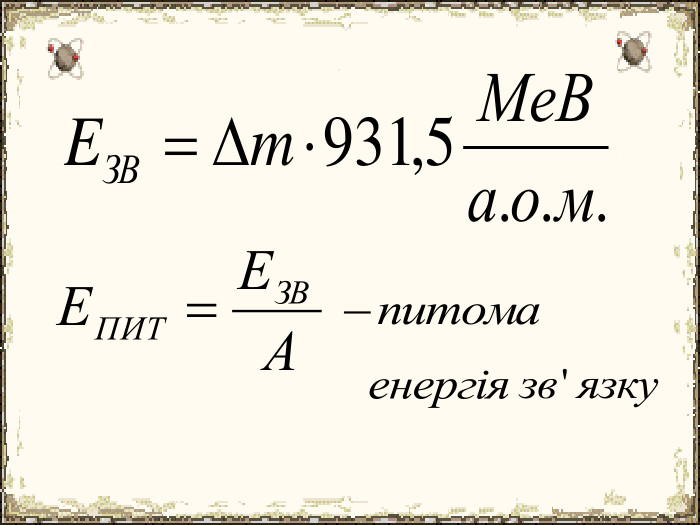


















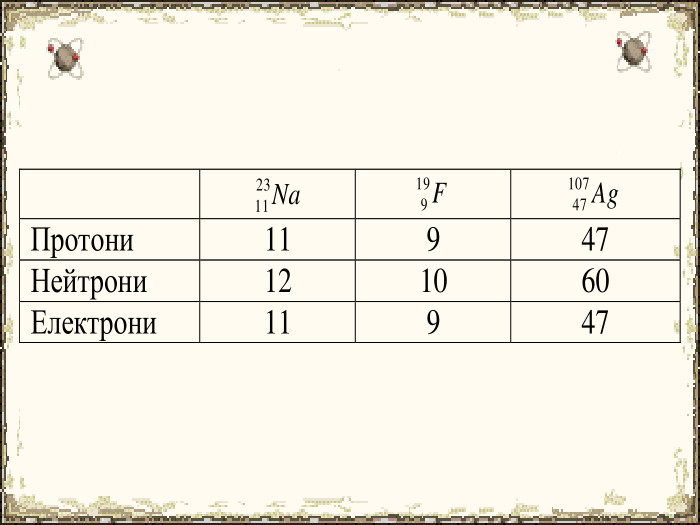

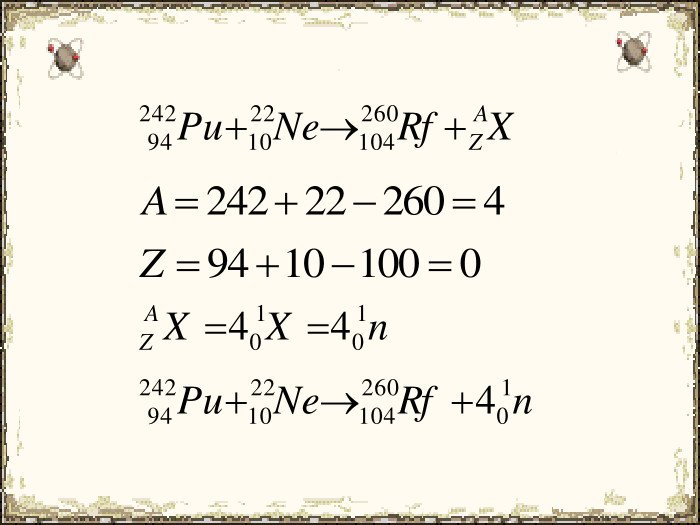






Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку
Рекомендовані матеріали
Схожі матеріали
docx
4606
0
docx
13136
0