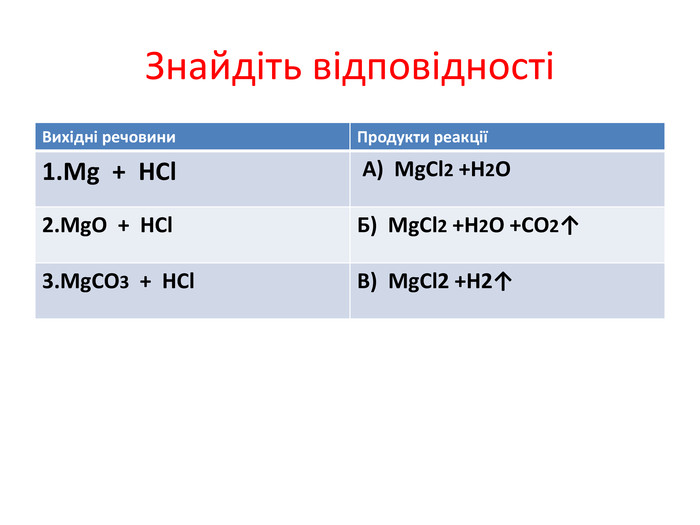
8 клас хімія Хімічні властивості кислот
Про матеріал
Презентація, яка допоможе вчителю формувати компетентності у учнів, зацікавить їх , буде сприяти розвитку логічного мислення і бажання пізнавати нове Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку