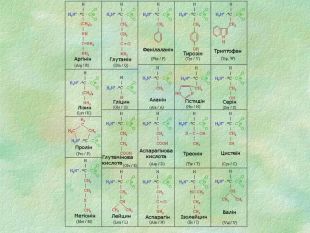
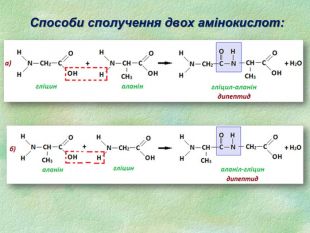
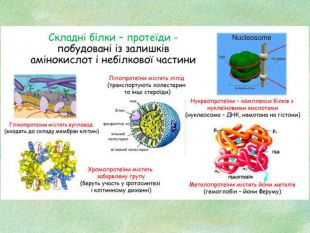
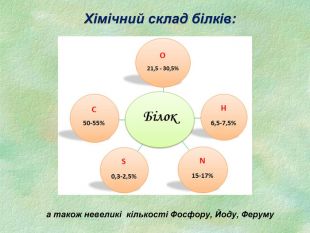
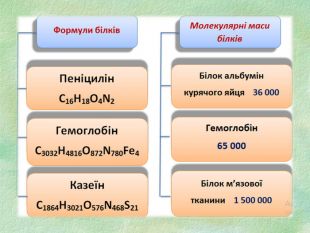
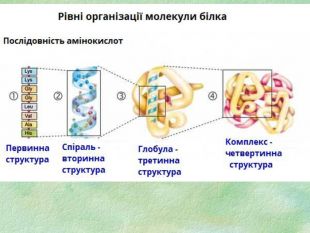
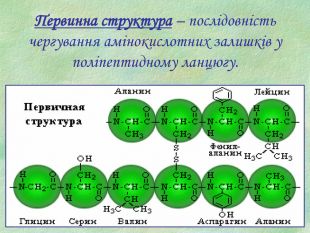
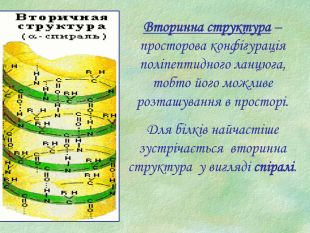
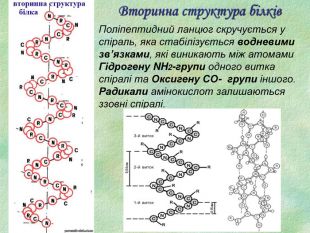
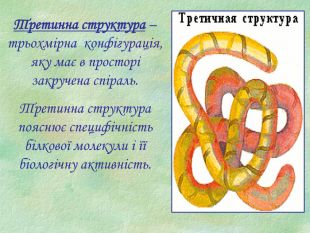
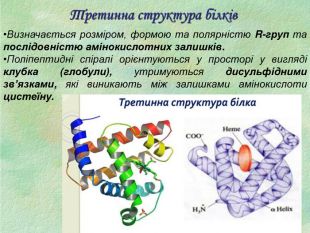
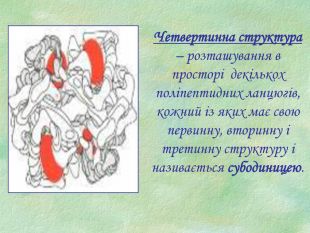
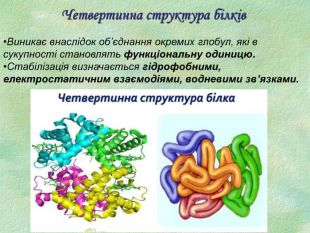
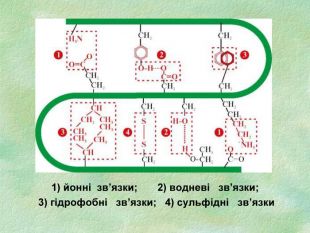
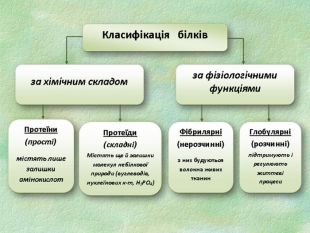
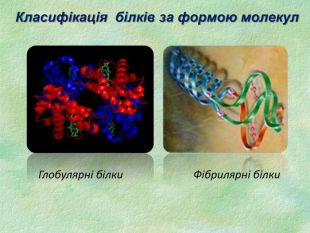
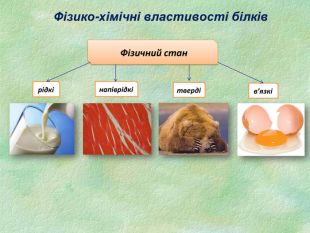
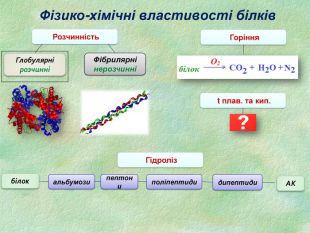
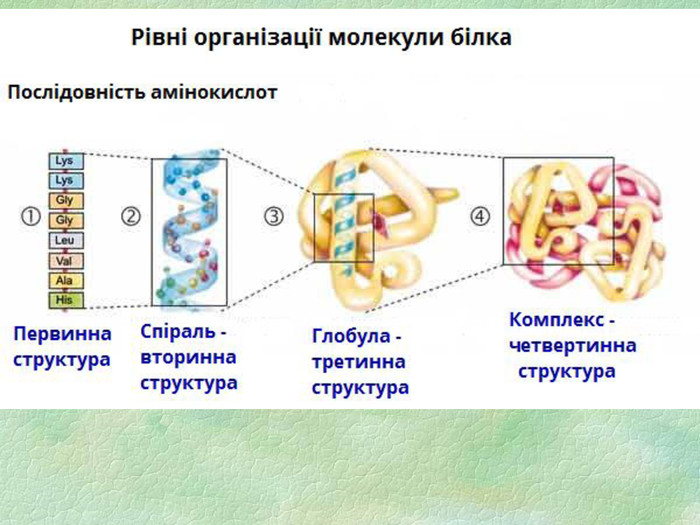
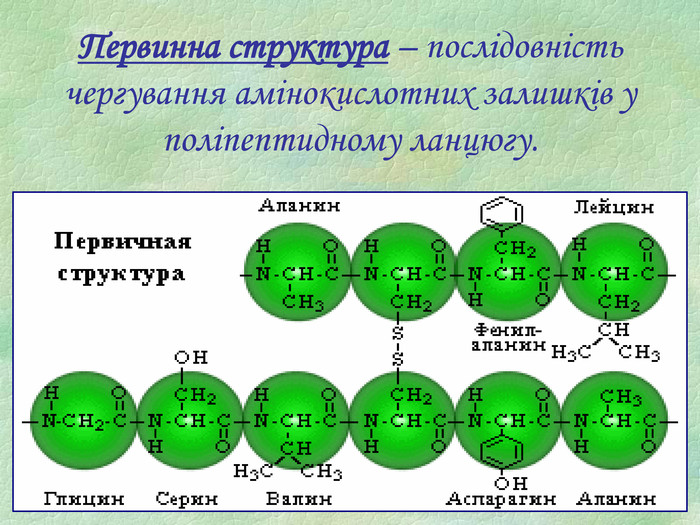
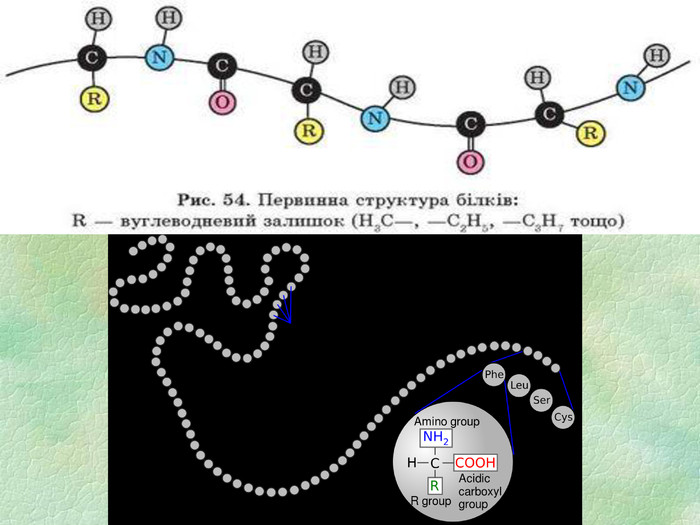
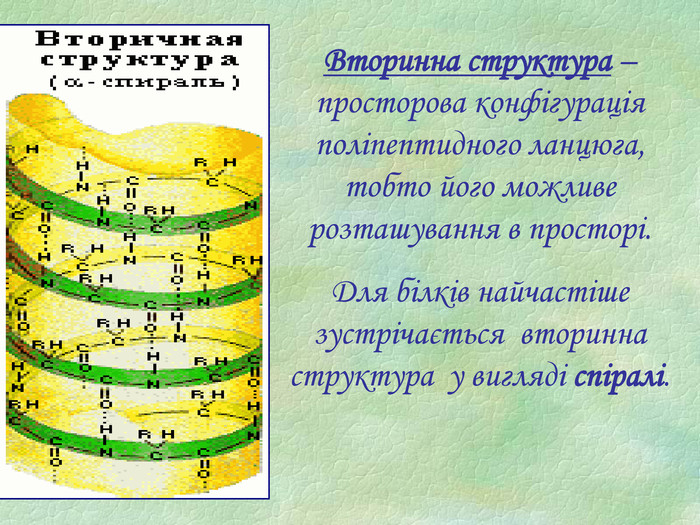
Білки, як біологічні полімери.


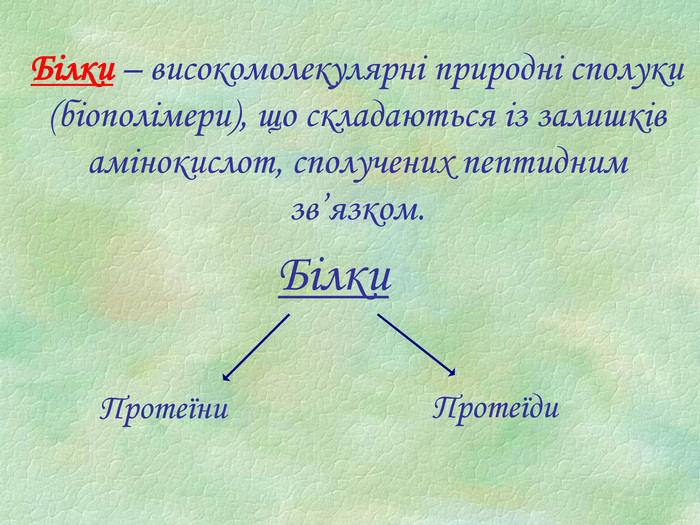
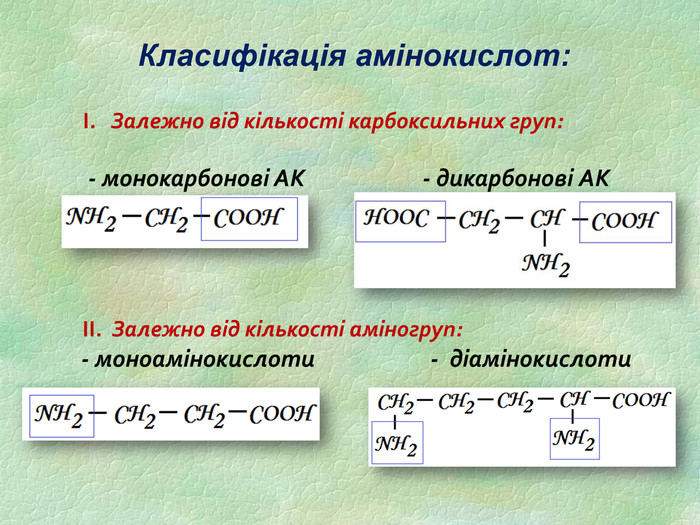
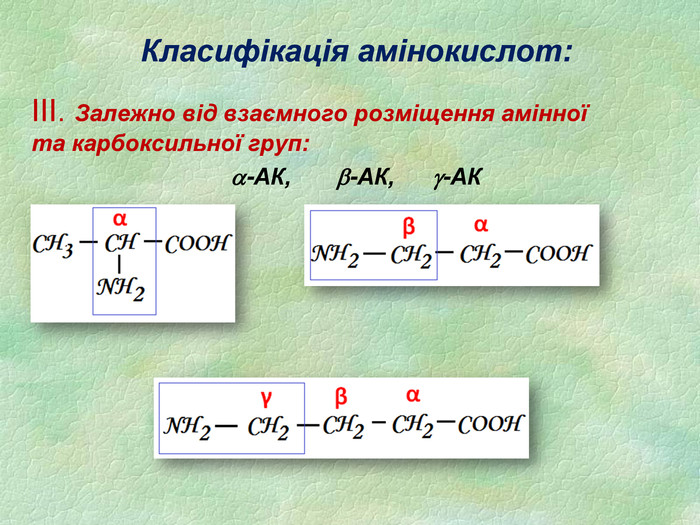




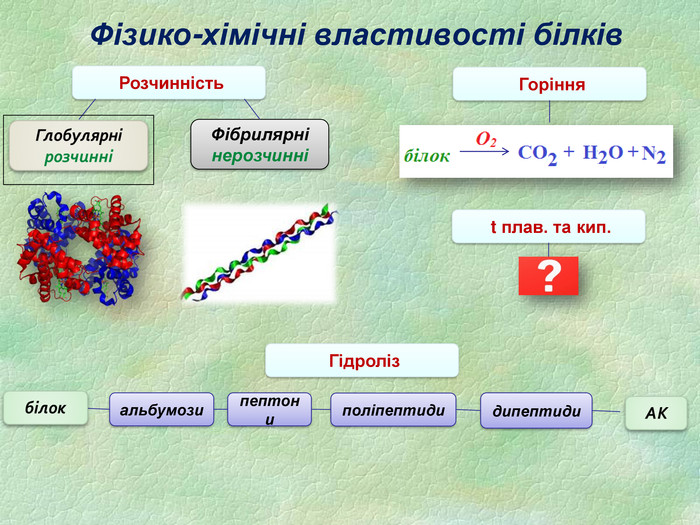








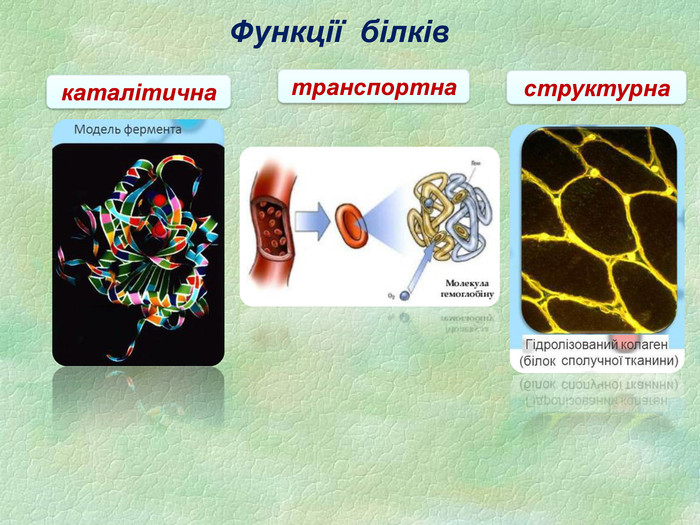
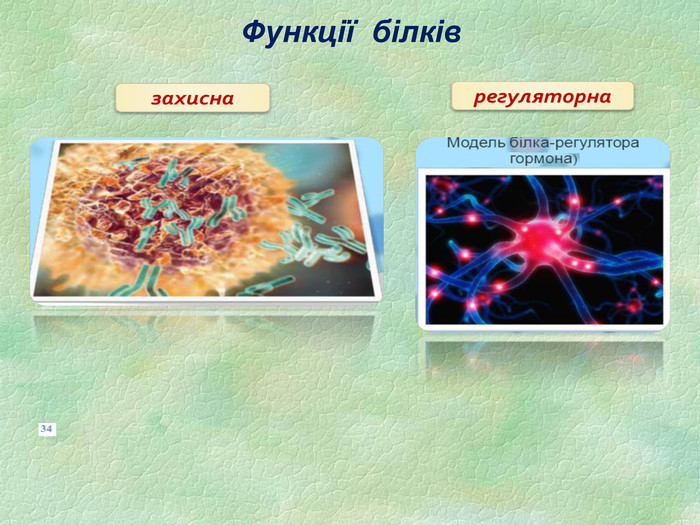





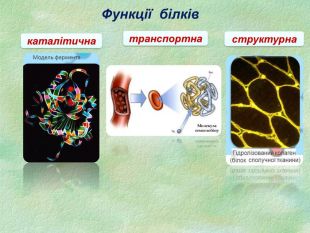
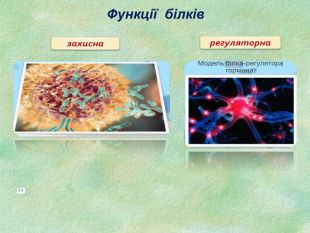
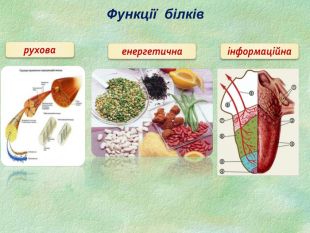
Функції білків Будівельна (пластична) – білки приймають участь в утворенні оболонки клітини, органоїдів і мембран клітини. Каталітична – всі клітинні каталізатори – білки (активні центри фермента). Рухова – скорочувальні білки викликають різноманітний рух. Транспортна – білок крові гемоглобін приєднує кисень і разносить його до всіх тканин. Захисна – вироблення білкових тіл і антитіл для знешкодження чужорідних речовин. Енергетична – 1 г білка еквівалентний 17,6 кДж. Рецепторна – реакція на зовнішній подразник.
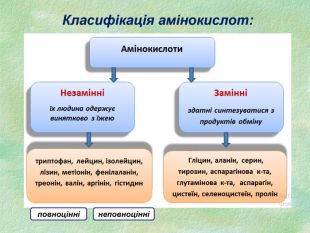
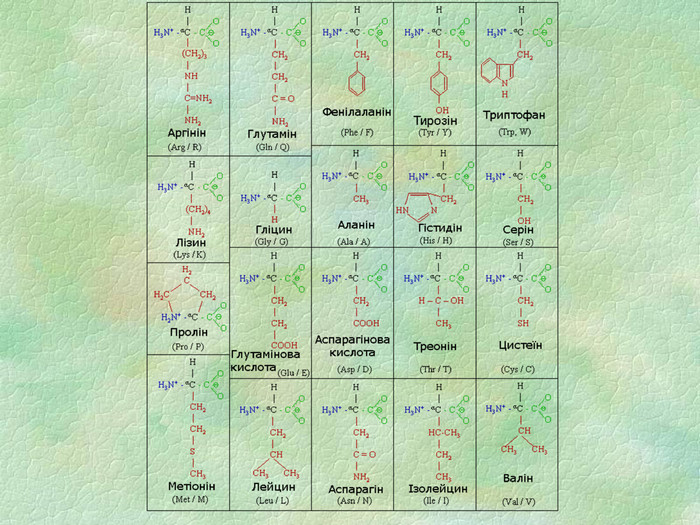
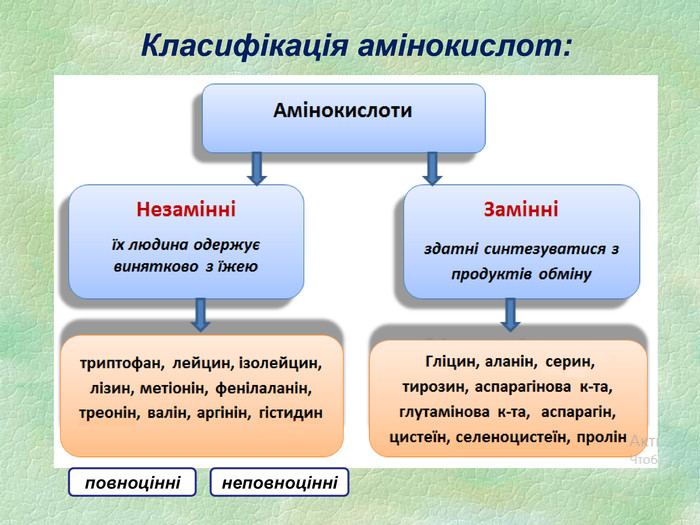
1) Які речовини входять до складу білків? а) амінокислоти; б) спирти; в) ефіри; г) кислоти 2) Скільки амінокислот беруть участь в утворенні білків? а) 16; б) 20; в) 30; г) 10 3) Які білки називаються неповноцінними? а) у яких відсутні деякі амінокислоти; б) у яких відсутні деякі незамінні амінокислоти; в) у яких відсутні деякі замінні амінокислоти. Питання для закріплення вивченого матеріалу:
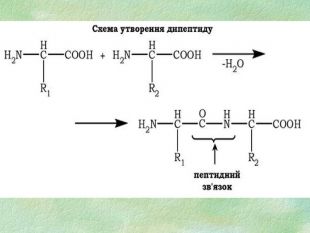
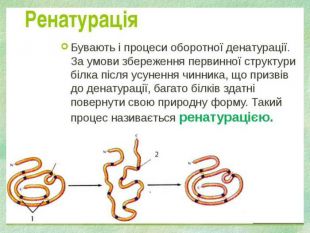
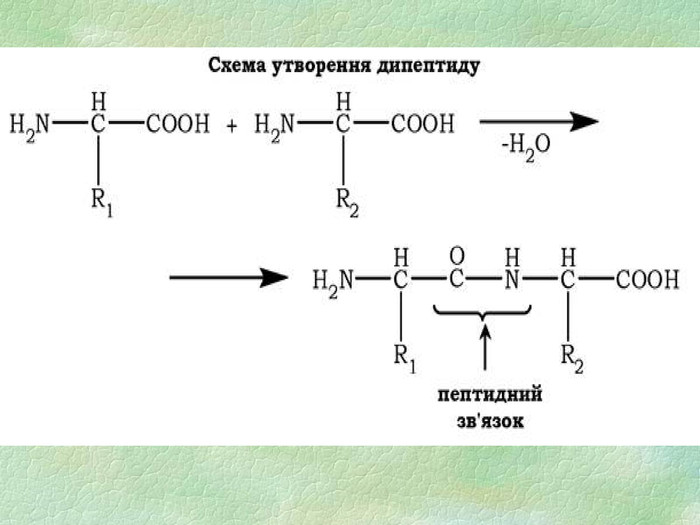
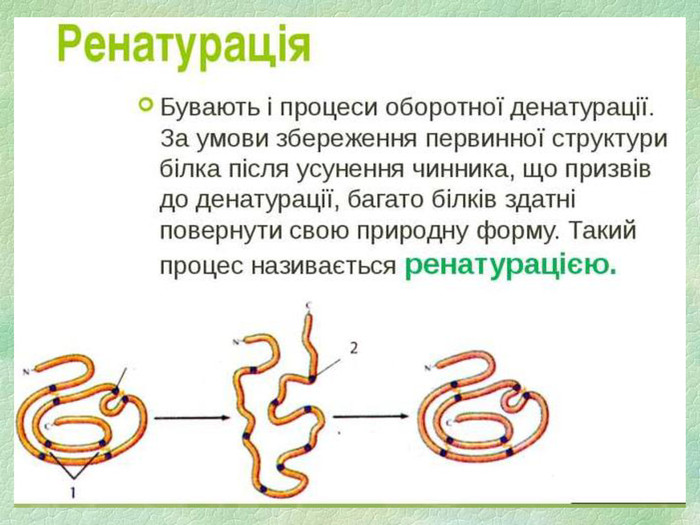
4. У результаті якої реакції утворюються білки? а) гідролізу; б) поліконденсації; в) гідратації; г) етерифікації. 5. Якого кольору утворюється осад при взаємодії білка з концентрованою нітратною кислотою: а) білий; б) жовтий; в) фіолетовий; г) блакитний. 6. Незворотній процес порушення первинної структури білків називається: а) ренатурацією; б) денатурацією; в) деструкцією.
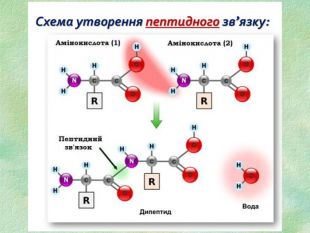
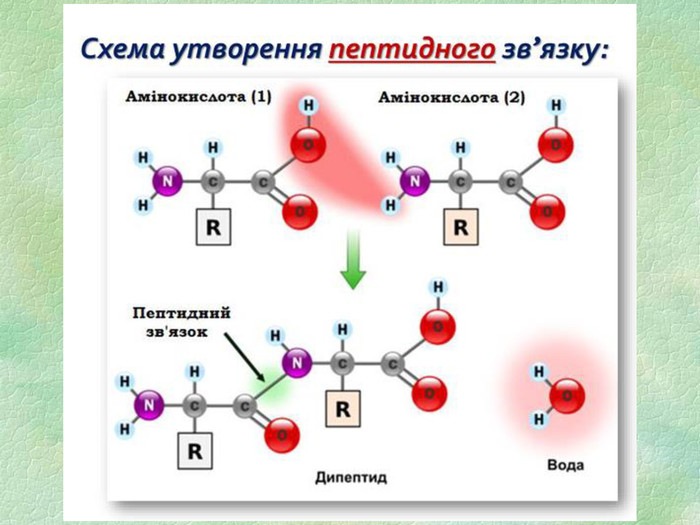
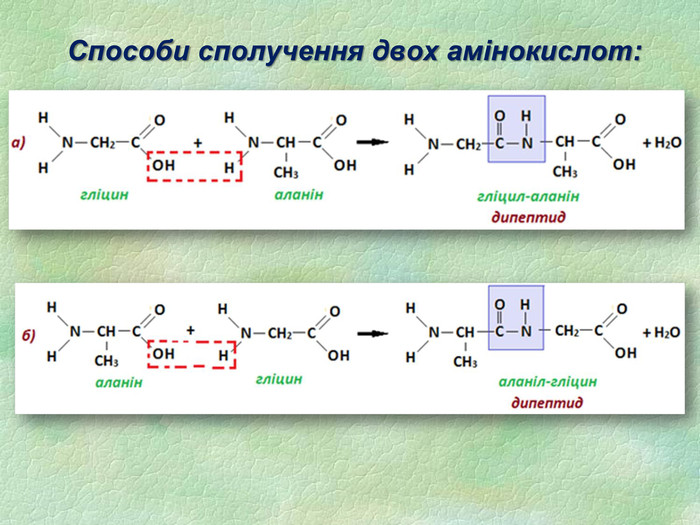
7. Пептидним називають зв’язок між: а) карбоксильною групою однієї амінокислоти і аміногрупою іншої б) карбоксильними групами двох амінокислот в) аміногрупами двох амінокислот 8. Амінокислоти, які синтезуються в організмі людини та тварин з інших сполук (з продуктів обміну речовин), називають: а) незамінними б) частково замінними в) замінними


про публікацію авторської розробки
Додати розробку