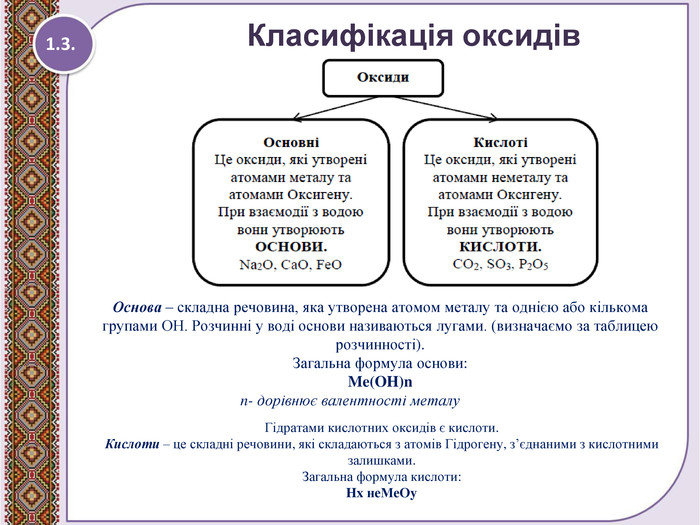
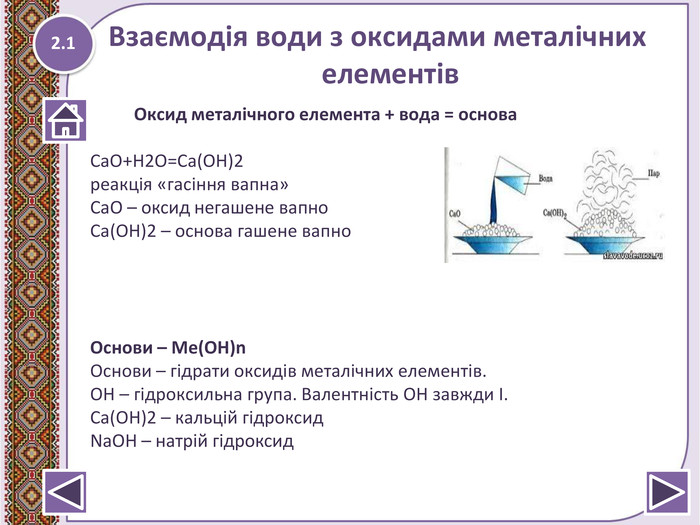
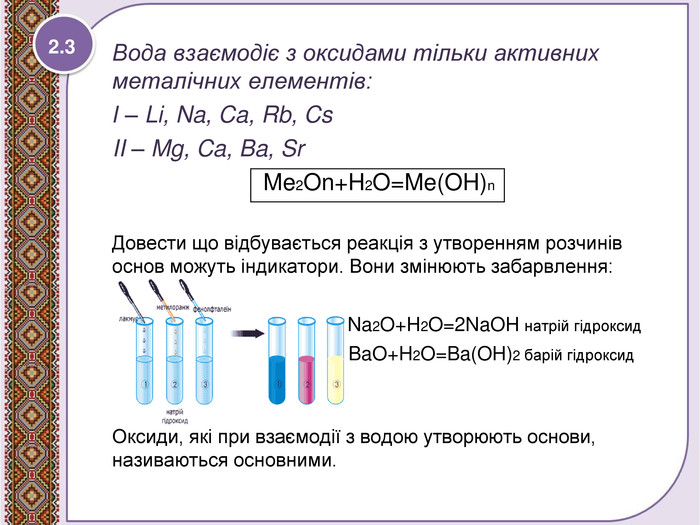
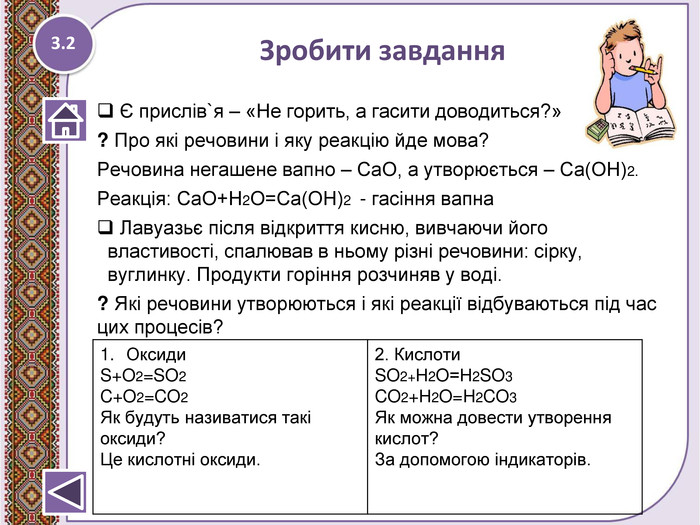
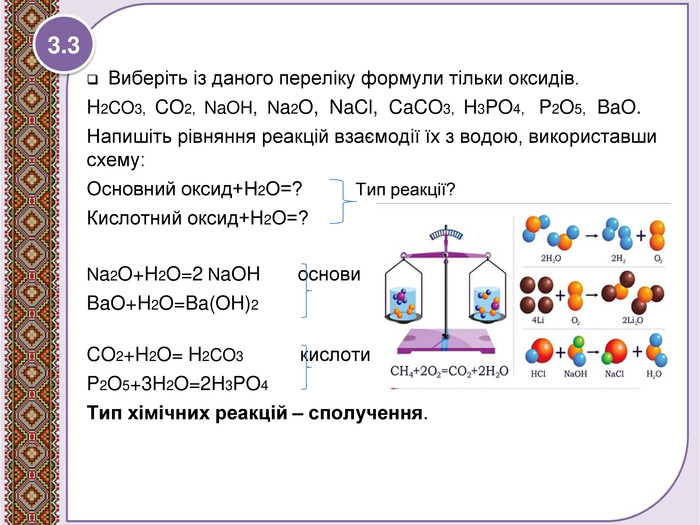
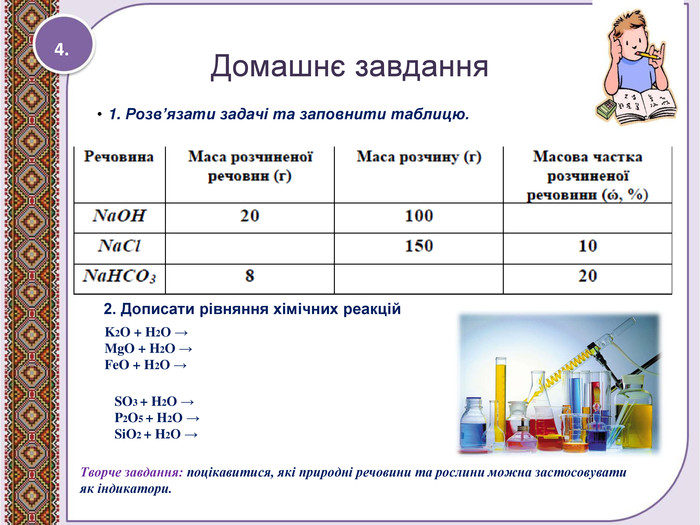
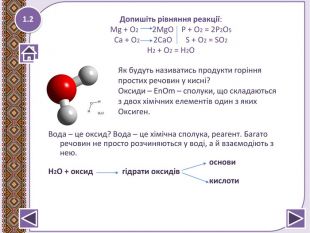
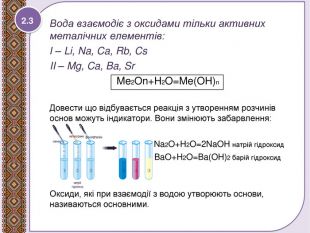
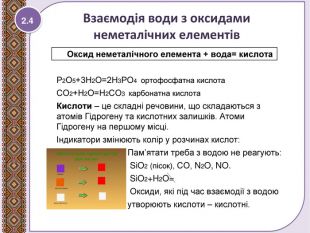
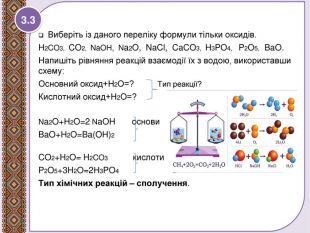
Взаємодія води з оксидами. Поняття про гідрати оксидів.
Про матеріал
Презентація до уроку 7 класу. Взаємодія води з оксидами. Поняття про гідрати оксидів - кислоти, основи. Рівняння реакцій утворення кислот та основ. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку