Презентація "ЕСТЕРИ, ЗАГАЛЬНА ТА СТРУКТУРНІ ФОРМУЛИ, СИСТЕМАТИЧНА НОМЕНКЛАТУРА, ФІЗИЧНІ ВЛАСТИВОСТІ. ГІДРОЛІЗ ЕСТЕРІВ"
Про матеріал
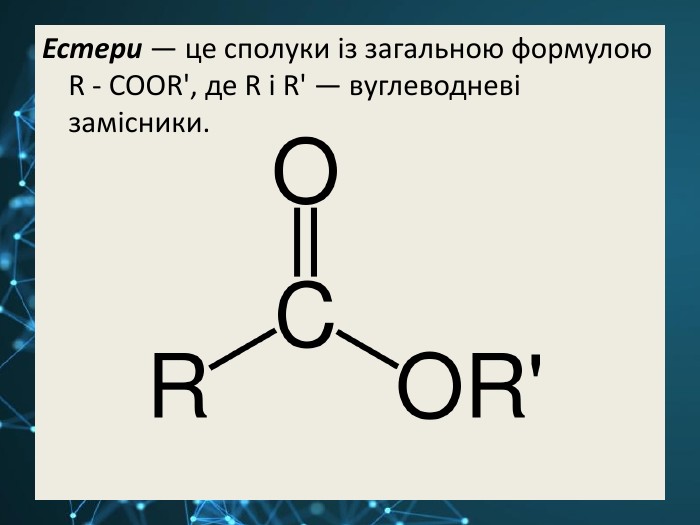
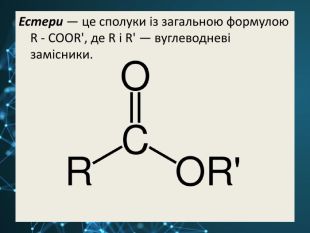
Презентація містить матеріал до уроку з теми "Естери".
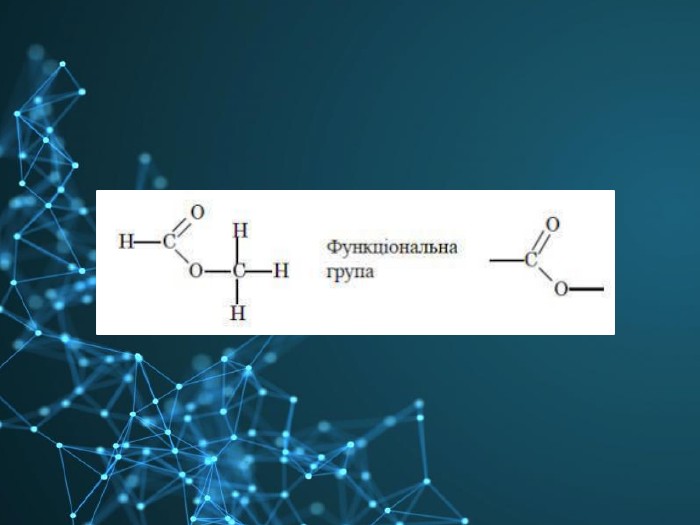
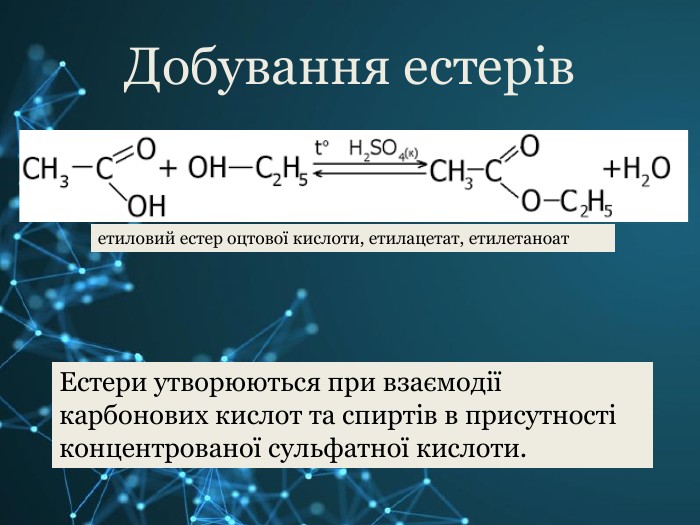
В ній розглянуто питання номенклатури, хімічних та фізичних властивостей, добування та використання естерів у промисловості.
Презентація також містить опитування на початку уроку та наприкінці.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку




















-

Фертак Наталя Володимирівна
22.02.2025 в 15:09
Дякую.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Грищенко Ирина
10.02.2025 в 19:55
дякую.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Malicki Viktor
11.03.2024 в 21:01
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Kornienko Liana
21.02.2024 в 00:59
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук