Обчислення об'ємних відношень газів за хімічними рівняннями
Про матеріал
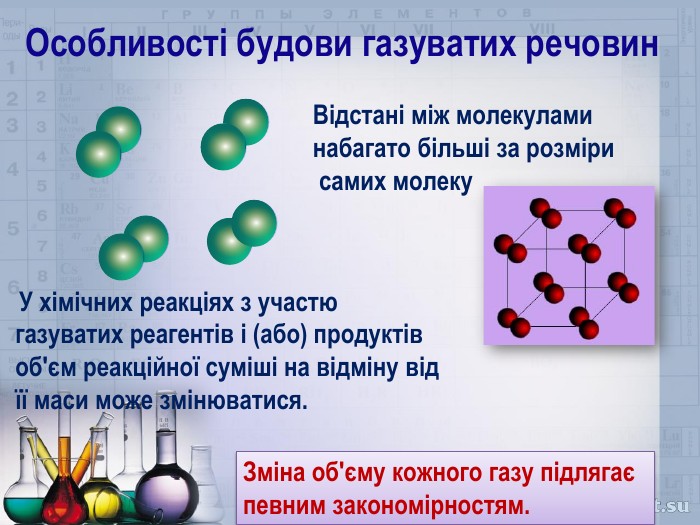
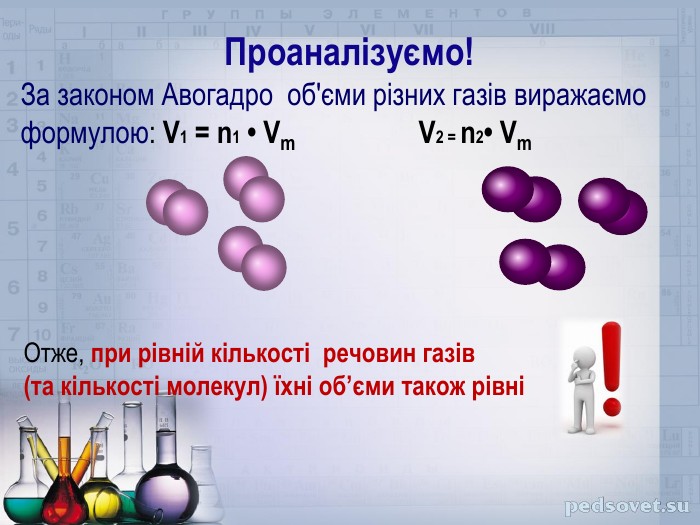
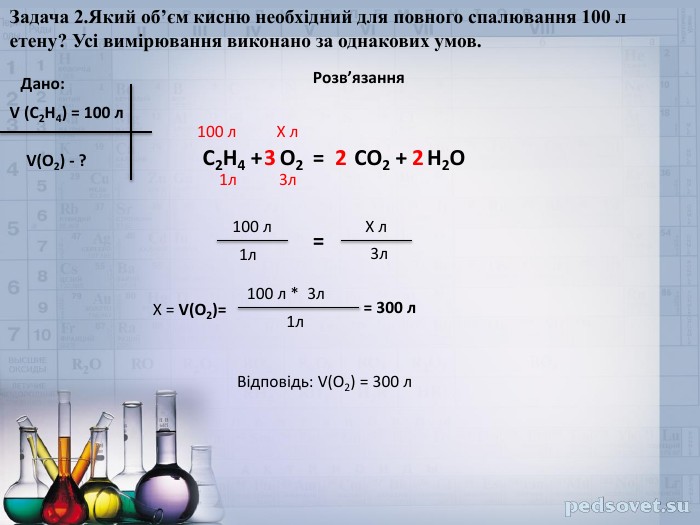
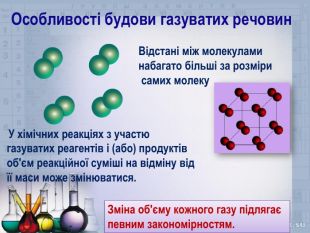
Розробка містить приклади розв'язування задач з теми "Об'ємні відношення газів" Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку