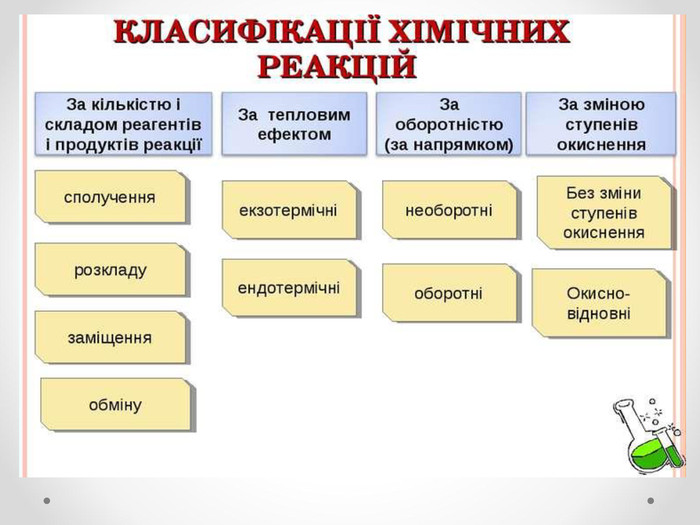
Хімічні реакції. Класифікація реакцій
Про матеріал
Довкола нас, в природі, в людському організмі, в організмах рослин і тварин, на виробництвах відбувається безліч хімічних реакцій.
Учням пропонується згадати все, що вони знають про хімічну реакцію з курсу хімії 7-8 класу;
1.Пригадайте:
1. Що таке хімічна реакція? (Процес, внаслідок якого з одних речовин утворюються інші за рахунок перегрупування атомів)
2. Які ознаки хімічних реакцій? (зміна забарвлення, виділення газу, виділення світла і тепла, випадання осаду, поява запаху).
3. Яким чином записується хімічна реакція? (за допомогою хімічного рівняння).
4. Що таке хімічне рівняння? (умовний запис хімічної реакції за допомогою хімічних формул та коефіцієнтів).
5. Що таке реагенти? продукти реакції? ( Реагенти- це речовини, які реагують між собою. Продукти реакції – речовини, які утворилися в результаті реакції.)
2.Пропоную вам зіграти в гру « Так чи ні » (сл №4)
Я називатиму вам різні явища, які відбуваються навколо нас, а ви визначте: відносяться вони до хімічних чи ні?
1. Жовтіння листя …….( так)
2. Утворення криги на річках ….( ні )
3. Подих людини …….( так )
4. Скисання молока ….( так )
5. Туман на дорозі …..( ні )
6. Ржавіння автомобіля ….(так)
7. Сніг на вулиці …………( ні )
Проаналізуємо, що об’єднує явища, які ми визначили як хімічні?
Чи правильне твердження : « хімічне явище – це хімічна реакція »?
Давайте згадаємо які ознаки хімічної реакції ви знаєте? ( газ, осад, вода, виділення тепла і світло, поява або зникнення запаху, зміна забарвлення , зміна смаку ).( на дошці малюємо сонечко , в якого промінчики це кожна ознака реакції)
Перегляд файлу
Зміст слайдів
ppt
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку