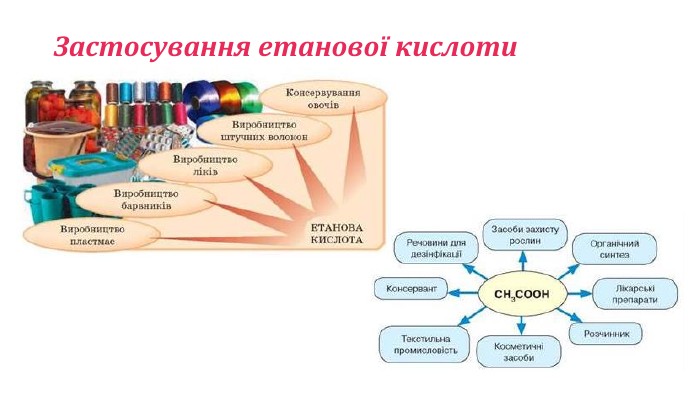
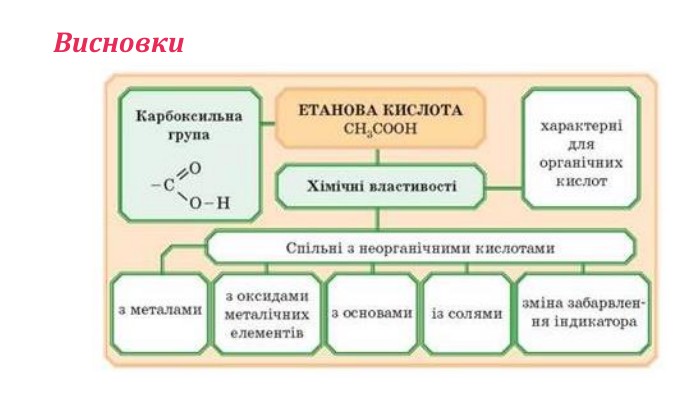
Хімічні властивості етанової (оцтової) кислоти, 9 клас
Про матеріал
Хімічні властивості етанової (оцтової) кислоти. Рівння реакція, відеодосліди. Застосування Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку