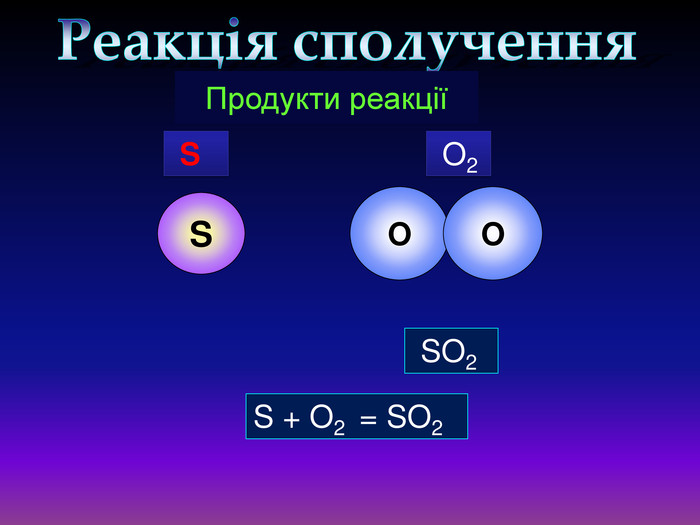
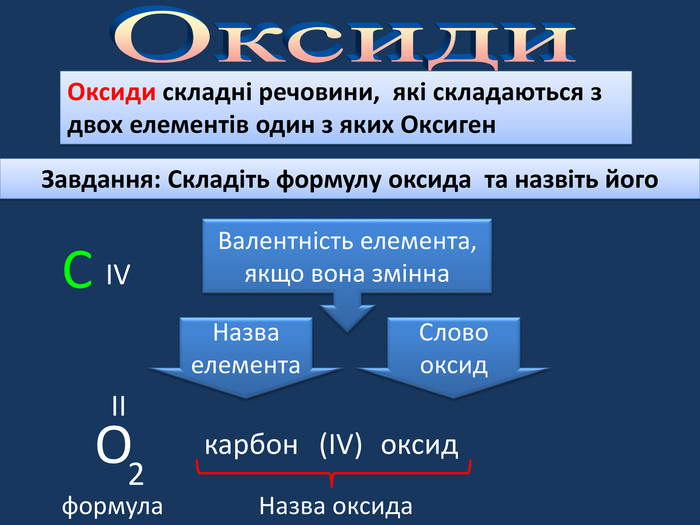
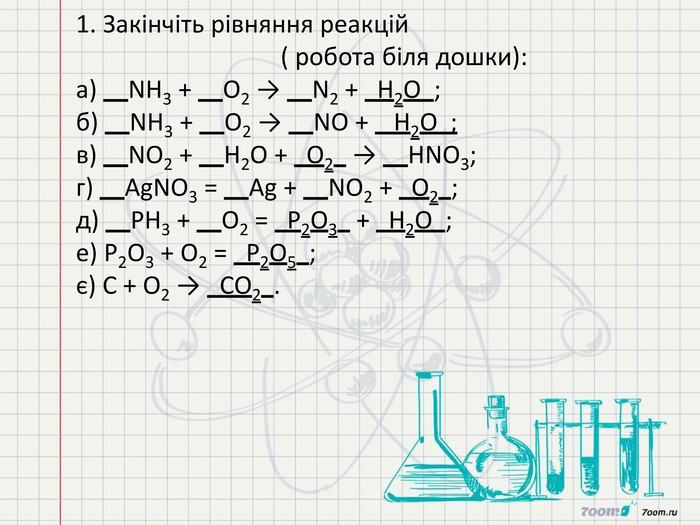
Хімічні властивості кисню: взаємодія з простими речовинами . Реакція сполучення.
Про матеріал
Презентаці до уроку на тему: ,,Хімічні властивості кисню:
взаємодія з простими речовинами. Реакція сполучення,,.
Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку