Карбонові кислоти. Мило.
КАРБОНОВІ КИСЛОТИ. МИЛО.
Очікувані результати навчально-пізнавальної діяльності учнів
з теми «Карбонові кислоти»
Учень/учениця
Знаннєвий компонент
знає і розуміє суть понять гомолог, гомологія; поділ органічних речовин за якісним складом на вуглеводні, оксигеновмісні та нітрогеновмісні сполуки;
називає елементи-органогени, найважливіші оксигеновісні органічні сполуки (метанол. етанол, гліцерол, етанова кислота, стеаринова, пальмітинова, олеїнова, аміноетанова кислоти);
наводить приклади карбонових кислот, мила;
пояснює реакції горіння органічних речовин, деякі хімічні властивості етанової кислоти, утворення мила.
Діяльнісний компонент
складає молекулярні й структурні формули; реакції взаємодії етанової кислоти (електролітична дисоціація, взаємодія з металами, лугами, солями); реакцію утворення рідкого та твердого мила.
розрізняє за складом етанову кислоту, вищі карбонові кислоти, мило ;
порівнює: органічні неорганічні кислоти, насичені і ненасичені вищі карбонові кислоти;
характеризує склад, фізичні властивості етанової кислоти;
визначає дослідним шляхом, етанову кислоту;
розв'язує розрахункові задачі на обчислення за хімічними рівняннями та інших типів раніше вивчених на прикладі органічних сполук;
дотримується правил безпечного поводження з горючими речовинами, побутовими хімікатами.
Ціннісний компонент
усвідомлює необхідність збереження довкілля для майбутніх поколінь;
обґрунтовує роль органічних сполук у живій природі;
оцінює вплив продуктів синтетичної хімії на навколишнє середовище в неправильного разі використання їх;
висловлює судження щодо значення органічних речовин у суспільному господарстві, побуті, харчуванні, охороні здоров'я тощо; захисту довкілля від органічних стійких забруднювачів.
РОБОТА З ОПОРНИМ КОНСПЕКТОМ
Зручно і доцільно при вивченні нової теми використовувати опорні конспекти . Даний дидактичний прийом полегшує і прискорює засвоєння нового матеріалу на уроці.
|
ОДНООСНОВНІ КАРБОНОВІ КИСЛОТИ |
|||
|
ЕТАНОВА ( ОЦТОВА) КИСЛОТА |
|||
|
Поелементний склад
|
Функціональна група |
Особливості утворення назви
|
|
|
Молекулярна форула
|
Повна структурна формула |
Скорочена структурна формула
|
|
|
ВИЩІ КАРБОНОВІ КИСЛОТИ |
|||
|
Пальмітинова
|
Стеаринова |
Олеїнова |
|
|
ХІМІЧНІ ВЛАСТИВОСТІ |
|||
|
|
||
|
Зміна кольору індикаторів |
Назва індикатора |
колір в кислоті |
|
|
лакмус |
|
||
|
універсальний індикаторний папір |
|
||
|
метиловий оранжевий |
|
||
|
фенолфталеїн |
|
||
|
|
||
|
|
||
|
|
||
|
|
||
( горіння) |
|
||
|
ЗАСТОСУВАННЯ ЕТАНОВОЇ КИСЛОТИ |
|||
|
Заповнити , працюючи за принципом « 2-4-разом» |
|||
|
|
|||
|
|
|
||
ВИКОРИСТАННЯ МЕТОДУ «ІНТЕЛЕКТ – КАРТА»
Для дітей, що позитивно сприймають он – лайн навчання, полюбляють використовувати комп’ютер та телефон для навчання, варто запропонувати створювати та використовувати «Інтелект – Карти»
Інтелект-карта, відома також як ментальна карта або асоціативна карта (з англійського «Mind map» - «карти розуму», «карти розуму», «інтелект-карти», «карти пам'яті »,« ментальні карти »,« асоціативні карти »,« діаграма зв'язків », «асоціативні діаграми» або «схеми мислення») - спосіб зображення процесу загального системного мислення за допомогою схем. Також може розглядатися як зручна техніка альтернативної запису. Метод використання інтелект-карт розроблений психологом Тоні Бьюзеном, який під час свого навчання шукав спосіб ефективного запам'ятовування і систематизування інформації. Тоні Бьюзен є фахівцем в області саморозвитку, розвитку пам'яті та мислення.
Зручним сервісом для створення даних карт є Coggle Coggle - безкоштовний сервіс, що дозволяє створювати красиві онлайн-карти. Тут можна створювати будь-яку кількість гілок, викривляти їх, змінювати кольори, і переміщати елементи. Ви можете поділитися картами в соцмережах, а також працювати над ними спільно з колегами. Можна вбудувати карту в сайт або блог, а також зберегти її у вигляді PNG або PDF-файлу. Є функція збереження історії всіх змін, що дозволяє Вам в будь-який момент повернутися до попередніх версій карти. Для використання Coggle потрібен обліковий запис в Gmail. Хороший варіант для навчальних закладів, де вже активно використовуються інструменти Google.
АЖУРНА ПИЛКА
За даним методом доцільно вивчати теми «Застосування етанової кислоти» , «Поширення карбонових кислот в природі»
- Поширення арбонових кислот в природі;
- Застосування етанової кислоти в побуті ;
- Застосування етанової кислоти в народноу господарстві.
Метод дозволяє учням працювати разом, щоби вивчити значну кількість інформації за короткий час, а також заохочує їх допомагати один одному вчитися, навчаючи.
Спершу кожен учень працюватимете в «домашній» групі. Завданням для кожного учня у домашній групі є аналіз та засвоєння певної порції інформації на такому рівні, щоб він був здатний чітко і зрозуміло викласти її з метою навчання інших учнів.
Потім в іншій групі, яка називається експертною, такі учні виступатимуть в ролі «експертів» із питання, над яким вони працювали в домашній групі, вчитимуть цій інформації інших та відповідатимуть на їхні питання. В експертній групі учні також повинні отримати інформацію від представників інших груп. Завдання експертної групи – здійснити обмін інформацією.
В останній частині уроку учні знову повертаються до своєї «домашньої» групи, щоби поділитися тією новою інформацією, яку їм надали учасники інших груп. Їхнім завданням тепер буде знов обмінятись інформацією, узагальнити її та виробити спільні рішення разом з учасниками «домашньої» групи.
Порядок роботи в «домашніх» групах:
- В кожній групі обирається головуючий, спостерігач (тайм-кіпер) і той, хто ставить запитання, щоб переконатися, що кожний розуміє зміст матеріалу;
- Кожна група отримує завдання, вивчає його та обговорює свій матеріал.
Порядок роботи в «експертних» групах:
- Після об’єднання у нові групи, кожен учень стає «експертом» з тієї теми, що вивчалась у його «домашній» групі.
- По черзі та за визначений час кожний має якісно і в повному обсязі донести інформацію учням з інших груп і сприйняти нову інформацію від кожного з них.
Під час повернення до «домашніх» груп:
- Учні мають поділитися інформацією з членами своєї «домашньої» групи про нову інформацію, яку вони отримали від представників інших груп, узагальнюють її.
- Учні виробляють спільні висновки та рішення.
Таким чином, за допомогою методу «Ажурна пилка» за короткий відрізок часу можна надати і опрацювати велику кількість інформації.
ДІЛОВА ГРА: «ЕТАНОВА КИСЛОТА – ТАКИЙ ЗНАЙОМИЙ ОЦЕТ»
Учні працюють в групах – лабораторіях, по 4 – 6 учнів і кожна група досліджує власну тему :
- Лабораторія «Хімічна промисловість» ( виробництво барвників, застосування оцтової кислоти як розчинника, виробництво ацетатного волокна)
- Лабораторія «Агрохімічна» ( виробництво засобів захисту рослин)
- Лабораторія «Харчова промисловість» ( застосування оцтової кислоти в харчовій промисловості)
- Лабораторія «Хозяюшка» (застосування оцтової кислоти в побуті)
- Лабораторія «Фармацевт» ( виробництво лікувальних засобів, застосування оцтової кислоти в медицині)
Результатом роботи є презентація кожної з груп. Вчитель зазделегіть готує пакет інформаційних матеріалів, в тій її частині, де учням важо самотужки знайти інформацію.
ГРА «ЗНАЙДИ ГОСПОДАРЯ».
Учня роздаються картки з назвамими карбонових кислот, що містяться у природніх об’єктах та власне картки з овочами, фруктами та рослинами, де вони містяться. Ціллю є засвоїти поширення карбонових кислот у природі.
|
яблучна кислота
HOOC-CH(ОН)- -CH2-COOH |
|
|
|
|
|
|
|
|
лимонна кислота HOOC-CH2-C(OH)COOH-CH2-COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мурашина кислота
НСООН |
|
|
|
|
|
|
щавелева кислота
HOOC-COOH |
|
|
|
|
|
|
|
|
|
|
|
|
молочна кислота CH3-CH(OH)-COOH |
|
|
|
|
|
|
|
|
винна кислота
НООС-СН(ОН)-СН(ОН)-СООН |
|
|
|
|
ПРИЙОМ «ДІАГРАМА ВЕНА»

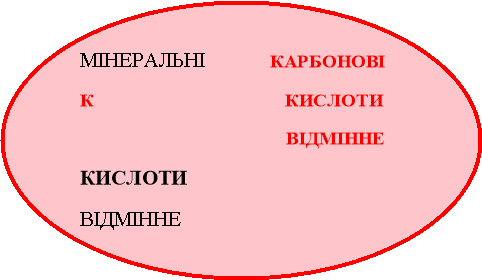
 Доцільно застосувати для порівняння властивостей мінеральних і карбонових кислот.
Доцільно застосувати для порівняння властивостей мінеральних і карбонових кислот.
ІНТЕРАКТИВНИЙ МЕТОД «КАРУСЕЛЬ»
Учні за урок уже декілька разів звертали увагу на формули кислот. Використовуючи записи на дошці (формули і назви кислот), вони повинні знайти відповідність між картками, які роздає вчитель. Учні розміщують стільці у два кола так, щоб один учень сидів навпроти іншого. Рухається зовнішнє коло. Одні учні (внутрішнє коло) отримують картки з формулами кислот, інші — тільки з назвами кислот (зовнішнє коло). Кожна пара учнів, спілкуючись між собою, повинні знайти відповідність між формулою і назвою, при цьому кожна пара повинна оформити тільки одну кислоту.
Додатковим завданням є обчислити масові частки елементів у кислотах.
Дану вправо доцільно використовувати для учнів, що мають не високий рівень навчальних досягнень.
КОМПЕТЕНТІСНІ ЗАДАЧІ.
Цікавим і мотивуючим фактором на уроці є використання компетентісних задач і завдань.
Задача № 1
Оцтова кислота відома людству з прадавніх часів. Оцет, 4—12% розчин оцтової кислоти у воді, як продукт ферментації вина набув широкого використування більш ніж 5000 років тому, перш за все як харчовий консервант.
Давньогрецький лікар Гіппократ використовував розчини кислоти як антисептик, а також у складі настійок від численних захворювань, включаючи лихоманку, запори, шлункові виразки, плеврит.
- Обчисліть масу чистої етанової кислоти, що іститься в 1 л столового 9% розчину оцту, якщо густина 1,0446 г/см³
- Обчисліть масу 9 % оцту, що потрібен для приготування 100 г 6 % розчину.
Задача № 2
У продаж надходять оцтова есенція - водний розчин з масовою часткою кислоти 80% і столовий оцет – водний розчин з масовою часткою оцтової кислоти 9%. Їх широко використовують у харчовій промисловості і домашньому побуті, як приправу до їжі і для консервування харчових продуктів (виготовлення маринадів). Обчисліть масу оцтової кислоти і води в оцтовій кислоті і столовому оцті масою 250г.
Задача № 3
Звичайно, що з часом певні металеві предмети починають іржавіти. Регулярне використання, вплив вологи та відсутність догляду може поступово призвести до їх погіршення і скоротити термін служби. Цвіль й іржа, як правило – результат процесу окислення, який відбувається із залізом, коли воно вступає в контакт із водою. Це може завдати значних збитків цьому об’єкту і може навіть викликати алергічні реакції у деяких людей. На щастя, немає ніякої необхідності викидати речі, тому що є деякі хитрощі, які допоможуть вам видалити цю речовину та змусити їх виглядати по-новому.
Кислота в оцті можуть ефективно видалити іржу, яка накопичується на предметах, виготовлених із заліза. Як ви можете його використати?
Налийте достатню кількість оцту в миску, щоб повністю покрити предмет, який ви хочете очистити. Дайте йому мокнути цілу ніч, а наступного дня протріть його за допомогою щітки або жорсткої губки.
Обчисліть, яка маса ферум (ІІІ) гідроксиду може бути видалена з поверхні металу оцтовою кислотою масою 600 г з масовою часткою етанової кислоти 9%.
Задача № 4
Однозначної відповіді на питання, хто подарував цей незамінний продукт людству, не існує. Важко навіть вказати частину світу, звідки мило початок свою переможну ходу. Багато істориків, втім, називають «колискою чистоти” Середземномор'ї, де в достатку було природної соди, тварин і рослинних жирів, необхідних при виробництві мила.
Дослідивши дельту Нілу, єгипетські археологи виявили, що в цих місцях мило варили ще 6000 років тому. Правда, найдавніший документ «Папірус Еберса”, в якому є рецепт приготування мила, датується 1500 роком до н.е.Просвещенние римляни з претензією на лідерство в цьому питанні залишили після себе легенду, згідно якої, sаро (мило) було названо в честь однойменної гори.
Обчисліть масу мила, що можливо отримати взаємодією стеаринової кислоти з натрій гідроксидом масою 12г.
ЦІКАВІ ФАКТИ ПРО ОЦТОВУ ( ЕТАНОВУ) КИСЛОТУ
Цікаво знати. Оцтова кислота Оцтова кислота в історії людинию Оцтова кислота — перша кислота, отримана і використана людиною. «Народилася» понад 4 тис. років тому в Давньому Єгипті. Вперше отримали при скисанні вина. Процес виготовлення вина не змінюється вже багато століть: після збору врожаю виноград розминають і з цієї маси шляхом віджиму отримують сік. Сік повинен бродити в щільно закупорених посудинах. Якщо ж вино довго стоїть відкритим або погано закупореним, то замість вина утворюється оцтова кислота.
У Стародавньому Римі дію оцтової кислоти на свинець використовували для виготовлення солодкого густого напою. Скисле вино наливали у свинцеві горнятка й витримували певний час. Римські аристократи істотно вкорочували собі життя, ласуючи цим трунком. Адже солодкого смаку йому надавав так званий свинцевий цукор — отруйний плюмбум(ІІ) ацетат, який утворювався внаслідок реакції.
Концентровану оцтову кислоту у 1537 р. вперше добув німецький учений Теофраст Парацельс. 1864 р. участь бактерій у перетворенні спирту на оцет довів Луї Пастер. Латинська назва — Асеі;ит асісіит, звідси назва солей — ацетат.
Назва «оцтова кислота» — тривіальне, яке історично склалося; за сучасною номенклатурою — етанова кислота. У вигляді 5-15%- ного розчину оцтова кислота добре відома як оцет. Оцет отримують при розведенні водою оцтової есенції — 80%-го розчину оцтової кислоти. У свою чергу оцтову есенцію отримують перегонкою продуктів оцтового бродіння.
Фізичні властивості оцтової кислоти повною мірою науковці змогли дослідити лише після того, як виокремили цю речовину з її водного розчину. Оцтова кислота — безбарвна прозора гігроскопічна рідина з характерним кислим смаком і різким запахом. Вона необмежено розчиняється у воді, між її молекулами й молекулами води утворюються водневі зв'язки. Оцтова кислота змішується з багатьма розчинниками, у ній розчиняється чимало органічних речовин. Між молекулами оцтової кислоти утворюються водневі зв'язки. Плавиться при 16,75°С, кипить при 117,9°С за нормального тиску. Замерзла вона нагадує лід, тому її кристали називають льодяною оцтовою кислотою.
Застосування оцтової кислоти Розчин етанової кислоти використовують як смакову приправу та консервант продуктів харчування. Консервувальна дія полягає у тому, що кисле середовище пригнічує розвиток гнильних бактерій та пліснявих грибів. Досвідчені господині додають оцет до страв зі столового буряка й червонокачанної капусти не лише для того, аби надати страві гостроти, а й задля привабливого червоного кольору. Видалення за допомогою оцту накипу зі стінок посуду ґрунтується на реакції оцтової кислоти з кальцій карбонатом. Найважливіші галузі її застосування — органічний синтез, кулінарія і харчова промисловість, медицина, побутові потреби (чищення, виведення плям, дезінфекція). Оцтова кислота — один з базових продуктів промислового органічного синтезу. Більш ніж 65% світового виробництва оцтової кислоти іде на виготовлення полімерів, похідних целюльози та вінілацетату. Полівінілацетат є основою багатьох ґрунтівних покрить та фарб. З ацетатної целюльози виготовляють ацетатне волокно. Як розчинник, безводна оцтова кислота добре розчиняє значну кількість як органічних, так і неорганічних речовин. Вона входить до складу хімічних засобів захисту рослин та лікарських препаратів. Продукти реакції оцтової кислоти зі спиртами — естери. Ці запашні речовини широко використовують як ароматизатори кондитерських виробів і косметичних препаратів.
ІНТЕРАКТИВНИЙ ПРИЙОМ «Я ЗНАЮ. Я ВМІЮ. »

Гарним мотиваційним моментом для учнів є зв’язок матеріалу, що вивчається на уроці з життям та хатніми справами.
Оцет, без сумніву, знайдеться на кожній кухні. А ось область його застосування набагато ширша, ніж кулінарія. Оцет допоможе вам:
1. Позбутися від бур'янів. Пролийте їх, розвівши 40-відсотковий оцет напів з водою.
2. Видалити плями поту з одягу. Перед пранням на 10 хв. змочіть пляму поту білим столовим оцтом, і вона зійде дуже легко.
3. Вилікувати ангіну. Розведіть у склянці теплої води 1 ст. л. яблучного оцту (6%) і прополощіть цим розчином горло.
4. Зробити волосся слухняним. Після миття обполіскуйте волосся розчином яблучного оцту (1/2 ст. Л 6% оцту на склянку води).
5. Зняти м'язовий біль. Після інтенсивних навантажень у м'язах накопичується молочна кислота, яка викликає біль. Зняти її допоможе 20-хвилинний оцтовий компрес (2-3 ст. Л. На склянку води). Він розчиняє "зайву" молочну кислоту в нашому організмі.
6. Відклеїти цінник. Злегка підігрійте білий оцет, змочіть у ньому губку і прикладіть до наклейки. Вона відклеїться, не залишивши липких слідів.
7. Зняти іржу. Дрібні заіржавілі предмети (болти, гайки, цвяхи тощо) прокип'ятіть з оцтом, а потім добре промийте водою, і вони засяють, як новенькі.
8. Прибрати затхлий запах. Протріть поверхні холодильника, шафи або харчового контейнера ганчіркою, змоченою в оцті.
9. Видалити накип. Прокип'ятіть воду з додаванням оцту в чайнику або додайте його у відсік для ополіскувача при пранні. Оцет відмінно знімає вапняні відкладення.
10. Виправити смак зіпсованої страви. Якщо ви переперчили суп, для нейтралізації прянощі додайте в каструлю 1 ч. л. яблучного оцту.
11. Зберегти колір одягу. Для цього додайте 0,5 склянки 6% оцту в барабан пральної машини при пранні.
12. Освіжити повітря. Магазинні освіжувачі повітря часто мають різкий запах, який змішується з іншими і утворює ще більш неприємний. Протріть розчином столового оцту поверхні в кімнаті, розприскайте його по кутах, і самі не помітите, як неприємний запах зникне.
13. Розчинити засохлу фарбу на кисті. Закип'ятіть трохи оцту в каструлі, опустіть в неї пензлик і злегка потріть по дну. Фарба зійде.
14. Позбутися мурашок. Розведіть 6% яблучний або виноградний оцет напів з водою і розпоширьте в місці, де з'явилися комахи. Оцет зітре сліди мурах, і за ними не потягнуться їх родичі.
15. Вгамувати гикавку. Змочіть в оцтовому розчині (1/2 ст. Ложки 6%-го оцту на 1 ст. Ложки води) шматочок цукру, швидко розкусіть і проковтніть.
16. Помити скло, пластик і хром. Розведіть оцет водою напів і протріть забруднені поверхні. Змішайте трохи оцту з содою, щоб відчистити до блиску нержавійку і хром.
17. Продовжити життя букета. Додавши 2 ст. л. 6%-го оцту на 1 л води у вазу, де стоять зрізані квіти, ви зможете милуватися ними набагато довше.
18. Вилікувати грибок на ногах. Раз на кілька днів протягом 15-20 хв. приймайте ванночку з оцту з водою (1:5).
19. Приготувати смачне м'ясо для шашлику. Стакан столового оцту на 2 склянки води плюс спеції - відмінний маринад, що гарантує соковите м'яке м'ясо.
20. Усунути засмічення. Допомога сантехніка може і не знадобитися, якщо висипати в стік 3/4 склянки соди і залити її 1/2 склянки оцтової есенції (90%). Через 30 хв. пролийте стік чайником окропу. Таким чином видаляються навіть стійкі засори.
ІНТЕРАКТИВНИЙ МЕТОД «ПЕРЕВЕРНУТИЙ КЛАС»
Перевернутий клас (англ. flipped classroom) — принцип навчання, за яким основне засвоєння нового матеріалу учнями відбувається вдома, а час аудиторної роботи виділяється на виконання завдань, вправ, проведення лабораторних і практичних досліджень, індивідуальні консультації вчителя тощо.
Дослідницький етап
Група 1
Завдання. Спрогнозувати і дослідити дію оцтової кислоти на індикатори. На підставі здобутих результатів зробіть висновок, чи можна оцтову кислоту вважати органічною кислотою.
Обладнання. Оцтова кислота, фенолфталеїн, метилоранж, лакмус, універсальний індикаторний папір.
Група 2
Завдання. Спрогнозувати і дослідити дію оцтової кислоти на метали. На підставі здобутих результатів зробіть висновок, про спільні і відмінні властивості оцтової кислоти і неорганічних кислот.
Обладнання. Оцтова кислота, магній.
Група 3
Завдання. Спрогнозувати і дослідити дію оцтової кислоти на основи. На підставі здобутих результатів зробіть висновок, про спільні і відмінні властивості оцтової кислоти і неорганічних кислот.
Обладнання. Оцтова кислота, натрій гідроксид, фенолфталеїн.
Група 4
Завдання. Спрогнозувати і дослідити дію оцтової кислоти на солі. На підставі здобутих результатів зробіть висновок, про спільні і відмінні властивості оцтової кислоти і неорганічних кислот.
Обладнання. Оцтова кислота, натрій гідрокарбонат.
Оціночно-рефлексійний етап
Презентація результатів дослідження груп.
(Запис рівнянь реакцій, показ результатів досліджень)
В процесі презентацій роблять висновки про спільність властивостей етанової кислоти і мінеральних кислот. Визначають разом, який метод дослідження більш раціональний і продуктивний.
ВИКОРИСТАННЯ ДОМАШНЬОГО (УЖИТКОВОГО) ЕКСПЕРИМЕНТУ
Дослід 1. Видалення іржі з поверхні металу за допомогою оцтової кислоти
Мета: навчитися усувати іржу, використовуючи підручні засоби.
Хід дослідження: Для видалення іржі з поверхонь, тканин можна використати такі підручні засоби, як лимонна, щавелева або оцтова кислота. Соком лимона натріть поверхню, і через деякий час іржа легко видалиться з поверхні. Для очищення слідів іржі з емалі, використовують розчин ортофосфатної кислоти (емаль боїться сильних кислот). Для усунення сильних забруднень раковин, умивальників, ванн, використайте засіб для очищення поверхонь. Витримайте його кілька хвилин. Обробіть щіткою та ретельно змийте великою кількістю води. Пам'ятайте, що до складу мийного засобу входить хлоридна кислота, користуйтеся рукавичками!
Висновок: Для усунення слідів іржі з поверхонь, використовуємо розчини кислот, так як іржа містить ферум (ІІІ) гідроксид – Fe(OH)3.
Проблемне питання: Чи впорається з іржею оцет та кока – кола, якщо до її складу входить невелика кількість ортофосфатної кислоти?
Дослід 2. Видалення накипу з чайнику за допомогою оцтової кислоти
Мета: навчитися усувати накип з поверхні побутових приладів.
Хід дослідження: Готуємо розчин для усунення накипу: беремо склянку води, засихаємо півсклянки оцтової кислоти. Приготовлений розчин вливаємо в чайник. Кипятимо на повільному вогні. Через 20 – 30 хвилин виливаємо вміст чайника у банку для зливів і промиваємо чайник кілька разів чистою водою. Якщо накипу багато, повторюємо процедуру.
Висновок: Накип на поверхні побутових приладів – це нерозчинні солі Кальцію та Магнію. Під дією кислоти вони розчиняються.
Додаткове завдання: Використайте лимонну кислоту для усунення накипу з поверхні побутового приладу.
Проблемне питання: Чому накип не утворюється на каструлі під час приготування борщу?


про публікацію авторської розробки
Додати розробку