Конспект уроку на тему: Кислоти: класифікація та номенклатура. Фізичні властивості й поширення в природі.
Тема уроку: Кислоти: класифікація та номенклатура. Фізичні властивості й поширення в природі.
Мета уроку:
освітня: розширити і закріпити знання про класифікацію неорганічних кислот; ознайомити учнів із класифікацією кислот та номенклатурою; розглянути фізичні властивості; ознайомити з поширеністю кислот у природі та їх використанням, розвивати вміння логічно та критично мислити, творчо використовувати отриману інформацію, порівнювати та систематизувати;
розвиваюча: розвивати увагу, вміння логічно та критично мислити, творчо використовувати отриману інформацію, порівнювати та систематизувати;
виховна: виховувати самостійність, почуття відповідальності за свої вчинки, бережне ставлення до здоров'я.
Обладнання: комп’ютер, презентація, Періодична система хімічних елементів Д.І.Менделєєва, таблиця «Основні класи неорганічних сполук»
Базові поняття й терміни: кислота, кислотний залишок, одноосновна кислота, двоосновна кислота, триосновна кислота, оксигеновмісна кислота, безоксигеновмісна кислота.
Тип уроку: урок засвоєння нових знань.
Форма уроку: фронтальна, ідивідуальна.
Ключові компетентності: вільне володіння українською мовою; саморозвиток і самоосвіта – створення проблемних ситуацій; інформаційна – розуміння та усвідомлення отриманої інформації, вміння робити висновки й узагальнення, складання опорних схем.
ХІД УРОКУ
І. Організаційний момент (слайд 1)
Привітання вчителя. Перевірка усіх присутніх учнів та їхня готовність до уроку (1-2хв).
ІІ. Актуалізація опорних знань учнів (слайд 2)

(фото із презентації)
ІІІ. Мотивація навчальної діяльності
Сьогодні ми вивчатимемо ще один клас неорганічних сполук, а який саме, я вам пропоную розгадати за допомогою ребусу (демонстація слайду 3)

Перший малюнок – кит. Останню літеру забираємо, залишається «ки». Другий малюнок – масло. Із цього слова забираємо «ма», а залишається «сло». Третій малюнок – переклад із англійського слова «you» - «ти».
Отож, виходить слово «Кислоти». ІV. Оголошення теми і мети уроку (демонстрація слайду 4). Учні записують тему в зошит.
- Вивчення нового матеріалу (демонстація слайду 5)
Кислоти – це складні речовини, до складу яких входять атоми Гідрогену й кислотний залишок.
Кислота утвориться тоді, коли до складної речовин приєднати кислотний залишок та атом (атоми) гідрогену. Опорна схема:
Складна речовина + Атом (атоми) Гідрогену + Кислотний залишок = Кислота
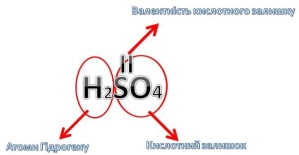 Важливо: Валентність кислотного залишку дорівнює числу атомів Гідрогену в молекулі кислоти.
Важливо: Валентність кислотного залишку дорівнює числу атомів Гідрогену в молекулі кислоти.
Запитання учням: чому? (бо валентність Гідрогену завжди дорівнює І)
Завдання: назвати зображену кислоту. Це сульфатна кислота.
Переглядаємо підручник на сторінці 120 (таблиця усіх кислот). Наголошення, що учням обов’язково потрібно її самостійно вдома опрацювати.
Класифікація кислот. Учні записують у зошит (слайд 6)
Кислоти класифікують:
- за числом атомів Гідрогену
- одноосновні (HBr, HCl)
- двоосновні (H2S, H2CО3)
- триосновні (H3РО4)
- за наявністю атомів Оксигену
- оксигеновмісні (H2CО3, HNО3)
- безоксигеновмісні (HBr, HCl, H2S)
(Демонстрація слайду 7). Дайте характеристику кислотам: назвіть їх, вкажіть валентність та кислотний залишок: Н2SO4 , НСl, НNО3.
Учні за бажанням коментують кожну кислоту.
Фізичні властивості кислот (слайд 8)
Більшість кислот при нормальних умовах (t=0°C) - це безбарвні рідини (сульфатна H2SO4, нітратна HNO3, хлоридна HCl), відомі також тверді кислоти (ортофосфатна H3PO4, метафосфосфатна HPO3, боратна H3BO3). Майже всі кислоти розчинні у воді. Практично нерозчинною є силікатна кислота.
Розчини кислот мають кислий смак: багатьом плодам надають кислий смак кислоти, що містяться в них. Звідси назви кислот: лимонна, яблучна і т.д.
Деякі кислоти є летючими і в концентрованому вигляді мають різкий запах (концентровані нітратна і хлоридна кислоти).
Поширення в природі (слайд 9)
Деякі продукти, скисаючи, також стають кислими, завдяки утворенню у них кислот. Наприклад, при скисанні молока утворюється молочна кислота. Утворюється вона і при скисанні капусти.

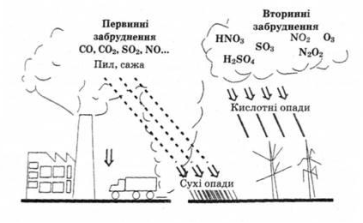 Слайд 10. Наприклад, дощова вода на перший погляд здається чистою. Насправді в ній є чимало інших речовин. За рахунок розчинення вуглекислого газу з атмосфери вона є розчином карбонатної кислоти. Після літньої грози в дощовій воді
Слайд 10. Наприклад, дощова вода на перший погляд здається чистою. Насправді в ній є чимало інших речовин. За рахунок розчинення вуглекислого газу з атмосфери вона є розчином карбонатної кислоти. Після літньої грози в дощовій воді
утворюється нітратна кислота, що поповнює запаси азоту в ґрунті. Виверження вулканів і згоряння палива сприяють появі в дощовій і сніговий воді сульфатної кислоти.
VІ. Узагальнення та систематизація знань.
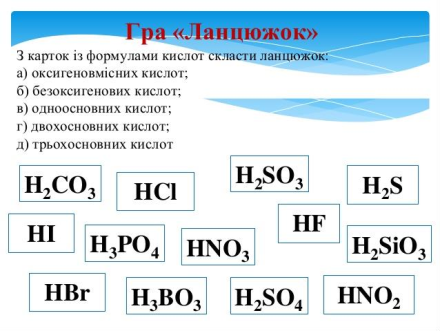
Завдання. Гра «Ланцюжок» (слайд 11)
Учні детально аналізують кожну кислоту, по порядку виписують в рядок кислоти по відповідних групах.
VІІ. Домашнє завдання (слайд 12)
- Опрацювати параграфи 20 (с.119-121), 25.
- Заповнити і вивчити таблицю (слайд 13)
|
Формула кислоти |
Назва кислоти |
Кислотний залишок |
Назва солі |
|
HCl
|
Хлоридна (соляна) |
Cl- |
Хлорид |
|
HBr |
|
Br- |
Бромід |
|
|
Йодидна
|
I- |
Йодид |
|
HF |
Фторидна
|
|
Фторид |
|
|
Сульфідна
|
S2- |
|
|
HNO3 |
Нітратна (азотна)
|
NO3- |
Нітрат |
|
H2CO3 |
(вугільна) |
|
Карбонат |
|
H2SiO3 |
Силікатна (кремнієва)
|
|
|
|
|
Сульфітна (сірчиста)
|
SO32- |
|
|
|
Сульфатна (сірчана ) |
|
Сульфат |
|
|
Ортофосфатна
(фосфорна) |
PO43- |
|
VІІІ. Підбиття підсумків уроку (слайд 14).
«Вільний мікрофон»: пропонується учням закінчити речення
- Сьогодні на уроці я дізнався (дізналась) про ...
- Сьогодні на уроці я вивчив (вивчила) …
- Мені сподобалось,


про публікацію авторської розробки
Додати розробку
