Конспект уроку з хімії на тему: "Вода у природі. Вода як розчинник. Фізичні та хімічні властивості води" для учнів 7-го класу
Конспект уроку з хімії на тему: "Вода у природі. Вода як розчинник. Фізичні та хімічні властивості води" для учнів 7-го класу це розробка яка містить в собі головну інформацію для ознайомлення. Доповнена ілюстраціями: "Агрегатні стани води" і "Водневий зв'язок".
Вода у природі. Вода як розчинник. Фізичні та хімічні властивості води.
Мета уроку:
Освітня: поглибити знання учнів про фізичні властивості води, її поширенні і значенні для живих організмів, познайомити учнів зі складом води і будовою її молекули; показати взаємозв'язок будови молекул води і фізичних властивостей.
Розвивальна: розвивати вміння учнів самостійно працювати з додатковою літературою, аналізувати, робити висновки.
Виховна: виховувати інтерес до навчання через роботу з додатковою літературою, демонстрування хімічних реакцій.
Тип уроку: вивчення нової теми..
Обладнання: малюнки "Агрегатні стани води", "Воднева зв'язок".
ХІД УРОКУ
I. Організаційний етап.
Вітання учнів. Перевірка готовності учнів і їхніх робочих місць до уроку.
ІІ. Актуалізація опорних знань.
Аналіз узагальнюючого уроку з теми: «Кисень».
Звернути увагу на:
1) Основні помилки.
2) Найкращі роботи.
3) Зробити декілька вправ.
ІIІ. Вивчення нової теми.
Учитель: Вода - найбільш популярна і найзагадковіша з усіх рідин, що існують на землі.
З давнього часу вищі уми людства задавали собі питання: у чому суть води, яке значення вона в людському житті? Перше наукове відкриття в даній області, яке до нас дійшло, називається «Вчення про чотири стихії».
Воно було написане в четвертому столітті до н. е. давньогрецьким філософом Аристотелем. До складу чотирьох стихій входять земля, вогонь, вода і повітря. Причому вода служить джерелом холоду та вологи. У наступний час вода все також приковувала до себе увагу кращих вчених умів свого часу. До вісімнадцятого століття н. е. ця речовина вважалося окремим хімічним елементом.
І лише поки вчений Франції Антуан Лавуазьє в 1783 року не повторив експерименти англійського вченого Кавендіша. Досліди полягали в роз'єднанні води за допомогою електричного струму. Лише француз зміг виявити те, що вода може розпадатися на водень і кисень. Тому він зробив висновок, що вода є окисом водню. Даний факт лягає в основу подальших дослідів води.
І дійсно спробуємо уявити собі, що вода раптово зникла з поверхні Землі. Як би виглядала наша планета?
Пересохлі русла річок, навіки замовк струмки, порожнечі морських і океанських западин, покриті товстим шаром солей, які коли - то були розчинні у воді.
Земля мертва - ні кущика, ні квіточки, жодної живої істоти ... Небо безхмарне, але незвичайного кольору від великої кількості пилу ... Жахлива картина!
Тисячі років людина захоплюється, милується, насолоджується водою. І весь цей час шукає відповіді на питання: Що таке вода? Чому вода має настільки дивовижні властивості? Скільки води на Землі?
Сьогодні на уроці ми спробуємо відповісти на ці питання.
Поширення води.
Вода - найпоширеніша на Землі речовина. Вона заповнює западини земної поверхні, утворюючи моря і океани. На їх частку припадає 95,7%. 2,14% води знаходиться в річках і озерах. Величезними масами снігу і льоду вона покриває полярні країни і вершини гір. 2,14% води укладено в гірських льодовиках і льодовиках Арктики і Антарктики. Хмари, туман - це теж вода, що міститься в атмосфері - 0,0005%.
Значення води для живих організмів.
Життя людини тісно пов'язана з водою і залежить від неї. Вода - обов'язковий компонент живої клітини. Кров людини складається на 30% з води, м'язи містять 75%, склоподібне тіло очі - 99%, кістки - 25%, зубна емаль і та містить воду - 0,2%. Сльози, слина, шлунковий сік - так само містять воду.
Вода бере участь у всіх процесах життєдіяльності: транспорт поживних речовин і кисню, виводить продукти розпаду, бере участь в диханні і терморегуляції - випаровуючись, вода сприяє охолодженню. Тому для забезпечення нормального існування людина щодня повинна споживати води в 2 рази більше, ніж поживних речовин: 2,5 - 6 л.
Втрата людиною води на 12 - 15% призводить до порушення обміну речовин, а втрата 25% води веде до загибелі організму. Без їжі людина може прожити 30-50 днів, а без води не більше 3-х днів. Вода також є середовищем існування для багатьох тварин і рослин.
Фізичні властивості води.
Чому вода так широко поширена на Землі і присутній повсюдно у вигляді рідини, твердого тіла або газу. Щоб відповісти на це питання згадаємо фізичні властивості води.
Чиста вода безбарвна, легко рухлива рідина без кольору, без смаку, без запаху. Щільність рідкої води (при температурі 4о С) = 1 г / см3.
Вода може перебувати в трьох агрегатних станах:

При 100о С і атмосферному тиску 101,3 кПа вода переходить у пароподібний стан. Саме в такому стані вона входить до складу повітря. При 0 С вода кристалізується і переходить в твердий стан - лід.
Вода володіє багатьма дивними властивостями. Її з повним правом можна назвати дивом природи. Глибокі моря, озера, річки не промерзають до дна, а лід знаходиться на поверхні води. Це явище можна пояснити тим, що при замерзанні вода розширюється, лід має меншу щільність і масу, ніж рідка вода, тому він плаває на поверхні. Завдяки цій властивості води у водоймах і взимку зберігається життя.
Вода має велику теплоємність - 42 Дж / г град - тому вона повільно нагрівається і повільно остигає, будучи хорошим теплоносієм. А водні басейни регулюють температуру на нашій планеті: влітку не дають їй перегріватися, а взимку постачають материки теплом. А від космічного холоду оберігають ті краплі води, які розсіяні в атмосфері.
Ще одна властивість - вода є універсальним розчинником. У ній розчиняються багато речовин.
Склад води.
Формула води - Н2О.
У молекулі води на один атом кисню доводитися два атоми водню.
Відносна молекулярна маса = 18.
Молярна маса = 18 г / Моль.
Будова молекули води.
Молекули води надзвичайно прості у своїй будові, але разом з тим надзвичайні. Завдяки силам міжмолекулярної тяжіння атом кисню однієї молекули води притягує атом водню іншої молекули води. Між сусідніми молекулами утворюється зв'язок, який називається водневым.
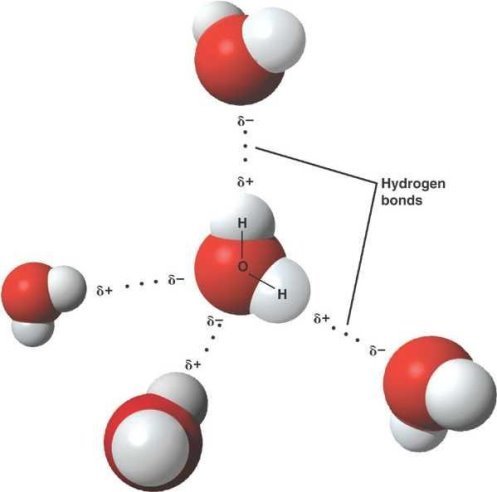
За рахунок водневого зв'язку утворюються групи таких молекул. Наявність водневих зв'язків обумовлює рідкий стан води. Коли вода закипає, воднева зв'язок між її молекулами руйнується, і вода з рідкого стану переходить в газоподібний. Щоб зруйнувати водневі зв'язки, необхідно докласти велику енергію, тому рідка вода має високу температуру кипіння. Зі зниженням температури між молекулами води збільшується число водневих зв'язків. Молекули води розташовуються таким чином, що між ними утворюються порожнечі, тому при замерзанні вода розширюється і лід "легше" води.
Поширення води.
Вода - найпоширеніша речовина на Землі. І в той же час, ми можемо сказати, що на Землі немає чистої води. Чому?
Все що ми називаємо водою, насправді - розчини тих чи інших речовин у воді. Вода - один з кращих розчинників, тому природна вода містить домішки:
-морська вода містить домішки солей;
-дощова вода містить домішки розчинених газів атмосфери (азоту, кисню, вуглекислого газу);
-колодязна вода містить сульфати і карбонати кальцію, магнію, натрію, калію.
На частку прісної води доводиться тільки 3%. Велика частина прісної води (85%) знаходиться на полюсах Землі у вигляді льодовиків і айсбергів.
Хімічні властивості.
- Вода реагує з багатьма металами з виділенням водню.
- З неметалів з водою реагують, наприклад, вуглець і його водневе з'єднання (метан). Ці речовини набагато менш активні, ніж метали, але все ж здатні реагувати з водою при високій температурі.
- Вода розкладається на водень і кисень при дії електричного струму.
- Вода реагує з багатьма оксидами неметалів. На відміну від попередніх, ці реакції не окислювально-відновні, а реакції з'єднання:
SO2 + H2O = H2SO3
сірчиста кислота
SO3+H2O=H2SO4
сірчана кислота
CO2+H2O=H2CO3
вугільна кислота
5. Деякі оксиди металів також можуть вступати в реакції з'єднання з водою. Приклади таких реакцій ми вже зустрічали:
CaO+H2O=Ca (OH) 2
гідроксид кальцію (гашене вапно)
6. Вода утворює численні сполуки, в яких її молекула повністю зберігається. Це так звані гідрати. Якщо гидрат кристалічний, то він називається кристаллогидрата. наприклад:
CuSO4 + 5 H2O = CuSO4.5H2O
речовина білого кольору кристаллогидрат (мідний купорос), сині кристали
ІV. Узагальнення.
Питання:
1. Історія відкриття води?
2. Поширеність води?
3. Значення води?
4. Формула води і її фізичні властивості.
5. З якими речовинами вода взаємодіє?
Деякі реакції я зараз продемонструю (взаємодія з металами, твердими речовинами і рідкими, термохімічні реакції)
V. Домашнє завдання.


про публікацію авторської розробки
Додати розробку
