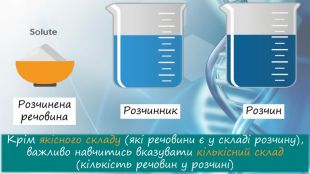
Масова частка речовини у розчину
Про матеріал
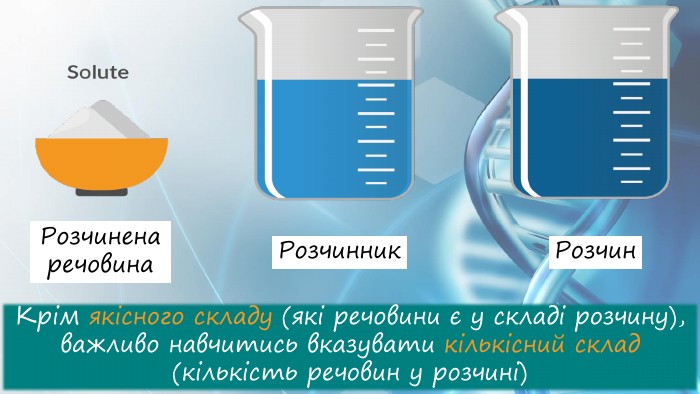
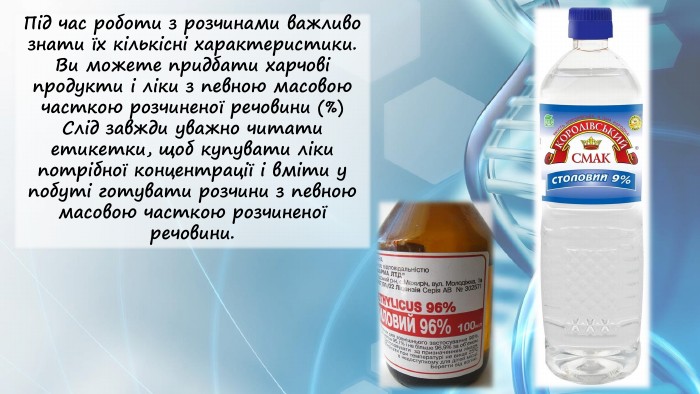
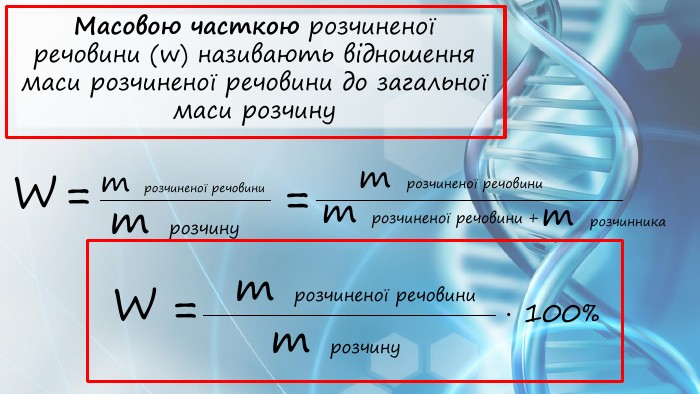
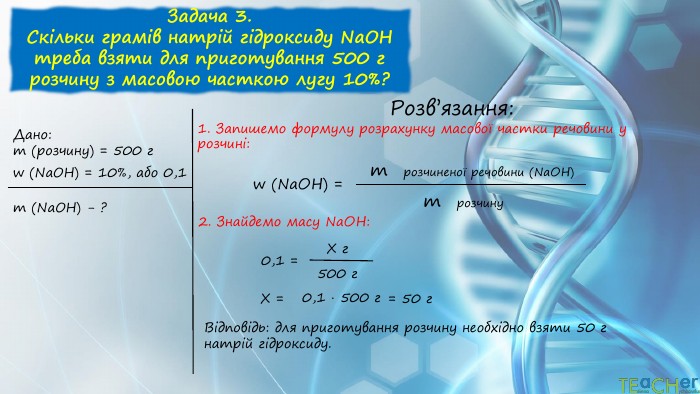
презентація на тему массова частка розчиненої речовини у розчині, кількісний склад розчину з прикладами розв'язання задач. Для учнів 7 класу з хімії Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку