Метанол, етанол, гліцерин: будова молекул, фізичні властивості. Застосування
Урок дозволяє сформувати уявлення про оксигеновмісні органічні сполуки, дати поняття про спирти та їхню функціональну групу, ознайомити учнів із представниками спиртів – метанолом та етанолом, навчити записувати їхні молекулярні , електронні та структурні формули; розглянути фізичні властивості спиртів і визначити їх залежність від утворення водневого зв'язку між молекулами; ознайомити учнів зі згубним фізіологічним впливом спиртів на організм людини, виявити причини токсичності етилового спирту.
Конспект уроку з теми: Метанол, етанол, гліцерин: будова молекул, фізичні властивості. Застосування
Мета:
- освітня: сформувати уявлення про оксигеновмісні органічні сполуки, дати поняття про спирти та їхню функціональну групу, ознайомити учнів із представниками спиртів – метанолом та етанолом, навчити записувати їхні молекулярні , електронні та структурні формули; розглянути фізичні властивості спиртів і визначити їх залежність від утворення водневого зв’язку між молекулами; ознайомити учнів зі згубним фізіологічним впливом спиртів на організм людини, виявити причини токсичності етилового спирту.
- виховна: сформувати науковий світогляд учнів при вивченні фізичних властивостей спиртів,їх фізіологічного впливу на організм; сприяти естетичному, екологічному вихованню;
- розвиваюча:
1) розвивати спостережливість учнів на уроці хімії;
2) розвивати пізнавальний інтерес учнів до предмету;
3) розвивати такі мисленнєві операції : вміння узагальнювати, робити висновки.
Тип уроку: Урок засвоєння нових знань та вмінь.
Обладнання: підручник з хімії для 9 класу.
Базові поняття й терміни: спирти, метанол, етанол, гідроксильна група,функціональна група.
Хід уроку
І. Організаційний етап
Доброго дня, вітаю тих хто:
- Вже прокинувся;
- Випив кави;
- Не снідав;
- Хоче працювати;
- Має на собі щось червоне;
- У доброму гуморі;
- Хотів би дізнатись про щось нове;
- Хоче спілкуватись.
Формування в учнів здоров´язберігаючих компетенцій
Щоб не мати сколіозу
Сидіть прямо за столом,
Тримайте ноги на підлозі
Тільки під прямим кутом.
Також про зір не забувайте –
Рівно голову тримайте
ІІ. Актуалізація опорних знань:
1 Самостійна робота
Давайте ми з вами повторимо те, що вже вивчили на попередніх уроках.
2 Бесіда
1. Які хімічні елементи можуть входити до складу органічних сполук?
2. Які хімічні елементи входять до складу вуглеводнів?
3. Як поділяють вуглеводні?
4. Чим відрізняються насичені вуглеводні від ненасичених?
5. Назвіть загальну формулу насичених вуглеводнів.
6. Назвіть загальну формулу ненасичених вуглеводнів.
7. Чому у ненасичених вуглеводнів дві загальні формули?
ІІІ. Мотивація навчальної діяльності учнів:
На минулих уроках ми з вами вивчали насичені й ненасичені вуглеводні і ви вже знаєте що до їх складу входять атоми Карбону й Гідрогену. Ми довідалися про їх склад, структуру, властивості та застосування.
Багато органічних сполук містять у своїх молекулах, крім атомів Карбону і Гідрогену, ще й атоми Оксигену. Такі сполуки називаються оксигеновмісними. І ми розпочинаємо ознайомлення з ними. Оксигеновмісні сполуки поділяються на класи – клас спиртів, клас карбонових кислот, клас естерів, клас жирів тощо. Сьогодні на уроці ми ознайомимося із класом спиртів.
Отже, записуємо тему уроку: «Метанол, етанол, гліцерин: будова молекул, фізичнівластивості.Застосування »
Учніповинні:
- знати: загальну формулу одноатомнихспиртів, фізичнівластивостіметанолу,етанолу та гліцерину;
- вміти: складатимолекулярні, електронні та структурніформули метанолу,етанолу та гліцерину.
ІV. Вивчення нового матеріалу:
Як уже зазначалося, молекули органічних сполук, крім атомів Карбону і Гідрогену, можуть містити атоми Оксигену і називаються оксиненовмісними.
Оксисен, як правило, входить до складу органічних сполук у вигляді груп атомів. Такі групи атомів називають функціональними групами.
Функціональні групи – це групи атомів, що визначають хімічні й фізичні властивості речовин.
Наприклад:
– ОН – гідроксильна група;
– СОН – карбонільна;
– СООН – карбоксильна.
Органічні речовини, молекули яких містять одну або кілька функціональних гідроксильних груп, з’єднаних з вуглеводнями називаються спиртами.
За кількістю гідроксильних груп спирти поділяють на одноатомні і багатоатомні.

![]()
![]()

![]()
За природою вуглеводневого радикала
- Насичені
- Ненасичені
- Ароматичні
Уявімо, що в молекулі метану один атом Гідрогену заміщений гідроксильною групою. Хімічна будова такої сполуки – метанолу – виражається структурною формулою:
Н Н
![]()
![]()
Н – С – Н Н – С – О – Н , або скорочено СН3 – ОН, або СН3ОН
![]()
![]()
Н Н
Метан Метанол
Заміщуючи атом Гідрогену в молекулі етану, дістаємо сполуку етанол такої хімічної будови:
Н Н Н Н
![]()
![]()
![]()
![]()
Н – С – С – Н Н – С – С – О – Н , або скорочено СН3 –СН2 – ОН, або
![]()
![]()
![]()
![]() С2Н5ОН
С2Н5ОН
Н Н Н Н
Етан Етанол
У цих сполуках вуглеводневі радикали метил – СН3 і етил – С2Н5 з´єднані з гідроксильною групою – ОН. Наявність цієї групи є ознакою класу органічних речовин, що належить до класу спиртів.
Загальну формулу насичених одноатомних спиртів можна вивести із загально формули насичених вуглеводнів шляхом заміщення атома Гідрогену на гідроксильну групу.
Сn Н2n+2Сn Н2n+1 OH
загальна формула загальна формула насичених
насичених вуглеводнів одноатомних спиртів
Якщо вуглеводневий радикал позначили літерою R, то загальна формула спиртів позначається як R – ОН.
Оскільки до складу молекул наведених спиртів входить одна функціональна гідроксильна група, такі спирти належать до одноатомних.Насичені одноатомні спирти утворюють гомологічний ряд
|
Формула |
Систематична назва |
Традиційна назва |
|
СН3ОН |
Метанол |
Метиловий спирт |
|
С2Н5ОН |
Етанол |
Етиловий спирт |
|
С3Н7ОН |
Пропанол |
Пропиловий спирт |
|
С4Н9ОН |
Бутанол |
Бутиловий спирт |
|
С5Н11ОН |
Пентанол |
Аміловий спирт |
|
С6Н5ОН – СН2ОН |
Фенілкарбінол |
Бензиловий спирт |
|
СН2ОН – СН2ОН |
1,2-етандіол (етан -1,2-діол) |
Етиленгліколь |
|
СН2ОН – СНОН – СН2ОН |
1,2,3 – пропантриол (пропан – 1,2,3, - триол) |
Гліцерин |
Номенклатура спиртів
Відповідно до систематичної номенклатури, назви спиртів походять від назв відповідних вуглеводів з додаванням суфікса –ол. Нумерацію карбонового скелета починають із того краю, ближче до якого знаходиться гідроксильна група.
Положення гідроксильної групи вказують цифрою перед назвою спирту:
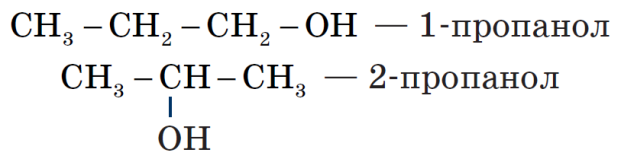
Фізичні властивості метанолу й етанолу.
У гомологічному ряду насичених одноатомних спиртів немає газуватих речовин. Перші члени гомологічного ряду – церідини, а вищіспирти (від С15) – тверді речовини. У гомологічному ряду нормальних (нерозгалужених) спиртів зі збільшенням молекулярної маси збільшуються температури плавлення та кипіння. Густина спиртів майже не змінюється. Розчинність у воді при цьому погіршується, хоча перші три члени гомологічного ряду змішуються з водою необмежено. Тверді спирти не мають запаху, у той час як рідкі спирти мають специфічні запахи. При цьому метанол та етанол за запахом дужесхожі й відрізнитиїхдуже складно.
Фізичнівластивостіспиртів.
|
Назва |
Формула |
М, г/моль |
Густина, г/мл |
tпл., 0С |
tкип., 0С |
Розчинність у воді |
|
Метанол |
CH3OH |
32 |
0,79 |
-97,5 |
64,5 |
Розч.необмеж. |
|
Етанол |
C2H5OH |
46 |
0,79 |
-114.5 |
78,3 |
Розч.необмеж. |
|
Пропанол |
C3H7OH |
60 |
0,80 |
-126,2 |
97,2 |
Розч.необмеж. |
|
Бутанол |
C4H9OH |
74 |
0,81 |
-89,5 |
117,1 |
Розчинний (7%) |
|
Пентанол |
C5H11OH |
88 |
0,81 |
-78,9 |
138,1 |
Малорозч.(2%) |
|
Гексанол |
C6H13OH |
102 |
0,81 |
-46,1 |
157,5 |
Пр.нерозч.(0,7%) |
|
Гептанол |
C7H15OH |
117 |
0,81 |
-30,6 |
176,4 |
Нерозчинний |
|
Октанол |
C8H17OH |
130 |
0.82 |
-15 |
195,3 |
Нерозчинний |
Крім одноатомних спиртів, тобто тих, що містять у молекулі одну функціональну групу, існують багатоатомні спирти, до складу яких входять дві і більше функціональні гідроксильні групи. Найважливіший із них – гліцерин – трьохатомний спирт. Структурна формула гліцерину
Н Н Н
![]()
![]()
![]()
Н – С – С – С – Н , або скорочено СН2 – СН – СН2
![]()
![]()
![]()
![]()
![]()
![]()
ОН ОН ОН ОН ОН ОН
Загальна формула багатоатомних спиртів R-(ОН)n
Приклади багатоатомних спиртів
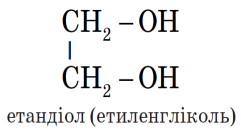
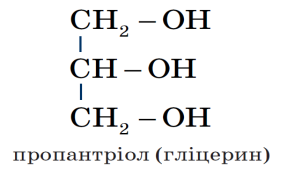
Фізичні властивості гліцерину.
Це густа сироподібна рідина без запаху і кольору, солодка на смак, добра розчинна у воді. Властивості гліцерину відбиває його назва «олійний цукор», вживана у ХVІІІ ст., коли гліцерин було добуто вперше з маслинової олії.
Аби дослідити розчинення гліцерину у воді, виконаймо лабораторний дослід.
Лабораторний дослід №8 «Фізичні властивості гліцерину»
Обладнання: піпетка, пробірка, фільтрувальний папір.
Реактиви: гліцерин, чорнило або харчовий водорозчинний барвник, дистильована вода.
Дослід 1. Розгляньте гліцерин у склянці. Трохи нахиліть її. Чи має гліцеринколір? Чи в’язка ця рідина? Пригадайте прийоми вивчення запаху речовин. Відкрийте склянку з гліцерином, визначте, чи має він запах. На аркуш фільтрованого паперу нанесіть краплю гліцерину, на інший – краплю води. Наприкінці уроку переконайтесь, що папір з водою висох, а з гліцерином став ще вологішим.
Дослід 2. Налийте в пробірку воду об’ємом 0,5 мл і добавте краплю барвника. Суміш збовтайте. Добавте в пробірку дві краплі гліцерину, збовтайте. Добавте ще краплю гліцерину і знов збовтайте. Чи розчиняється гліцерин у воді? Для чого воду попередньо підфарбували?
Застосування метанолу й етанолу й гліцерину
Метиловий спирт був вперше добутий у ХVІІ ст., а вивчений у першій половині ХІХ ст. Його називають ще деревним спиртом за першим із відомих методів добування, а саме шляхом сухої перегонки деревини.
Етиловий спирт,етанол, винний спирт, алкоголь – назви-синоніми однієї сполуки, що є основою алкогольних напоїв і найвідоміша із класу спиртів. Археологічні розкопки засвідчують, що в епоху найдавніших цивілізацій уміли виробляти вино й пиво. Скидається на те, що алкоголь був найпершою сполукою, синтезованою людиною. Перша літературна згадка про власне етиловий спирт як «горючу воду», добутою перегонкою вина, відноситься до VІІІ ст.,а елементний склад етанолу було з’ясовано на початку ХІХ ст.
Метанол і етанол – розчинники. Ця їхня властивість використовується в органічному синтезі та лабораторній практиці. Етанол як розчинник застосовується у фармації, медицині, харчовій промисловості.
Гліцерин – продукт, що має широке застосування. Завдяки гігроскопічності він використовується в парфумерії та фармації, як зм’якшувальний засіб або основа мазей, добавка до мила, у харчовій промисловості – як добавка до напоїв. У шкіряному виробництві та текстильній промисловості - для обробки пряжі і шкіри з метою їх пом’якшення та надання еластичності. З гліцерину добувають вибухову речовину нітрогліцерин, що використовується для виготовлення динаміту. Спиртовий розчин нітрогліцерину має судиннорозширювану дію й у вигляді ліків використовується при серцевих захворюваннях.
V. Узагальнення та систематизація знань.
Бліц-опитування
- Які органічні речовини називають спиртами?
- Що таке функціональна група?
- Яку функціональну групу мають спирти?
- За якою ознакою спирти поділяють на одноатомні та багатоатомні?
- Що спільного в застосуванні етанолу й гліцерину?
- Який спирт спричиняє захворювання – алкоголізм?
Прийом «Так чи ні»
- Спирти – це органічні сполуки, які містять гідроксогрупи.
- Одноатомні спирти містять одну гідроксогрупу.
- Гліцерин належить до одноатомних спиртів.
- Етанол можна застосовувати для пом’якшення шкіри.
- Гліцерин можна застосовувати для пом’якшення шкіри.
- Етанол і гліцерин застосовують у парфумерії.
- Метанол відносять до багатоатомних спиртів.
- Метанол – отрута.
- Етанол – багатоатомний спирт.
- Гліцерин – багатоатомний спирт.
VI. Підбиття підсумків уроку
На сьогоднішньому уроці ми з вами ознайомилися з представниками спиртів, а саме з метанолом, етанолом та гліцерином. Навчилися відрізняти одноатомні спирти від багатоатомних, ознайомилися з фізичними властивостями та їх застосуванням.
- Які нові поняття ми вивчили сьогодні на уроці?
- Чи мають для вас практичне значення нові знання, отримані на уроці?
- Метанол – рідина без кольору, з різким запахом добре розчинна у воді в будь-яких співвідношеннях, отруйна.
- Етанол - рідина без кольору, з різким запахом добре розчинна у воді в будь-яких співвідношеннях, отруйна.
- Гліцерин – грузла рідина без кольору й запаху, солодка на смак, добре розчинна у воді.
Ви сьогодні гарно попрацювали, були активними і допитливими, тож давайте оцінимо вашу роботу.
VII. Домашнє завдання:
Чит. §27(будова молекул, фізичні властивості) ст. 182-185;
§28(застосування метанолу, етанолу й гліцерину) ст. 190-192;
Впр. 1-6 ст. 189 і 1-5 ст. 194
Творче завдання. Підготувати розповідь про отруйність спиртів, шкідливий вплив метанолу й етанолу на організм людини та виготовити антирекламу на тему : «Мінздрав попереджає: алкоголь - це отрута для нашого організму»
Література:
1) Хімія. 9 клас: Розробки уроків (до підручника « Хімія. 9 клас » П.П. Попеля, Л.С. Криклі) /В.І. Гордієнко, О.В. Григорович, А.В. Віценцик, О.М. Гостиннікова. – Х.: Вид-во «Ранок», 2010. – 272с.
2) А.Т. Пилипенко, В.Я. Починок, И.П. Середа, Ф.Д. Шевченко. - Справочник по элементарной химии. / Под ред. Академика АН УССР А.Т. Пилипенко. – К.: Наукова думка. – 1985.
3) Органічна хімія : Посібник для вчителів хімії та учнів загальноосвітніх шкіл, ліцеїв, гімназій, слухачів і викладачів підготовчих відділень вузів / Березан О.В.- К.: Абрис, 2000. - 304с.


про публікацію авторської розробки
Додати розробку
