Методична розробка заняття з хімії на тему: "Хімічні властивості Алкенів та Алкінів"
Відокремлений структурний підрозділ - Львівський коледж «Інфокомунікації» Національного університету «Львівська політехніка»
Методична розробка заняття з хімії на тему:

Розробила:
Викладач Мельник Н.М.
Львів
Тема заняття: Хімічні властивості алкенів та алкінів Мета заняття: методична: Удосконалювати методику застосування інтерактивних методів навчання на заняттях з хімії;
навчальна: ознайомити студентів з хімічними властивостями ненасичених вуглеводнів на прикладі етилену та ацетилену;
закріпити знання про номенклатуру, ізомерію та будову молекул алканів, алкенів та алкінів; формувати навички і вміння працювати колективно;
розвивальна: розвивати науково- екологічний світогляд, пам’ять, логічне та критичне мислення, уміння чітко формулювати свої думки;
виховна: виховувати творчий підхід до навчання, активну життєву позицію, прищеплювати любов і дбайливе ставлення до природи, інтерес до хімії та її роль в житті людини.
Вид заняття: лекційне
Тип заняття: лекція з використанням презентації та евристичної бесіди
Методи та форми роботи: інтерактивні методи навчання: робота у групах, фронтальне опитування, дидактичні ігри віртуальної лабораторії, метод проектів, евристична бесіда, випереджувальні завдання - повідомлення студентів, дискусія.
Міжпредметні зв’язки: біологія, географія.
Обладнання: дидактичні матеріали: картки із завданнями з хімії, комп'ютерна презентація ходу заняття , комп'ютерні програми «Chemsk» («Будова молекул етилену та ацетилену») та «Віртуальна лабораторія»
Література:
1. Березан О.В. Органічна хімія: навч.посіб.- Тернопіль, 2018
2. Ярошенко О.Г. Хімія 10 кл. 2018
Хід заняття
1. Організаційна частина заняття 5 хв
- відмітка в журналі відсутніх;
- перевірка готовності до заняття студентів, аудиторії, обладнання.
2 Актуалізація опорних знань.
Один із загальновідомих,
Кістяк органічних сполук,
Цеглинка, фундамент, основа Для всіх природничих наук. Карбон «С»
2.1 Вступне слово викладача:
Сьогодні ми з вами узагальнимо ті знання, які здобули під час вивчення насичених та ненасичених вуглеводнів.
Завдання, які ви будете сьогодні виконувати, покажуть, наскільки ви засвоїли навчальний матеріал, вмієте його застосовувати.
Сьогодні ви покажете свою ерудицію, ораторську майстерність, вміння працювати індивідуально, в групах, знаходити правильні рішення тощо.
2.2 Фронтальне опитуваня
1. Наведіть загальні формули алканів ( СnH2n+2)
2. Назвіть види гібридизації атомів Карбону в молекулах метану(sp3)
3. Якими видами хімічного зв’язку утворені молекули алкенів та алкінів(подвійними та потрійними)
4. Вуглеводні — сполуки, що складаються з атомів ... і ... . ( С і Н)
5. За сучасною українською номенклатурою насичені вуглеводні називають . . .
(Алкани)
6. В усіх органічних речовинах валентність атомів С становить ... (4)
7. Найпростіший представник алканів .... (СН4 метан)
8. Загальна формула алкенів ... . (СnH2n)
9. Найпоширенішим представником алкенів є ..( етилен С2Н4).
10. Реакція ,яка характерна для алканів ... .(заміщення)
11. Загальна формула алкінів …( СnH2n-2)
12. Перший представник гомологічного ряду алкінів — .... ацетилен С2Н2)
13.Яку сполуку називають болотяним газом (метан)
14. У молекулі етилену, на відміну від молекули ацетилену, є … (подвійний звязок)
2.3 Використання дидактичних ігор віртуальної лабораторії (мультимедійна гра)
Група ділиться на дві підгрупи, які працюють автономно одночасно.
1 підрупа виконує завдання на мультимедійній дошці, виконуючи такі завдання:
- Знайдіть пару
- Класифікація вуглеводнів
а) Номенклатура IUPAK розгалужених вуглеводнів
б) Перемістити до формули назву вуглеводню
в) Розв'язання кросворду
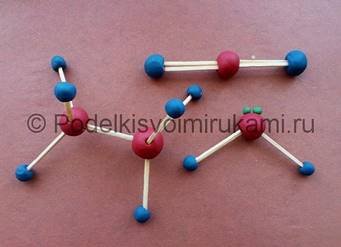
2 підгрупа за допомогою пластиліну та сірників ліплять моделі молекул алканів, алкенів, алкінів


Гра «Хрестики-нулики»
Серед наведених речовин викресліть формули алкенів.
|
СН3ОН |
СН4 |
С2Н4 |
|
С2Н2 |
С3Н6 |
С4Н9ОН |
|
С6Н12 |
НСООН |
С5Н11ОН |
Серед наведених речовин викресліть формули алкінів.
|
СН3СОН |
С4Н6 |
С2Н5СООН |
|
С2Н5СОН |
С3Н4 |
С6Н6 |
|
С3Н7СОН |
С5Н8 |
НСОН |
3 Повідомлення теми, мети та основних завдань заняття.
Тема та завдання до заняття подано на мультимедійній дошці.
3.1 Слово викладача
На даному занятті ми ознайомимось із хімічними властивостями ненасичених вуглеводнів на прикладі етилену та ацетилену. Хімічні властивості етилену і ацетилену:

4 Мотивація навчальної діяльності
Природний газ на 90% складається з метану та етану, решта припадає на пропан та бутан, а от ненасичених вуглеводнів в ньому практично немає. Чому?
Властивості речовин визначаються будовою речовини. Пригадайте алкани (насичені в.в.). Який зв’язок між атомами Карбону в молекулах алканів? (простий) Це були не дуже активні речовини.
Який зв’язок між атомами Карбону у алкенів і алкінів? (подвійний і потрійний, отже як поява кратних зв’язків в будові речовини відображається на їх хімічних властивостях? Відповідь на це питання ми будемо знаходити під час заняття тема якого: «Хімічні властивості алкенів і алкінів» ).
Отже, тема нашого заняття…(студенти записують тему заняття і формулюють мету), використовую комп'ютерну програму «Chemsk».
Мета студентів:
1) Ознайомитися з основними хімічними властивостями ненасичених вуглеводнів;
2) Сформувати вміння складати рівняння реакції;
3) Визначити яке практичне значення мають вивчені хімічні властивості;
5 Вивчення нового матеріалу
5.1 Лекція з використанням презентації та евристичної бесіди
Алкени та алкіни через наявність кратного зв’язку мають високу хімічну активність, здебільшого у них руйнується цей зв'язок і за рахунок цього вони можуть приєднувати по 2 (або 4) атоми.
Зверніть увагу на екран, де зображені структурні формули етилену та ацетилену. Наявність кратних зв’язків зумовлюють реакції приєднання, що супроводжуються розривом ¶- зв’язків.
Демонстрація дослідів відбувається на екрані за допомогою програми
«Віртуальна лабораторія».
Галогенування
С2Н4 + Br2 = С2Н4Br2
С2Н2 + 2Br2 = С2Н2Br4
Знебарвлення бромної води є ознакою для визначення ненасичених вуглеводнів.

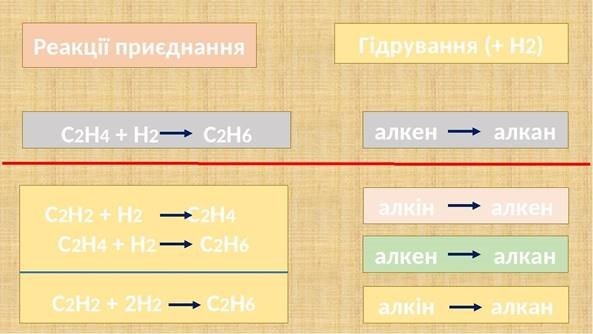
Гідрування
С2Н4 + Н2 = С2Н6
С2Н2 + 2Н2 = С2Н6
Взаємодія з галогеноводнями
С2Н4 + НСl = С2Н5Cl
С2Н2 + 2 НСl = С2Н4Cl2

Правило Марковнікова: атом Гідрогену приєднується до більш гідрогенізованого атома Карбону.
Горіння
С2Н4 + 3О2 = 2СО2 + 2Н2О
2С2Н2 + 5О2 = 4СО2 + 2Н2

6 Закріплення вивченого матеріалу
6.1 Отже,чому ненасичені вуглеводні легше вступають в реакції? Які реакції є якісними на кратні зв’язки ?
Які реакції є характерними тільки для ненасичених вуглеводнів?
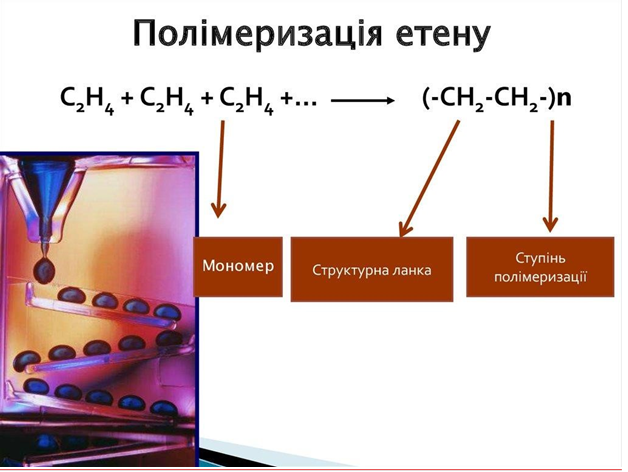
6.2 Повідомлення студентів за випереджувальними завданнями про використання поліетилену та його вплив на навколишнє середовище.
Студенти перед прослуховуванням повідомлення отримують завдання:
Студенти уважно слухають підготовлені доповіді і роблять для себе висновок щодо використання поліетиленових пакетів і їх вплив на навколишнє середовище.
6.3 Рольова гра « Групова дискусія на тему « ».
Усіх студенти розподіляємо на підгрупи: - Ті, що підтримують… - Ті, що проти….
Викладач виконує роль ведучого
7 Коментар роботи студентів на занятті, виставлення оцінок.
Викладач робить поглиблений аналіз роботи студентів на занятті. Всім студентам виставляє оцінки і аргументує їх.
8 Підсумок заняття проходить у формі бесіди - Які завдання ми ставили на початку заняття?
Студенти називають їх.
- Чи справились ми з ними?
- Що корисного ви взяли із цього заняття?
Отже, Сьогодні ви застосовували раніше здобуті знання, оволоділи новими знаннями та практичними навичками. І все це через діяльність, через вашу працю.
Б.Шоу сказав: «Єдиний шлях, який веде до знань - це праця».
«Без повсякденної працьовитості нема ні геніїв, ні талантів», - говорив Д.Менделєєв.
Чи поставленої мети ми з вами досягли?
Отже, Працюйте й будьте щасливі!
9 Домашнє завдання
Повторити матеріал про вуглеводні.


про публікацію авторської розробки
Додати розробку
