Надлишок. Алгоритм розв'язання задач
Про матеріал
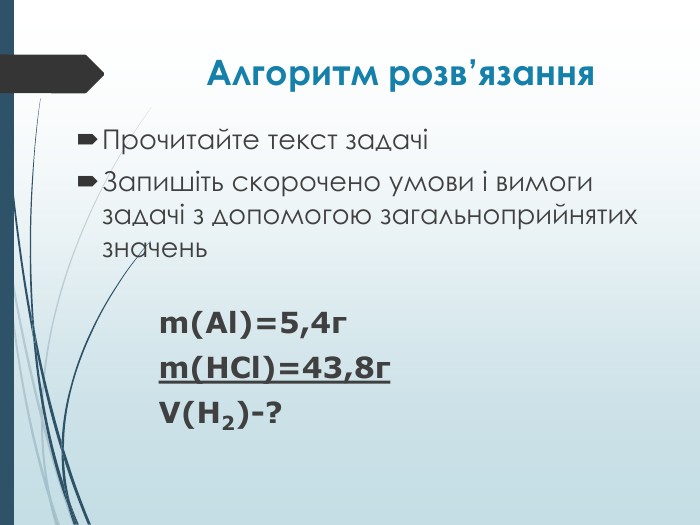
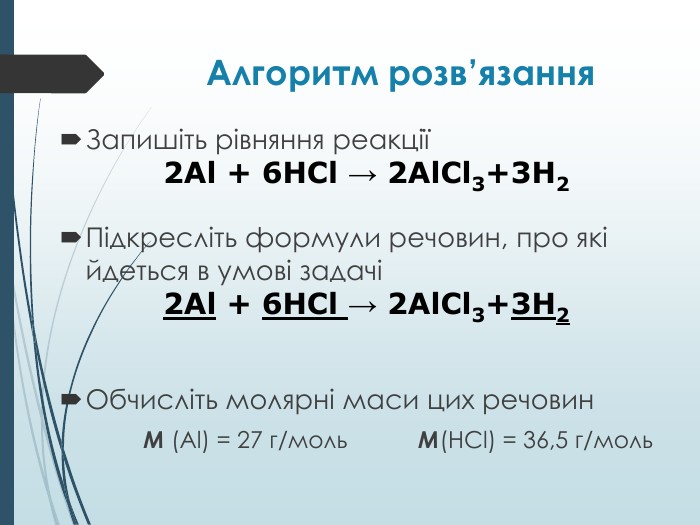
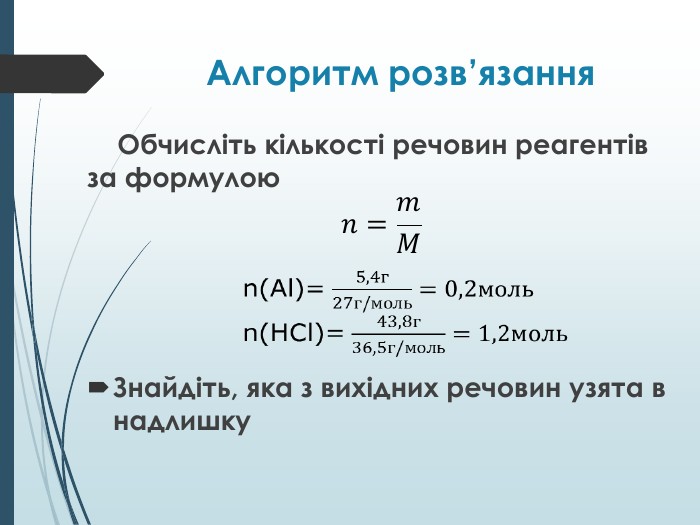
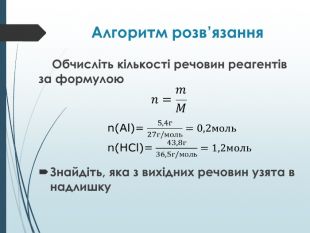
Мета уроку: а) навчальна: ввести поняття задачі на надлишок, довести до учнів алгоритм розв’язування задач такого типу, навчити учнів розв’язувати задачі за даним алгоритмом.
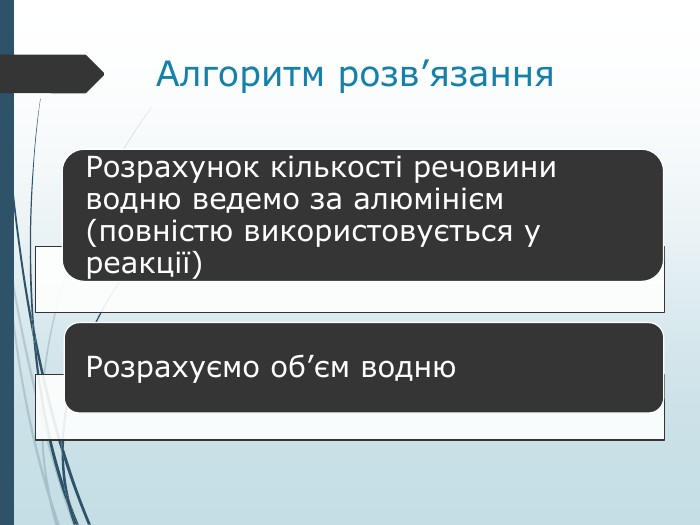
б) розвиваюча: розвивати вміння розв’язувати задачі на надлишок реагентів; розвивати логічне, творче мислення; вміння аналізувати, узагальнювати, робити висновки, спостерігати. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку