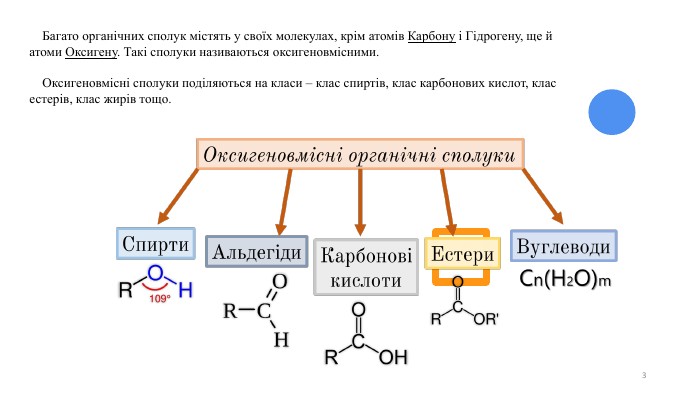
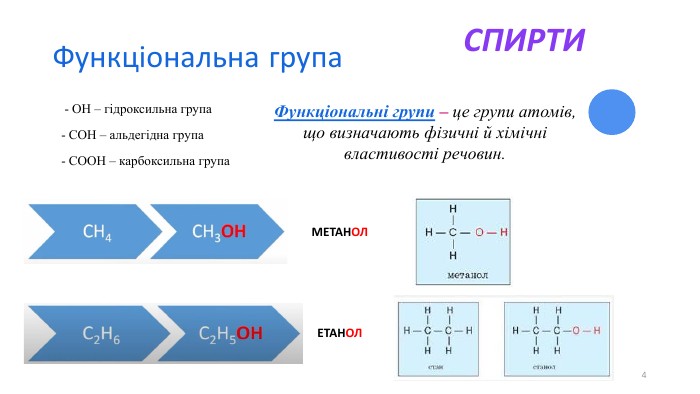
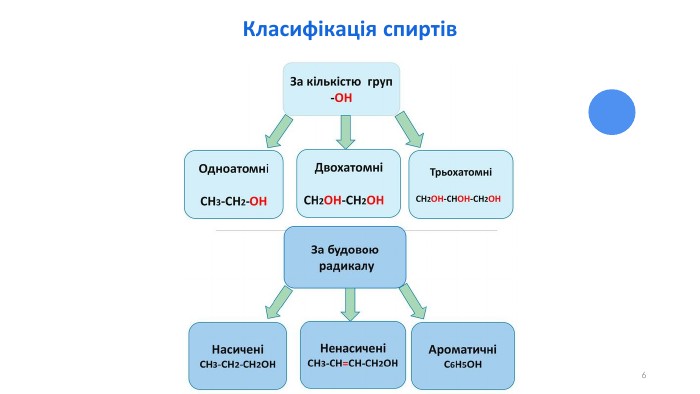
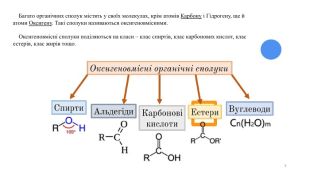
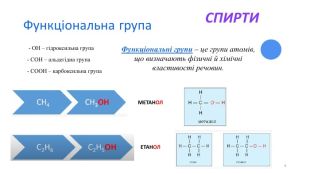
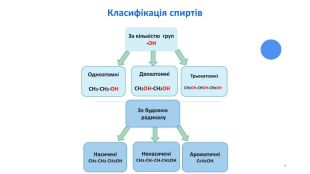
Оксигеновмісні органічні сполуки. Спирти
Про матеріал
Оксигеновмісні орагічні сполуки. Спирти. Будова молекули. Номенклатура. Властивості. Фізіологічна дія на організм людини Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку