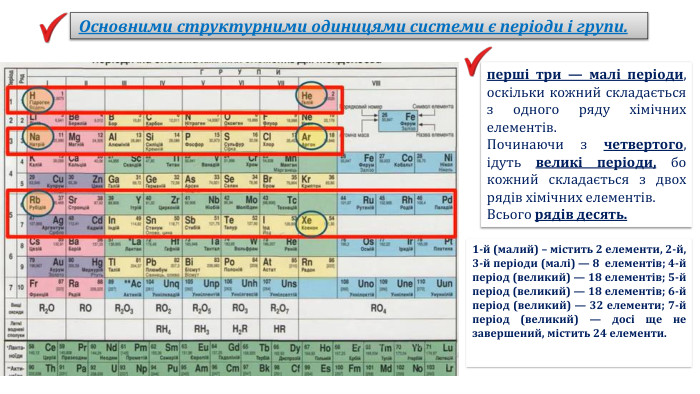
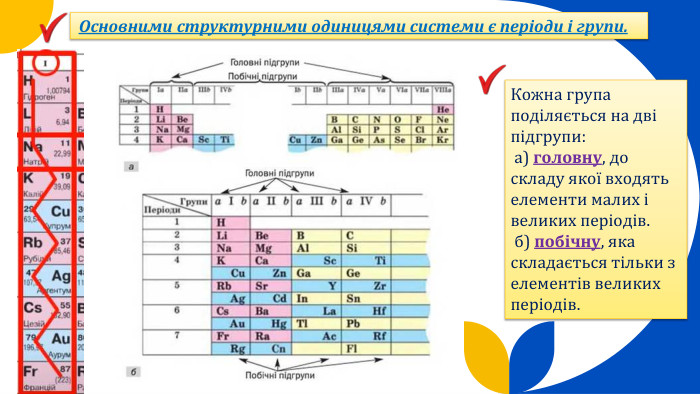
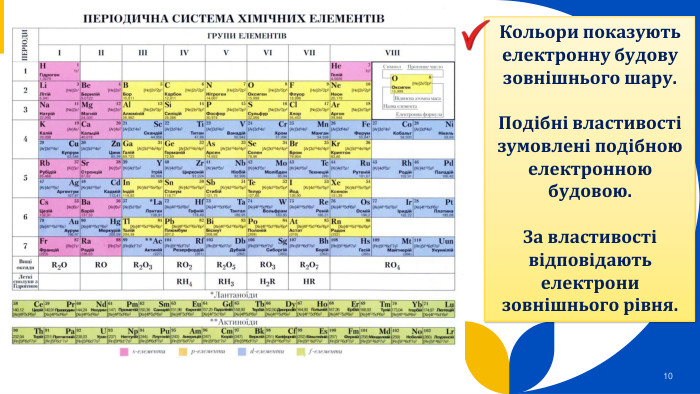
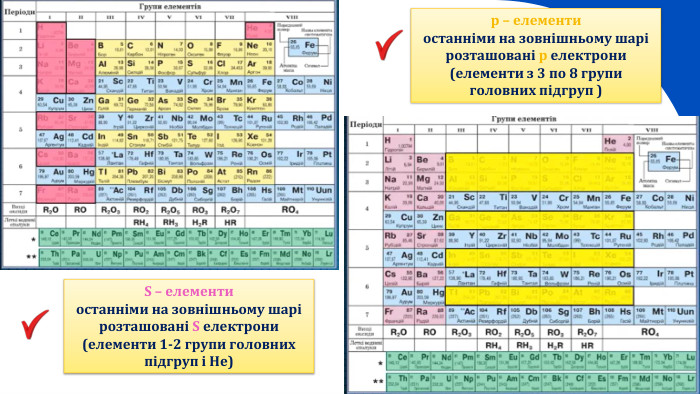
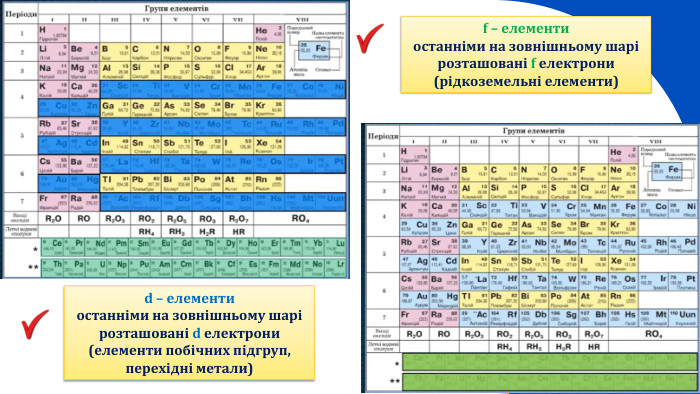
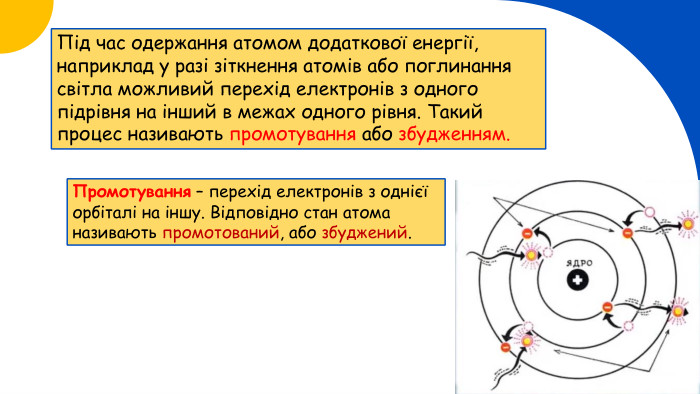
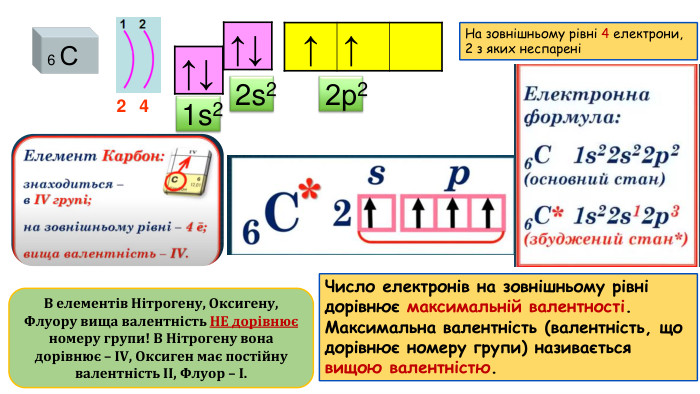
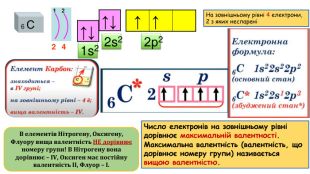
Періодична система хімічних елементів, її структура.(частина 1)
Про матеріал
Презентаційний матеріал з теми "Періодична система хімічних елементів, її структура (частина 1)" Перегляд файлу
Зміст слайдів
pptx
До підручника
Хімія (профільний рівень) 10 клас (Буринська Н.М. та інші)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку