Презенація "Генетичні зв’язки між основними класами неорганічних сполук"
Про матеріал
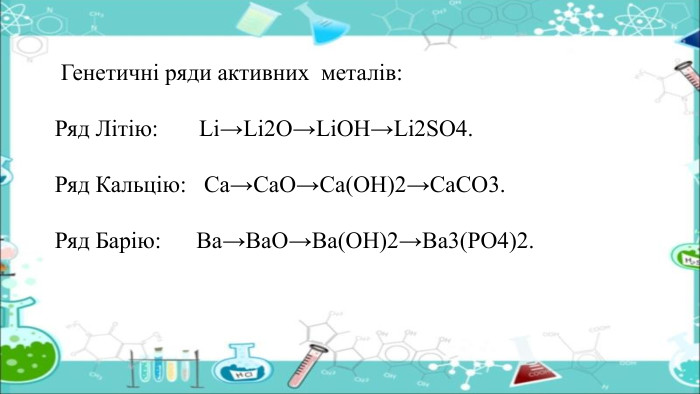
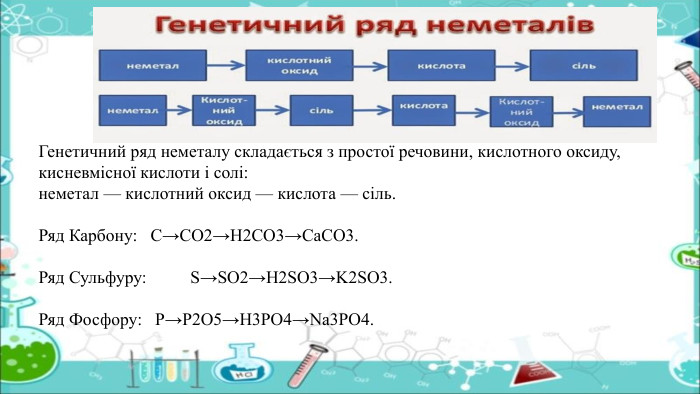
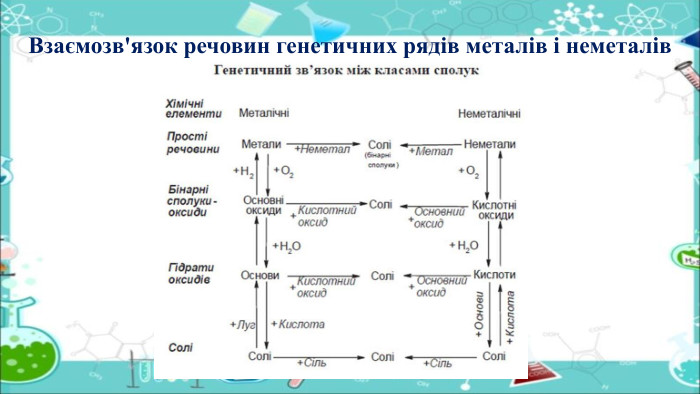
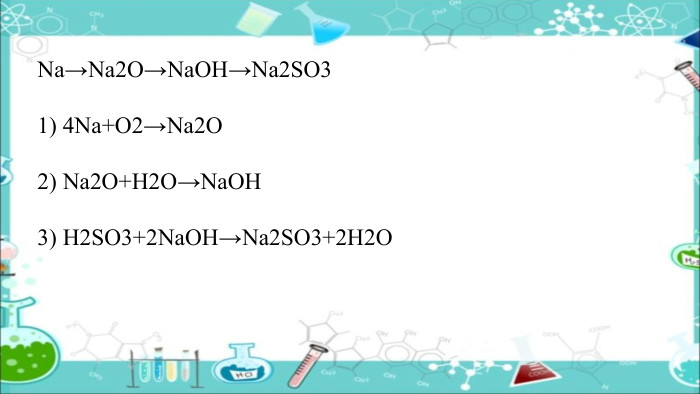
Презенація "Генетичні зв’язки між основними класами неорганічних сполук" допоможе розкрити взаємозв’язок явищ у природі на прикладі взаємоперетворень одних класів речовин на інші; узагальнити знання про неорганічні речовини та їх властивості; розвивати вміння порівнювати склад і властивості речовин, класифікувати речовини й реакції, встановлювати генетичний зв’язок між класами неорганічних сполук
Перегляд файлу
Зміст слайдів

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку