Презентація "Білки як біологічні полімери"
Про матеріал
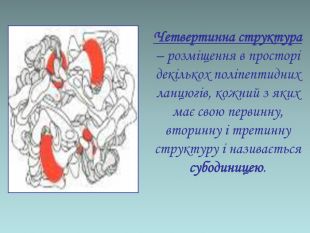
В презентації надається інформація про білки як біологічні полімери, розповідається про: рівні організації білкових молекул, хімічні властивості. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку