Презентація до конкурсної розробки уроку "Учитель року - 2020" - хімія.
Про матеріал
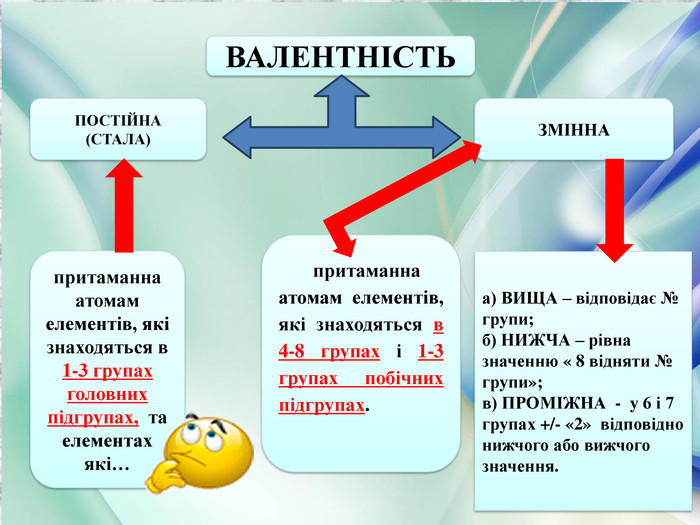
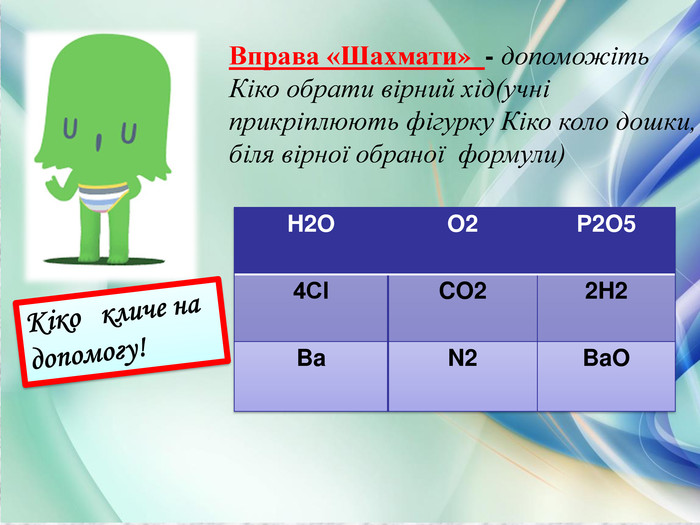
Конкурсна розробка уроку на 45 хвилин "Учитель року - 2020" Хімія , 7 клас Тема : « Валентність хімічних елементів. Складання формул бiнарних сполук за валентністю елементів.» Мета роботи була : сформувати поняття про валентність, одиницю валентності, навчити учнів складати формули сполук за валентністю; розвивати логічне мислення та творчі здібності. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку