Презентація до уроку: "Бензен: хімічна формула, фізичні та хімічні властивості"
Про матеріал
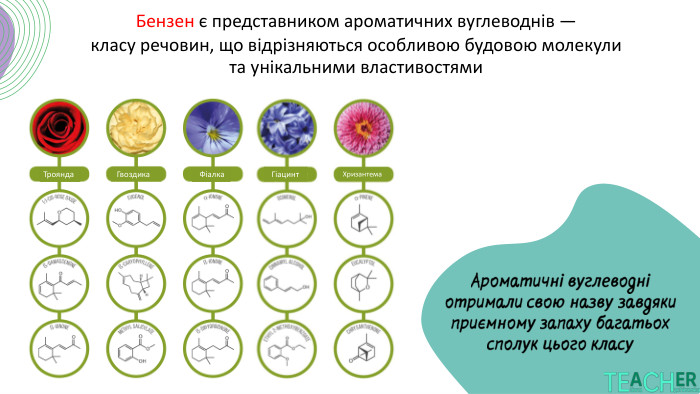
Презентація «Бензен» присвячена одному з найважливіших представників ароматичних вуглеводнів. У ній розкрито:
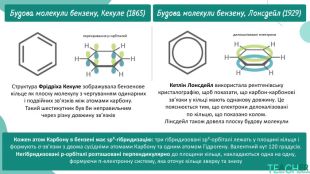
історію відкриття та значення бензену в органічній хімії;
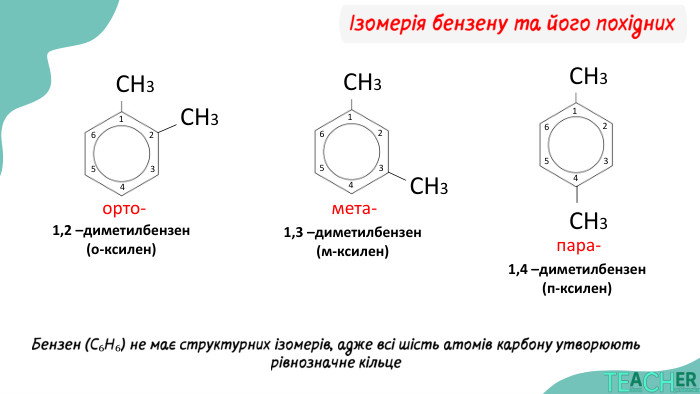
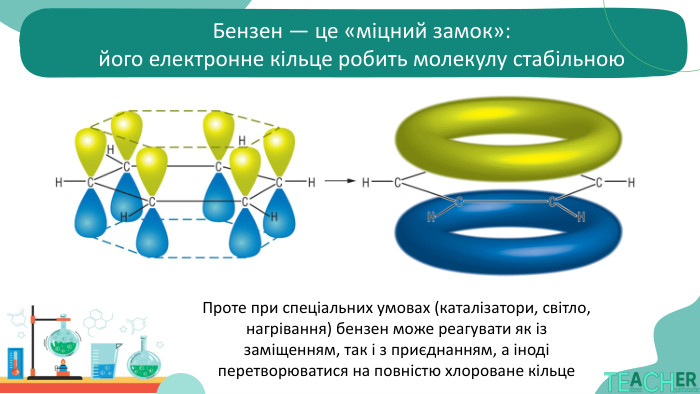
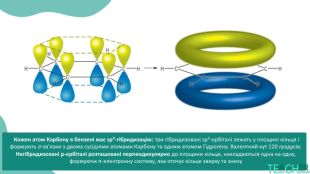
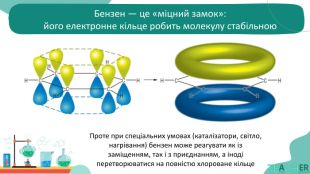
будову молекули та особливості ароматичного кільця;
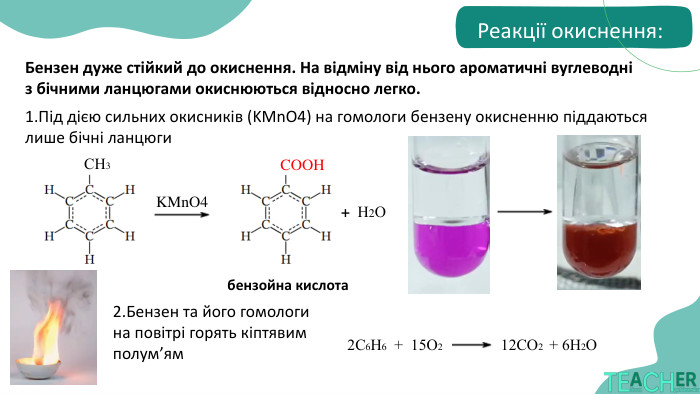
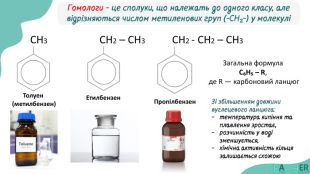
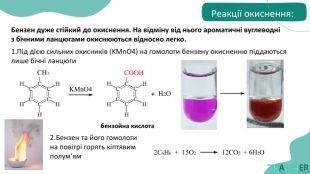
фізичні та хімічні властивості;
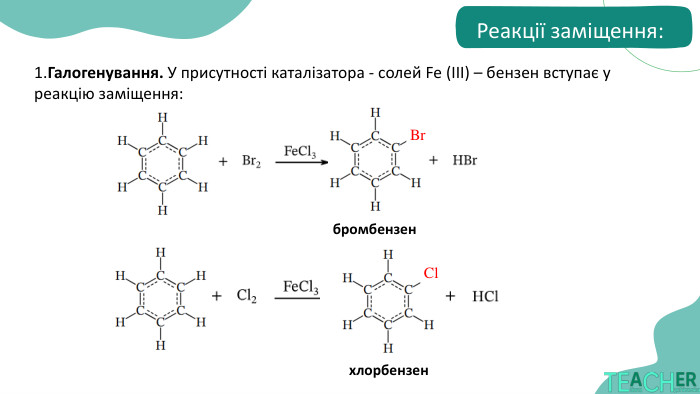
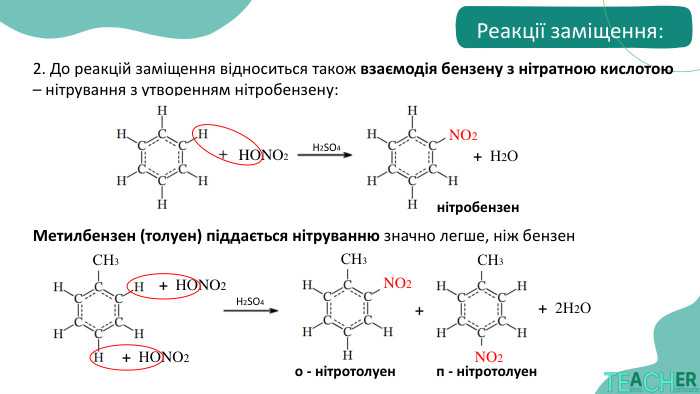
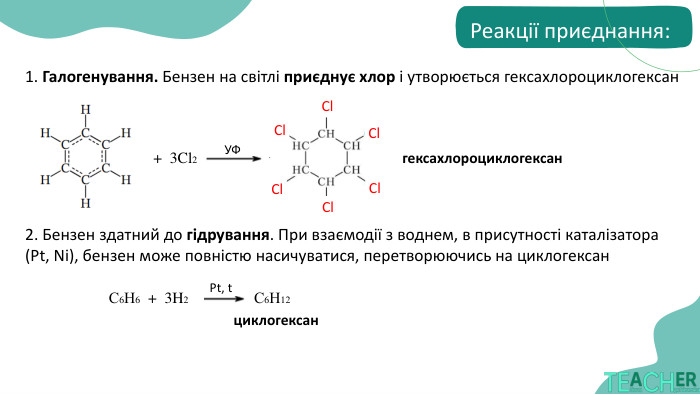
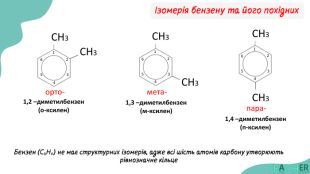
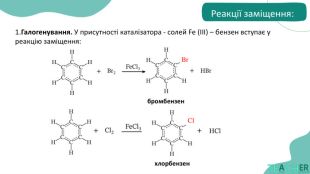
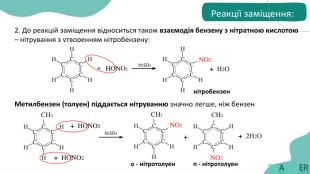
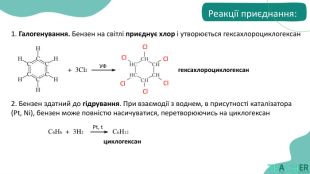
реакції, характерні для бензену та його похідних;
застосування у промисловості та повсякденному житті;
екологічні та токсикологічні аспекти.
Матеріал презентації допоможе учням сформувати цілісне уявлення про роль бензену в хімії та житті людини, а також усвідомити необхідність безпечного поводження з цією сполукою. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Щиро вдячна!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку