Презентація до уроку: "Фізичні тіла. Матеріали. речовини. Молекули. Атоми"
Про матеріал
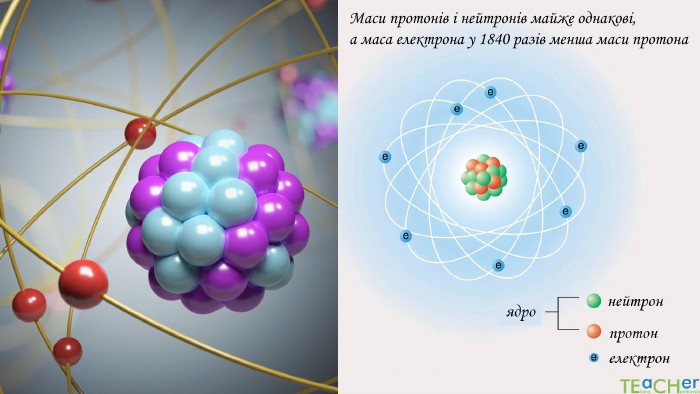
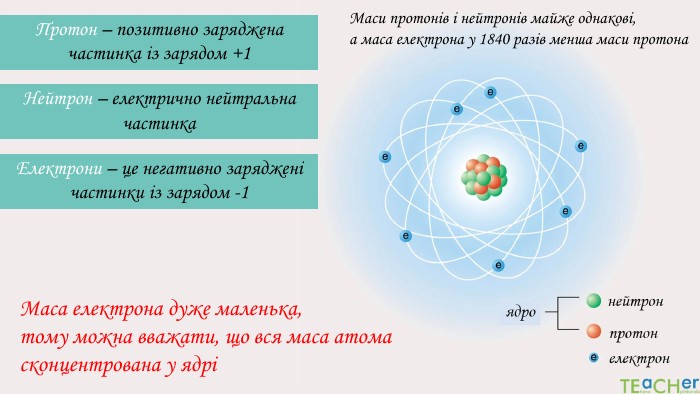
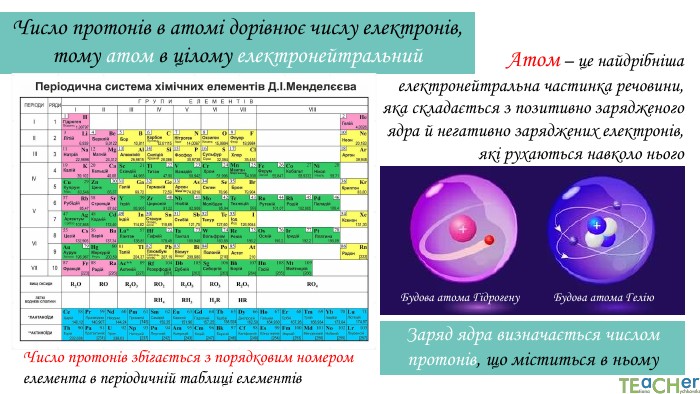
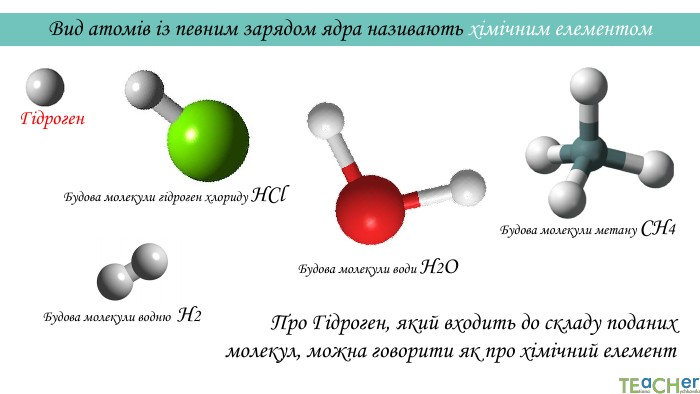
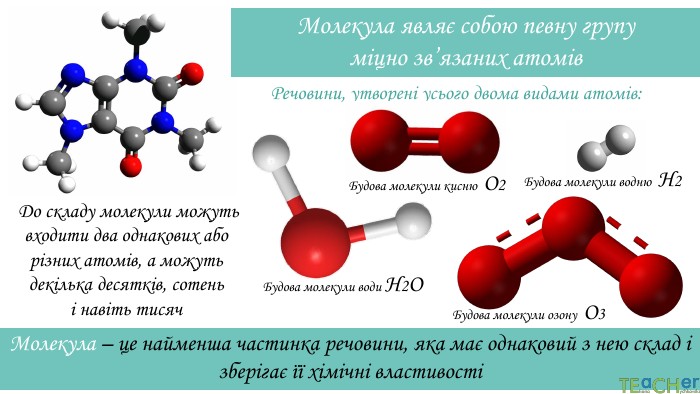
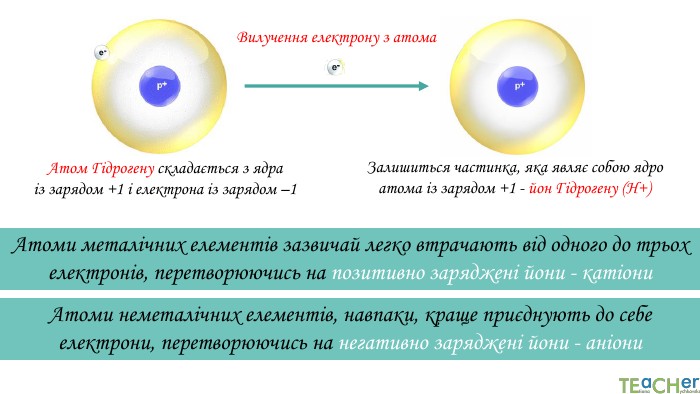
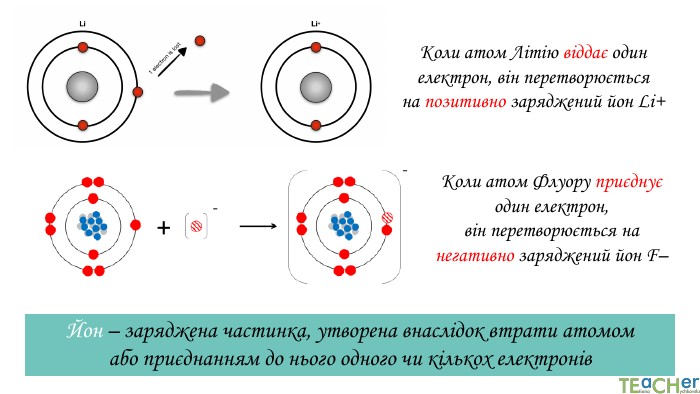
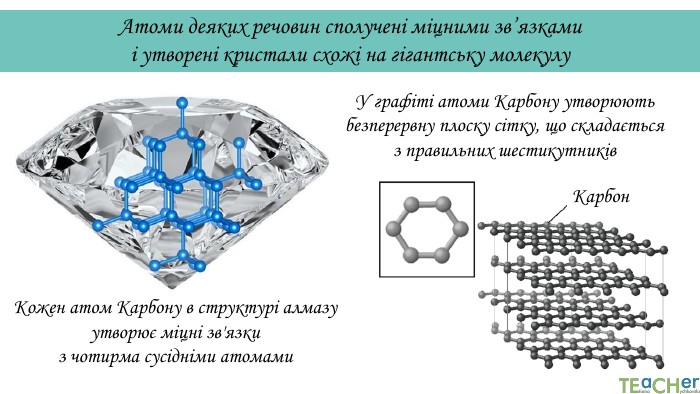
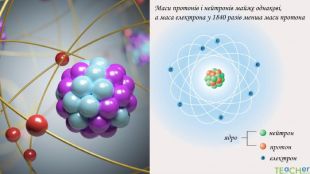
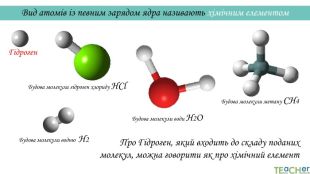
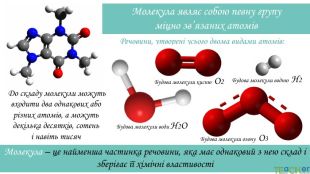
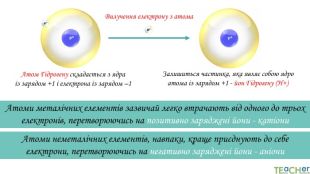
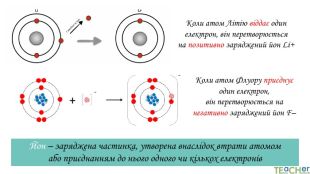
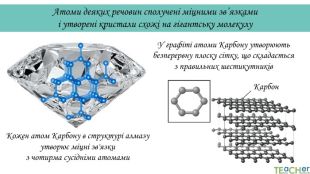
У презентації подано такі основні початкові поняття хімії, як тіло, матеріал, речовина, молекула, атом. Розглянуто будову атома. Слайди проілюстровано прикладами. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



























-

Полещук Сабіна
05.08.2025 в 19:09
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шкідченко Надія Миколаївна
01.02.2025 в 13:07
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Дудченко Алла
17.12.2024 в 16:43
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бурдейна Вікторія
10.06.2024 в 17:42
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Безсонова Оксана
18.09.2023 в 17:49
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пономаренко Лина
13.09.2023 в 02:09
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Кошелюк Катя
07.01.2023 в 12:12
Загальна:
4.3
Структурованість
4.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Паюк Ольга Миколаївна
25.09.2022 в 17:57
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Хворостяна Вікторія
21.09.2022 в 17:41
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Горбанева Ольга
19.09.2022 в 22:48
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Рабієвська Любов Анатоліївна
18.09.2022 в 20:39
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
14.09.2022 в 19:27
Дуже дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Виноградова Оксана Михайлівна
07.09.2022 в 20:13
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Івкова Юлія Олександрівна
05.09.2022 в 12:38
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 11 відгуків