Презентація до уроку "Прості та складні речовини. Хімічні формули"
Про матеріал
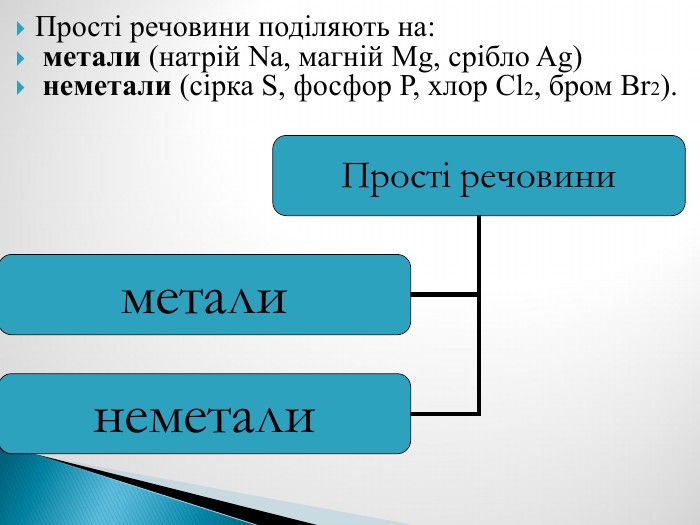
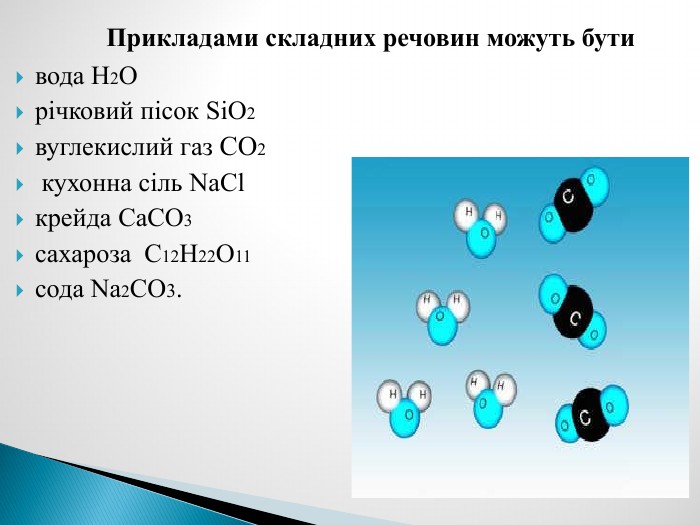
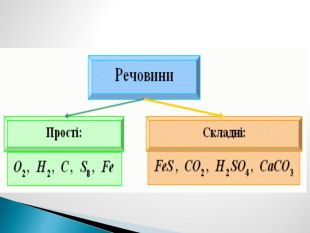
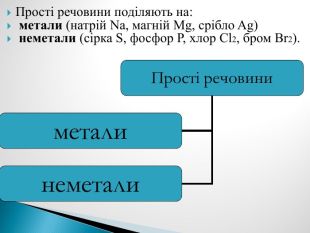
Презентація до уроку хімії в 7 класі , тема "Прості та складні речовини. Хімічні формули", розроблено за підручником "Хімія 7 клас" П.Попель
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку