Презентація до уроку: "Розчин і його компоненти"
Про матеріал
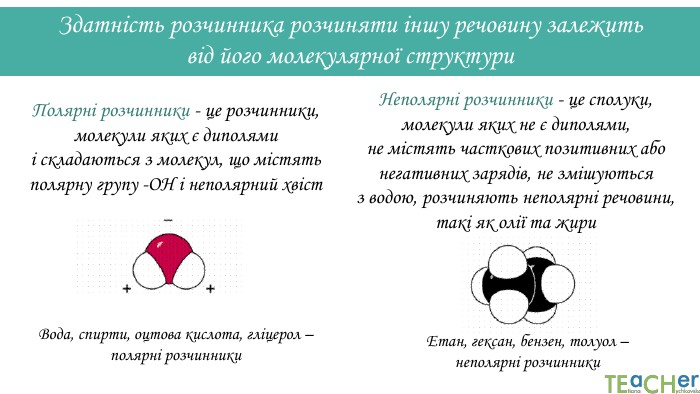
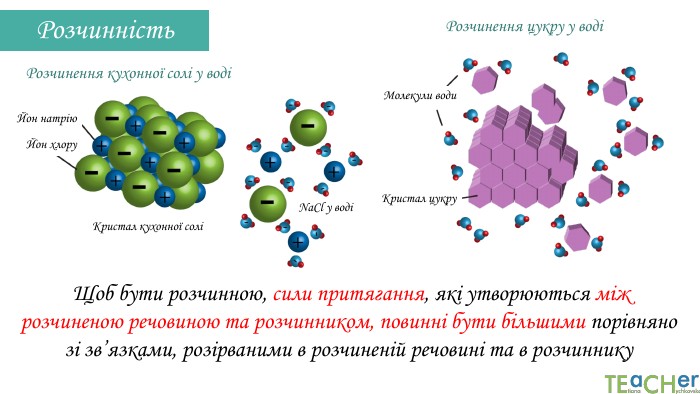
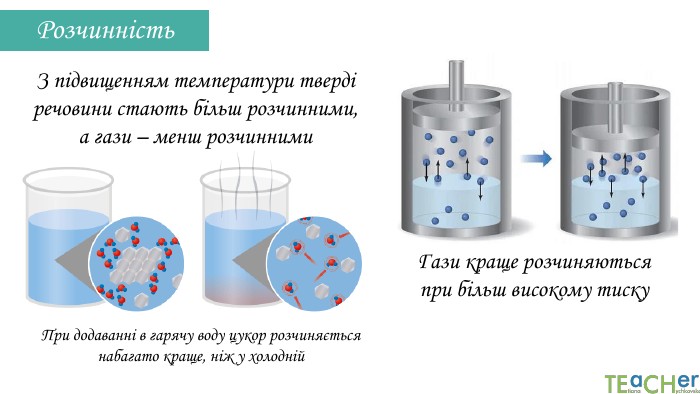
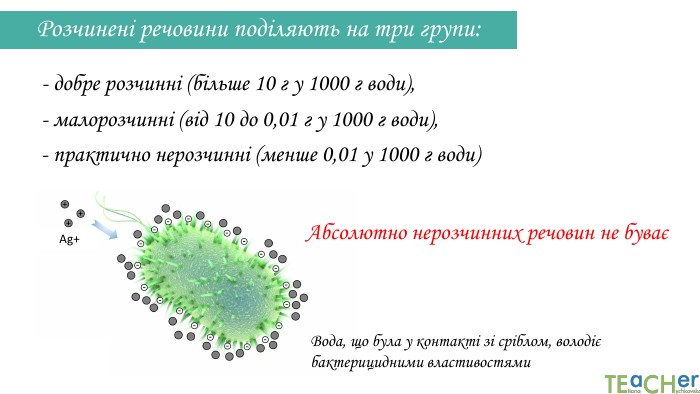
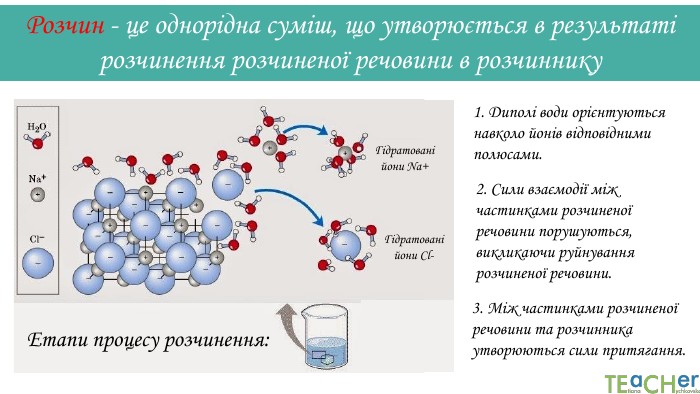
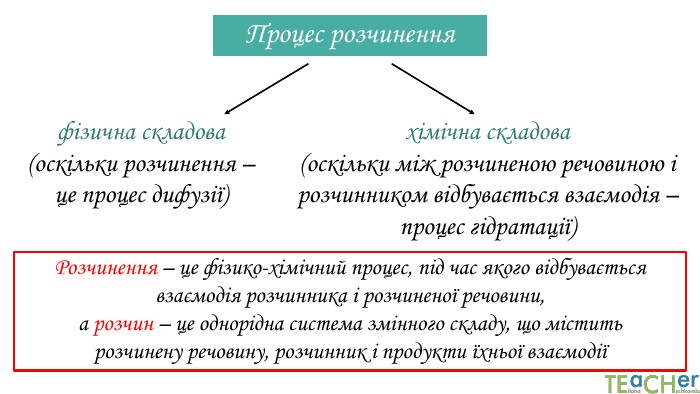
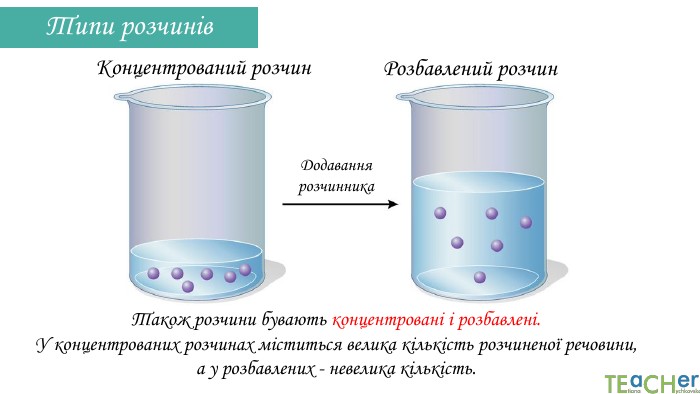
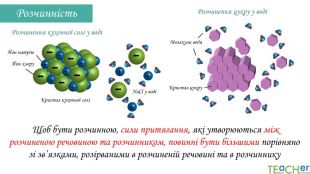
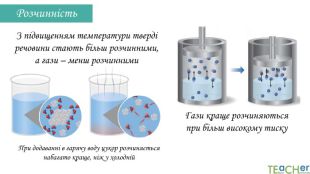
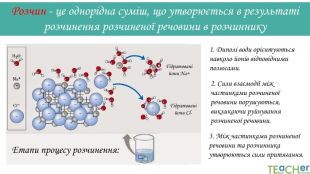
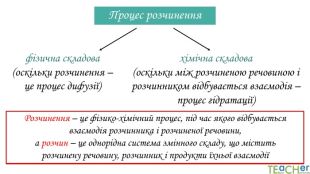
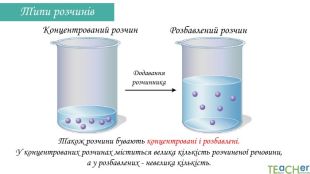
У презентації подано поняття розчинника. розчиненої речовини, розчину, показано етапи процесу розчинення, типи розчинів. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



























-

Юзьвяк Любов Михайлівна
15.04.2024 в 14:52
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Gaydova Oxana
01.04.2024 в 18:08
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Гурєєва Ольга В'ячеславівна
26.03.2024 в 11:46
Дякую! Ви супер!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Остаповець Юрій
06.03.2024 в 18:57
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шатовський Валентин Олександрович
22.02.2024 в 06:47
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Кострова Тетяна Маратівна
13.03.2023 в 17:01
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Лупол Людмила Анатоліївна
08.03.2023 в 16:41
дякую за те, що ділитесь своєю працею!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Орловська Наталія Вікторівна
05.03.2023 в 23:03
Чудові ваші презентації. Дякую за можливість ними користуватись .
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
02.03.2023 в 19:06
Дуже дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Хворостяна Вікторія
02.03.2023 в 08:56
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 7 відгуків