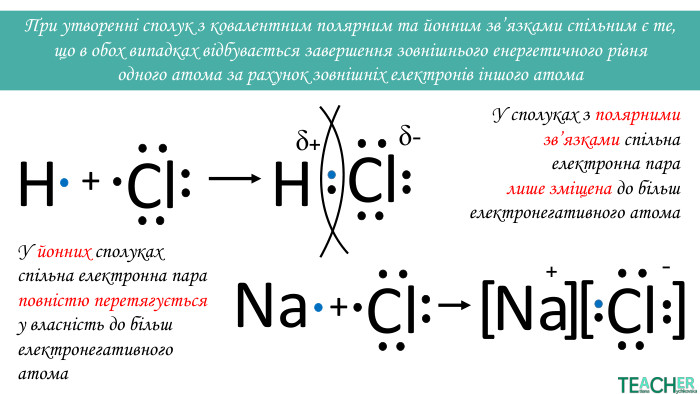
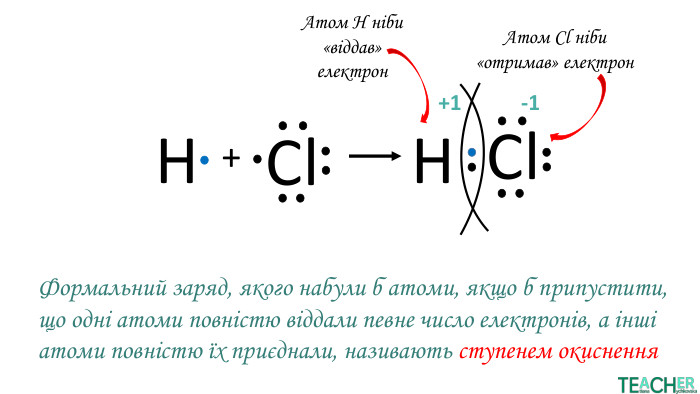
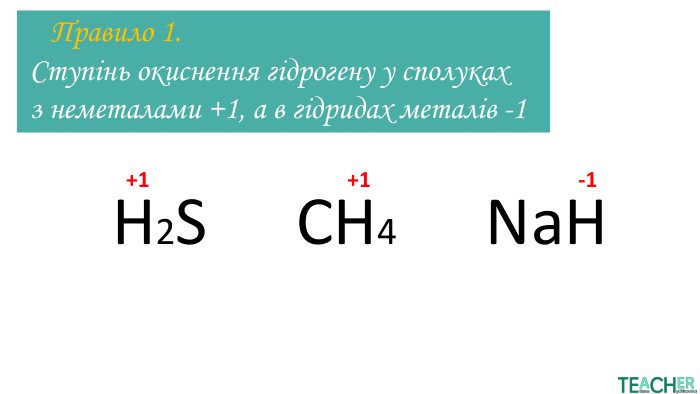
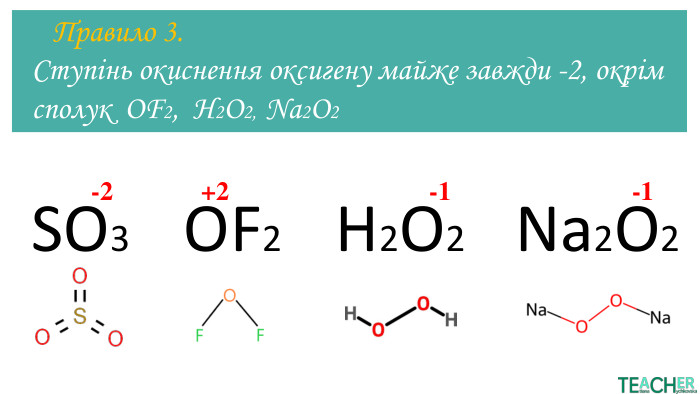
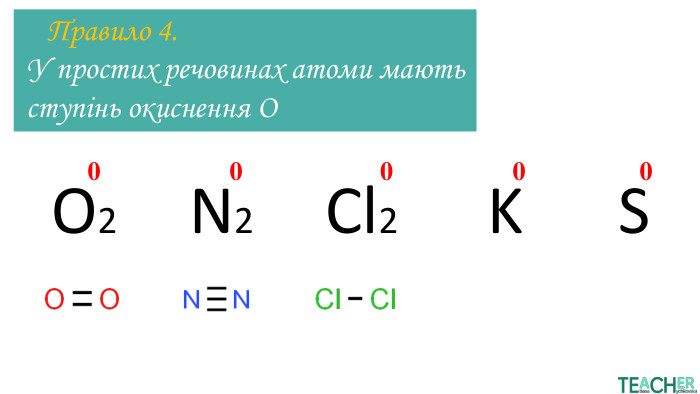
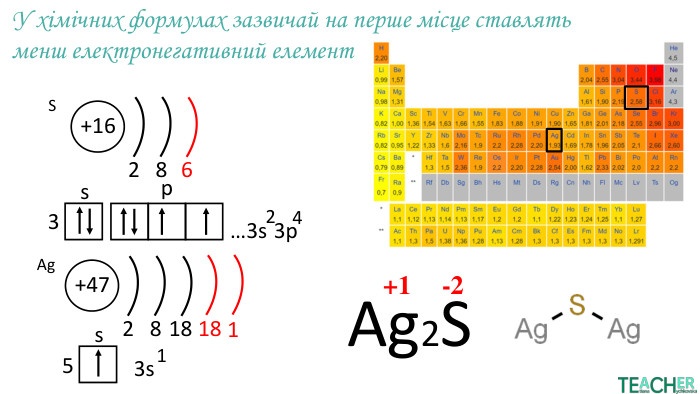
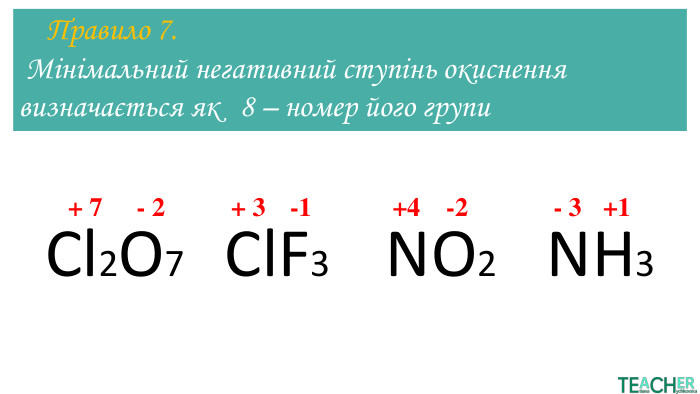
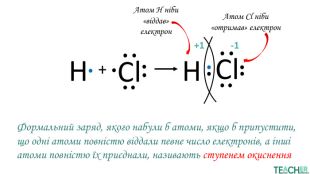
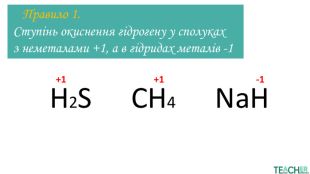
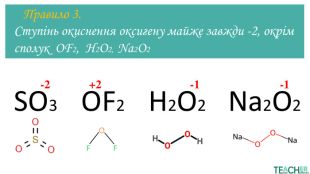
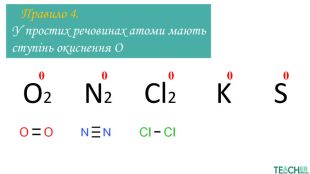
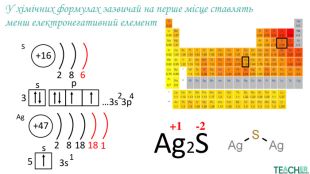
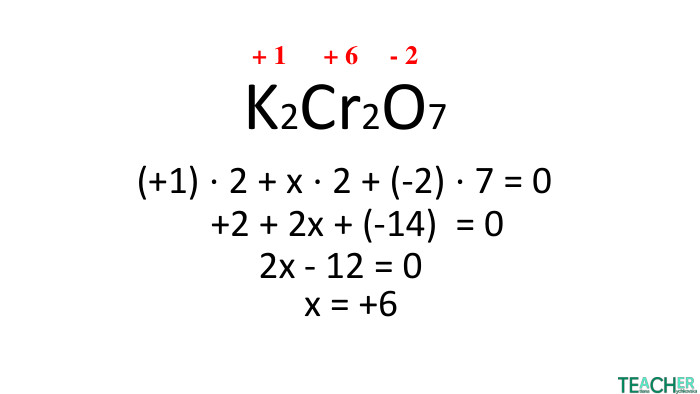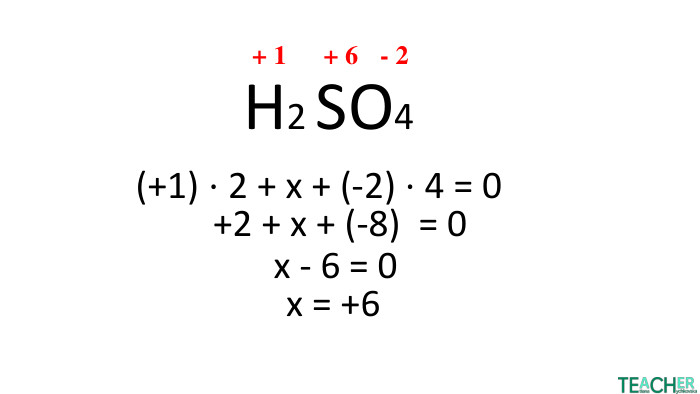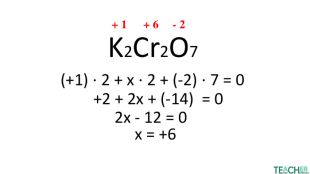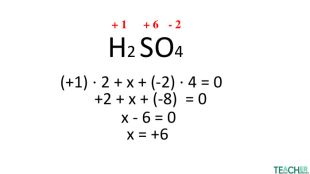Презентація до уроку: "Ступінь окиснення"
Про матеріал
У презентації докладно представлено тему Ступінь окиснення. Матеріал стане у нагоді вчителям під час дистанційного навчання. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дуже дякую!
-


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку