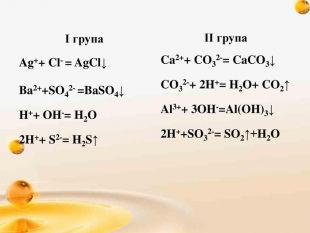
Презентація до уроку "Узагальнення і систематизація знань з теми Розчини"
Про матеріал
Презентація до конспекту уроку "Узагальнення і систематизація знань з теми Розчини". Урок містить різні форми роботи включаючи інтерактивні.
Перегляд файлу
Зміст слайдів
ppt
До підручника
Хімія 9 клас (Савчин М.М.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку