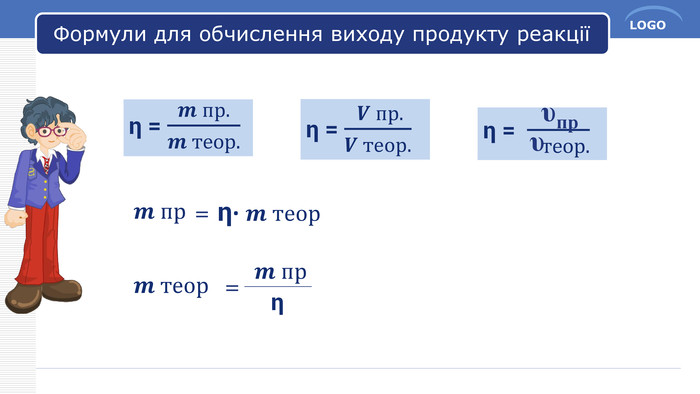
Презентація до уроку в 11 класі "Обчислення за хімічними рівняннями відносного виходу продукту реакції"
Про матеріал
Презентація до уроку в 11 класі "Обчислення за хімічними рівняннями відносного виходу продукту реакції". Використати під час дистанційного навчання. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку






















-

Литвинова Олеся Миколаївна
18.12.2024 в 08:21
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Потапова Галина Іванівна
12.11.2024 в 21:03
дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Земелько Катерина Олександрівна
07.11.2024 в 23:10
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Зінченко Наталія Миколаївна
04.11.2024 в 21:31
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Лійко Світлана
03.10.2024 в 18:11
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Кичук Світлана
16.04.2024 в 09:37
Дякую!
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Ковіна Ольга Юріївна
27.11.2023 в 12:46
Дуже дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Смакоуз Тамара Василівна
04.11.2023 в 19:11
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шапошнікова Ілона Михайлівна
29.11.2022 в 21:23
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бабак Лідія Дмитрівна
21.11.2022 в 22:02
Дякую. Пригодилось все
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Велика Наталія Миколаївна
06.11.2022 в 19:58
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Шкот Світлана
29.10.2022 в 19:24
дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Солод Ольга Олексіївна
28.10.2022 в 22:28
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Grigorjeva Anna
12.12.2021 в 21:31
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Прищенко Тетяна Іванівна
09.12.2021 в 10:39
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Переверзєва Інна
27.11.2021 в 23:35
Дякую за допомогу
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Виноградова Оксана Михайлівна
17.11.2021 в 22:59
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
4.0
-

Комлєва Олена Олексіївна
01.11.2021 в 01:41
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 15 відгуків