Презентація: "Хімічні властивості насичених одноатомних спиртів. Одержання етанолу"
Про матеріал
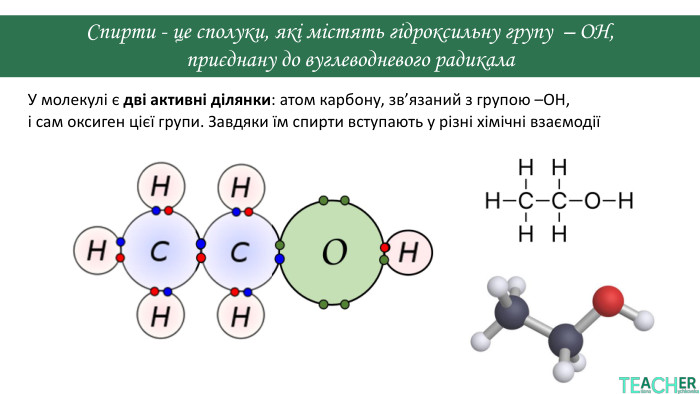
Презентація познайомить учнів із хімічними властивостями насичених одноатомних спиртів на прикладі етанолу.
Розглянуто основні типи хімічних реакцій, характерних для спиртів:
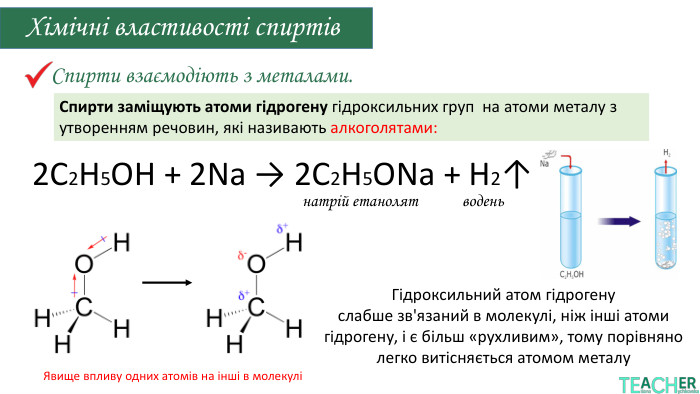
реакції з активними металами (утворення алкоголятів),
взаємодія з галогеноводнями (одержання галогеналканів),
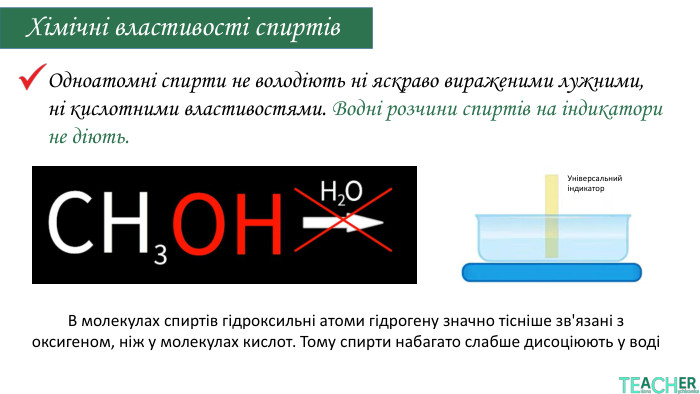
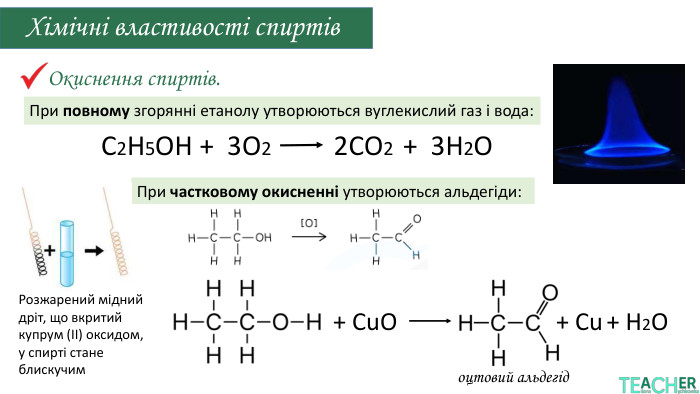
окиснення (повне, часткове),
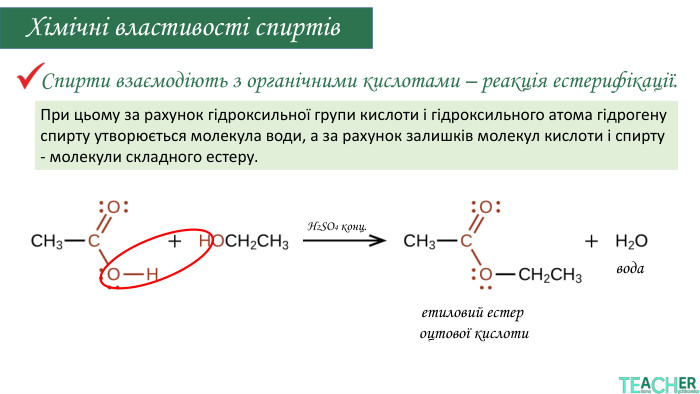
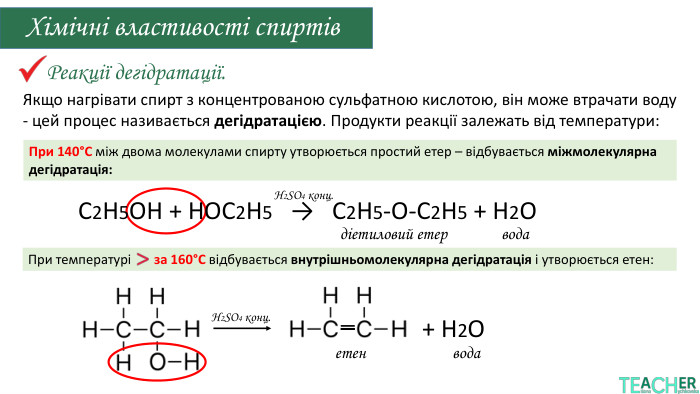
дегідратація (одержання етену або простих етерів).
Окремий розділ присвячено способам одержання етанолу.
Матеріал супроводжується схемами реакцій, рівняннями та ілюстраціями, які допомагають учням краще зрозуміти взаємозв’язок між будовою молекули та її реакційною здатністю. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дуже вдячна!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку