Презентація «Ізотопи» 8 клас
Про матеріал
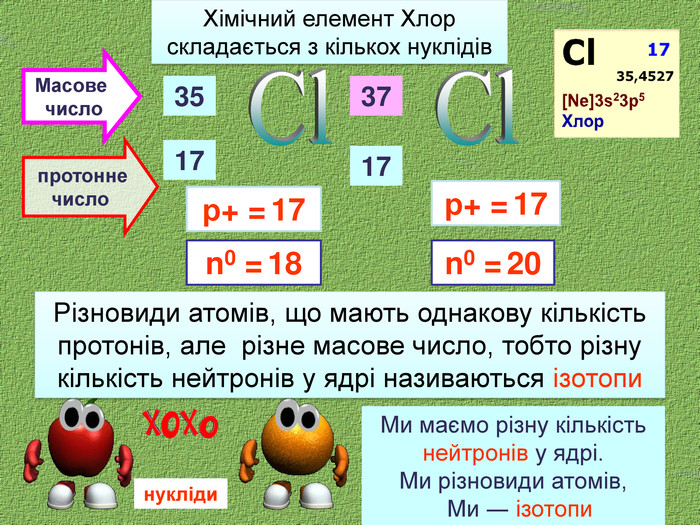
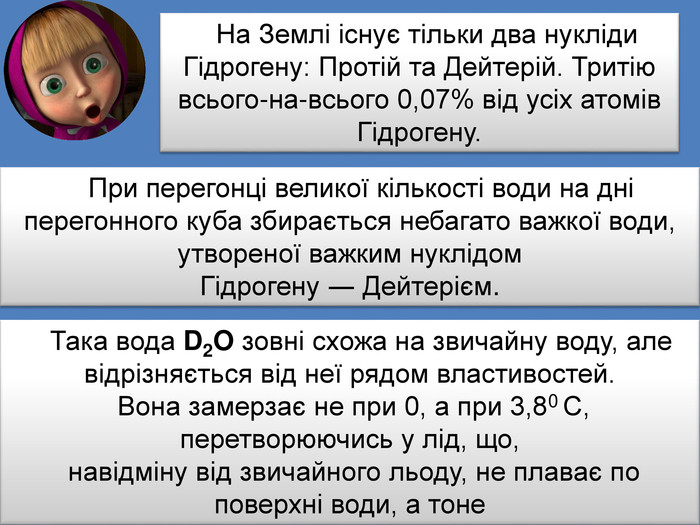
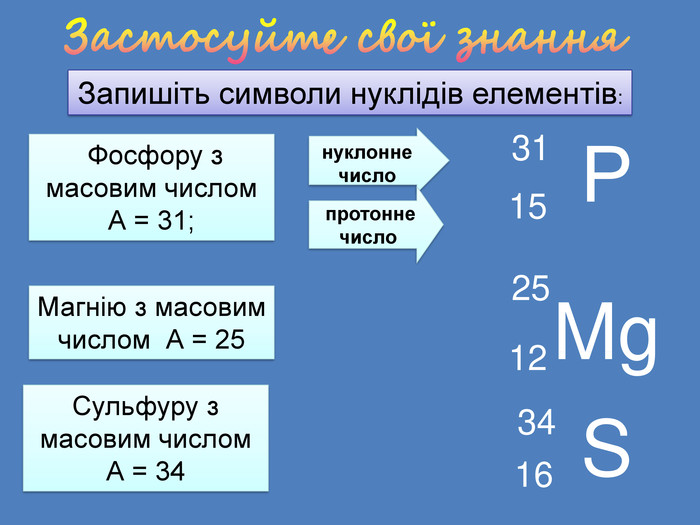
| Презентація допоможе учням та вчителю при проведенні уроку на тему: «Нукліди. Ізотопи» (§10) |
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку
































-

Юсин Надія Улянівна
03.10.2023 в 21:11
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Чоп Наталя
25.09.2023 в 18:34
Дякую!!!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Гайдук Катерина Віталіївна
02.10.2022 в 17:47
Дякую, за можливість скористатися вашою презентацією. Логічно і структуровано побудована, дуже ефективно використовується під час дистанційного навчання.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Товстолес Лариса
27.09.2022 в 21:34
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Оксана Проценко Григорівна
25.09.2022 в 12:06
щиро дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ковтун Тетяна Петрівна
20.01.2021 в 11:02
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 3 відгука