Презентація "Кальцій гідроксид"
Про матеріал
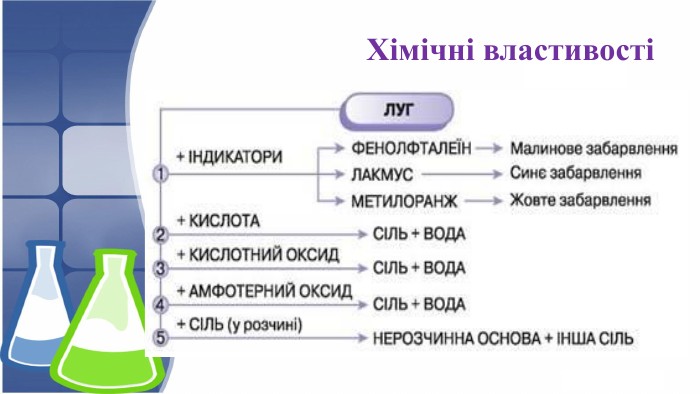
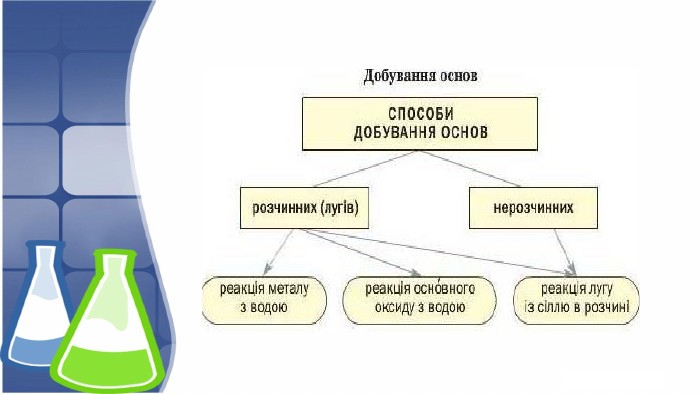
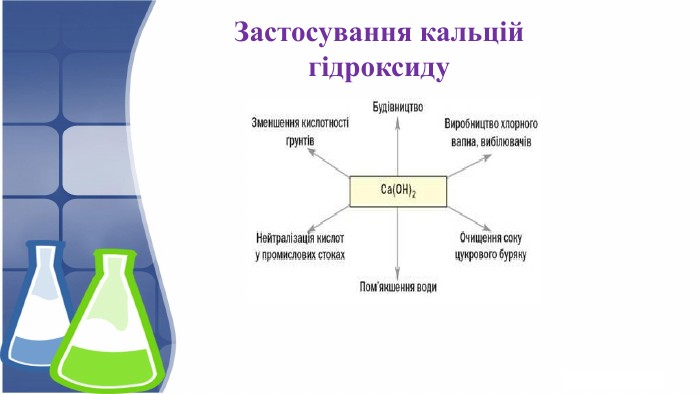
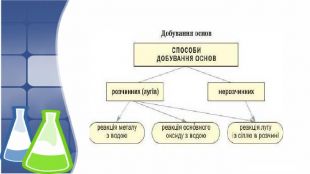
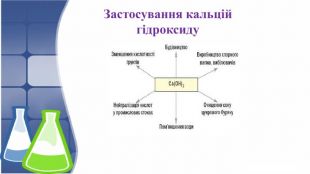
Презентація розкриває будову, фізичні та хімічні властивості кальцій гідроксиду; висвітлює способи добування та використання гідроксиду. Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку