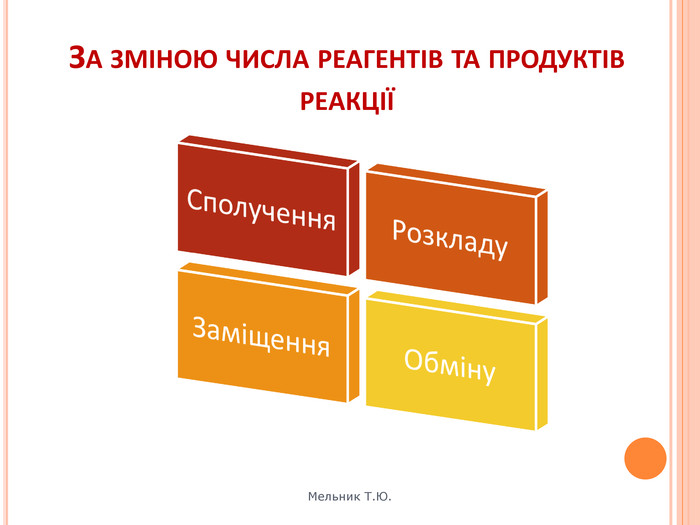
. Презентація "Класифікація хімічних реакцій"
Про матеріал
Презентація до уроків хімії з теми "Хімічні реакції" 9 клас. Презентацію можна використати під час підготовки до уроку (метод перевернутий клас) так і під час уроку. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку