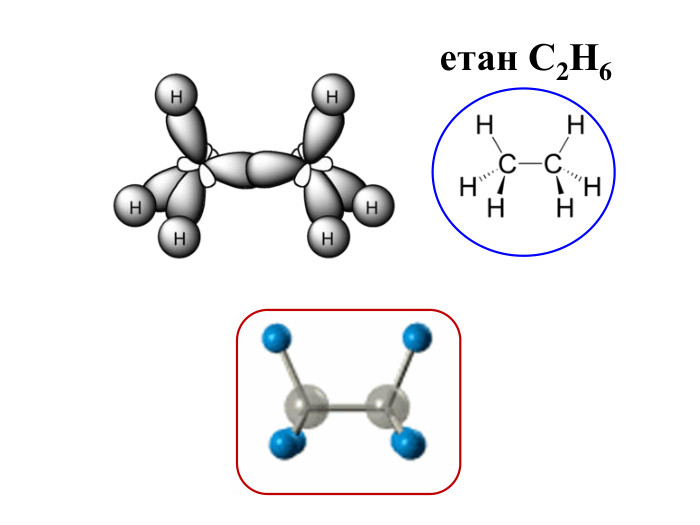
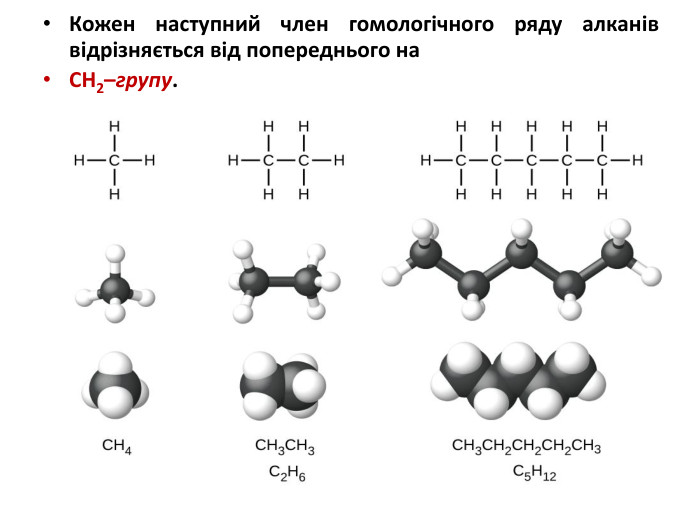
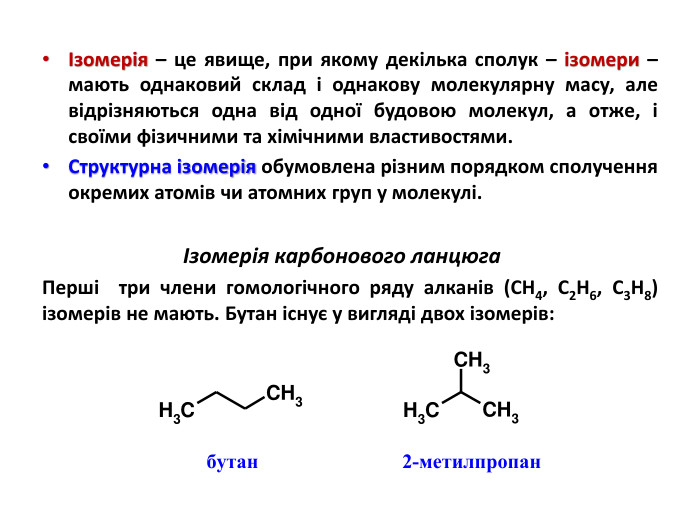
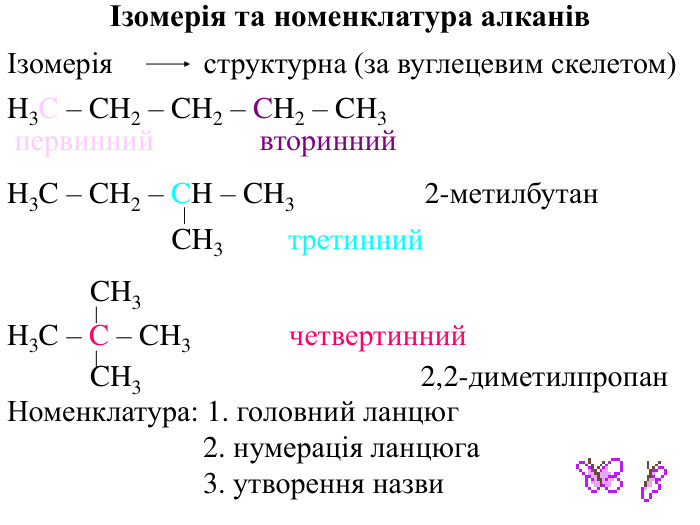
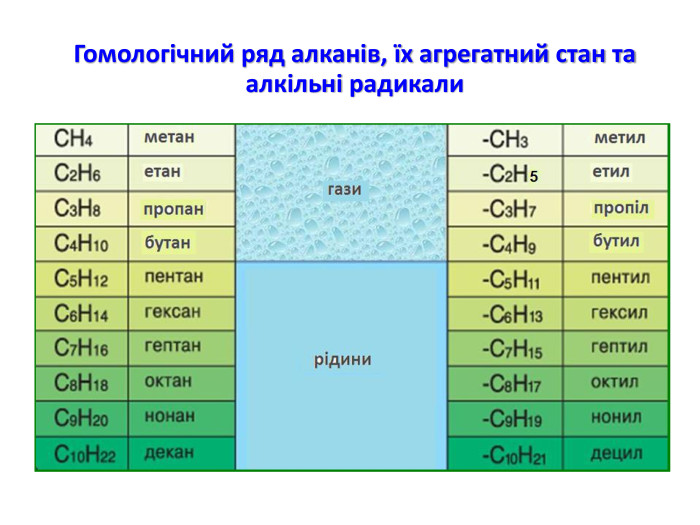
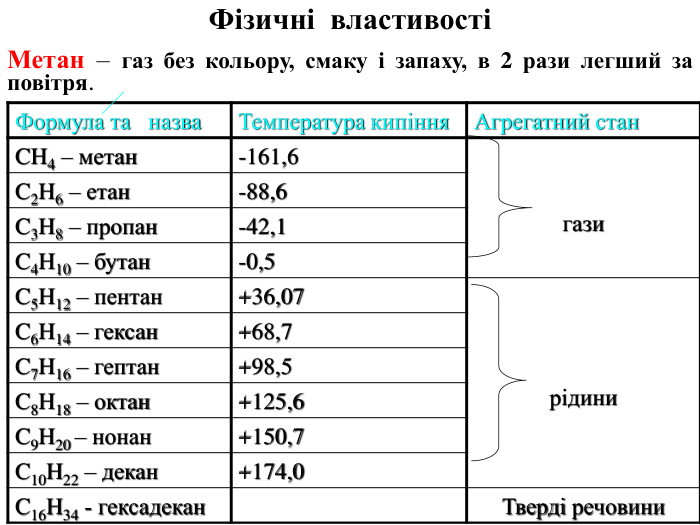
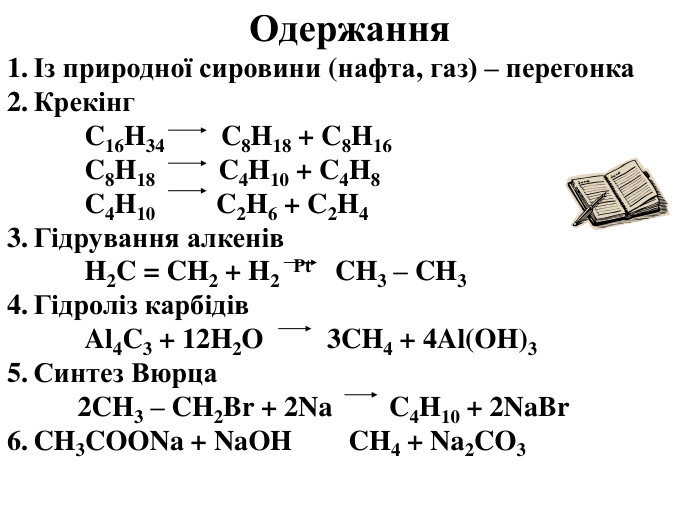
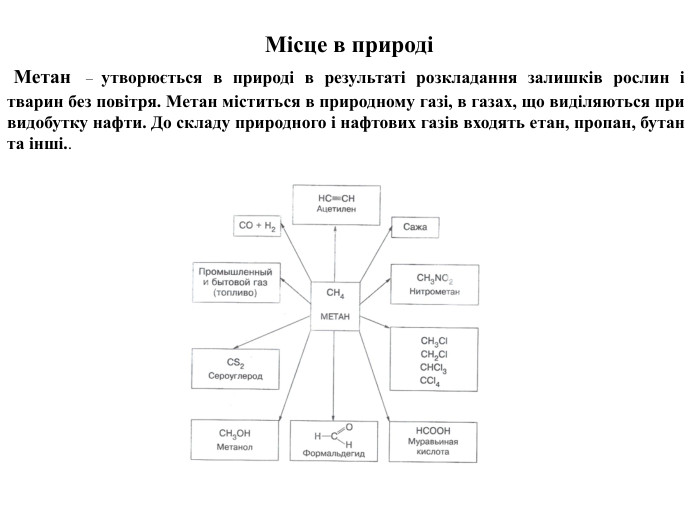
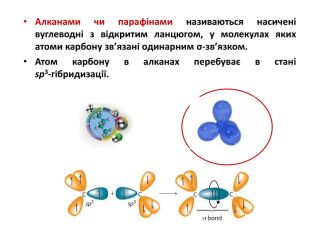
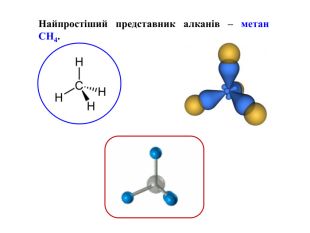
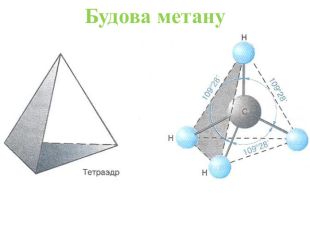
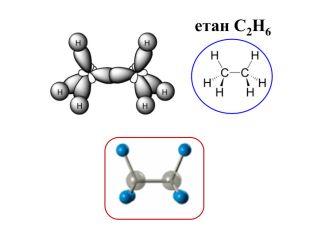
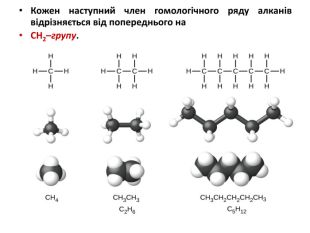
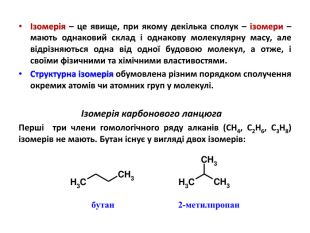
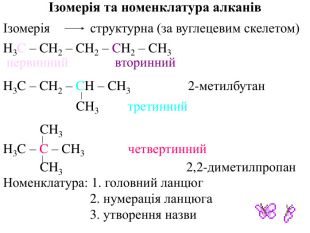
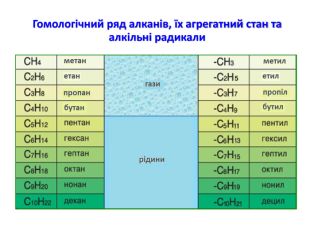
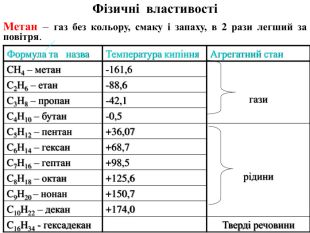
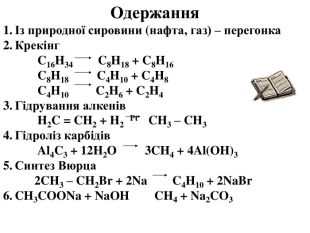
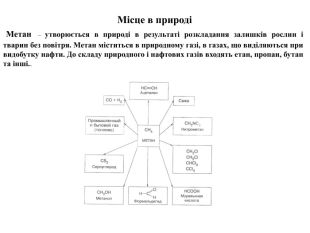
Презентація на тему "Алкани, загальна формула алканів, ізомерія, номенклатура"
Про матеріал
Презентація з хімії до уроку по темі "Алкани, загальна формула, ізомерія, номенклатура". Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
дякую!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку