Презентація на тему: " Хімічні рівняння"
Про матеріал
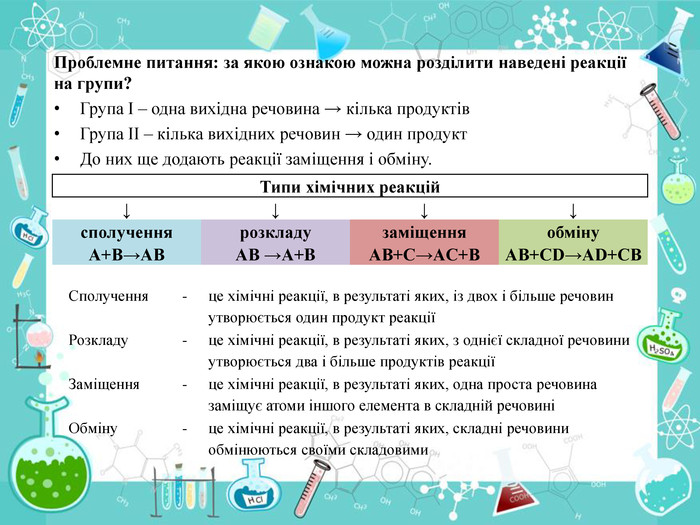
Навчити учнів складати хімічні рівняння, дотримуючись закону збереження маси речовини,зрівнюючи коефіцієнти. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку