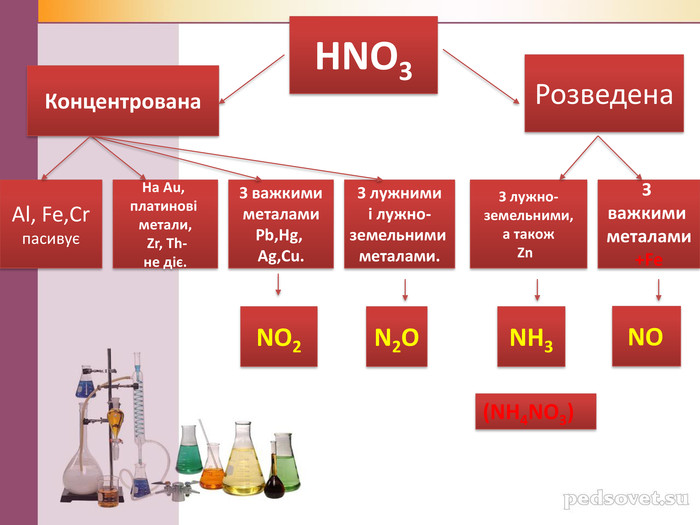
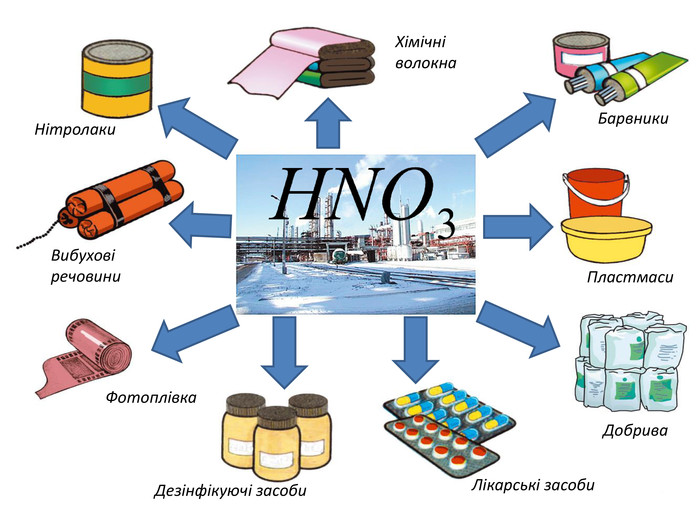
Презентація на тему "Нітратна кислота.Нітрати: проблема їх вмісту у прподуктах харчування"
Про матеріал
Презентація на тему "Нітратна кислота.Нітрати: проблема їх вмісту у прподуктах харчування". До презентації є розробка відповідногот уроку Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку